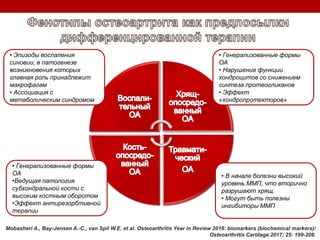
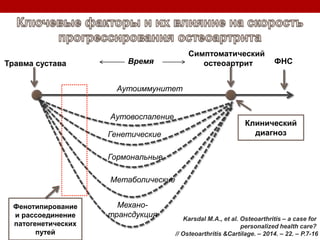
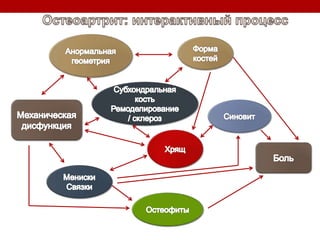
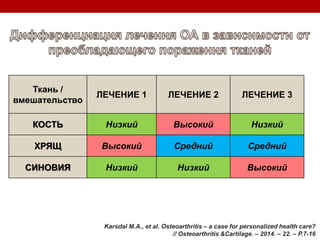
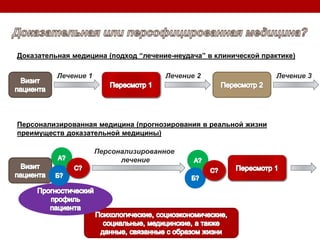
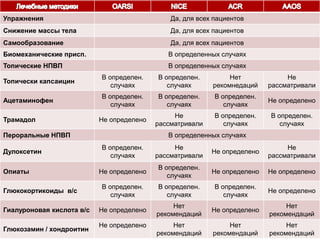
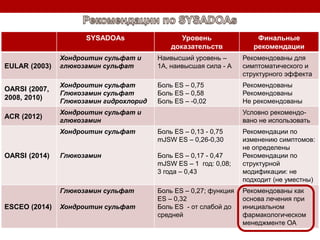
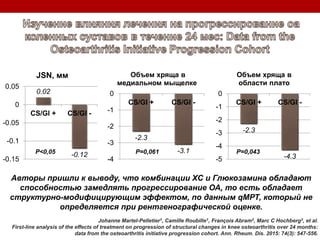
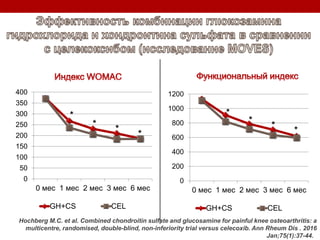
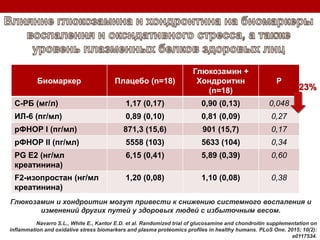
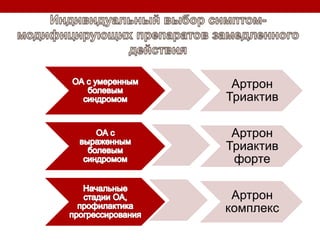
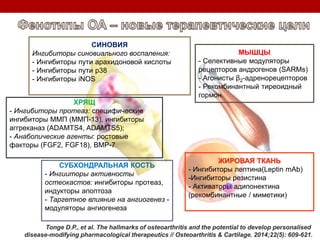
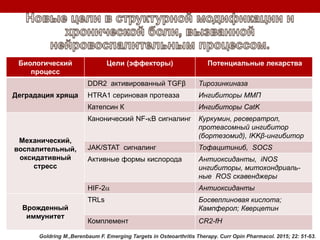
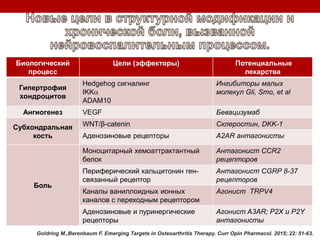
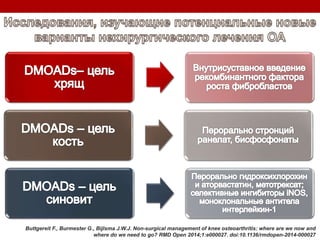
Остеоартрит – это заболевание суставов, вызванное клеточным стрессом и деградацией экстрацеллюлярного матрикса, что приводит к нарушению функции суставов. Заболевание требует индивидуального подхода в лечении, включая использование биомаркеров и целенаправленные терапии, направленные на различные аспекты патогенеза. Эффективность различных методов лечения, включая комбинированную терапию хондроитином и глюкозамином, была исследована, и результаты показывают необходимость клинического пересмотра подходов к лечению.