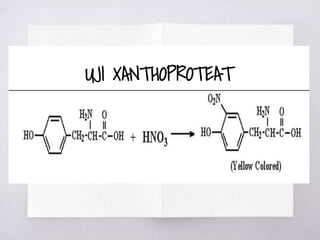
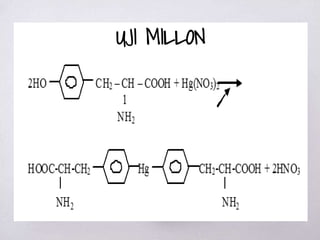
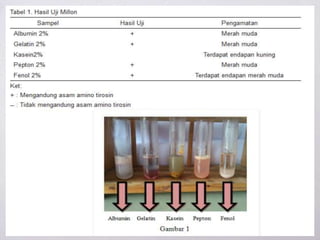
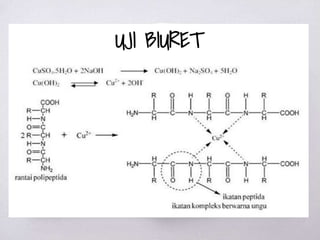
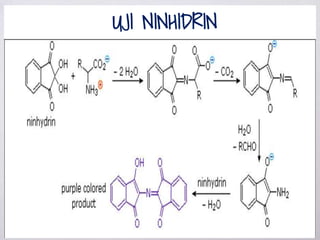
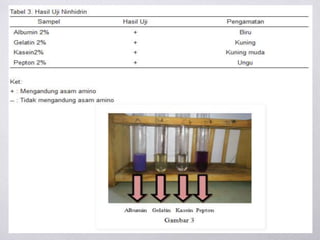
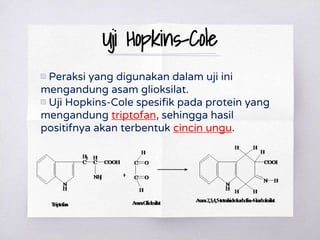
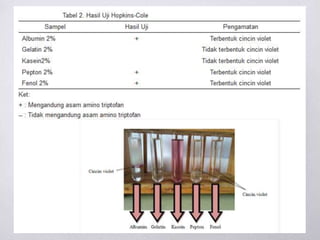
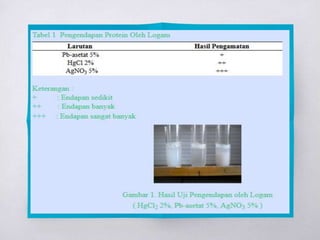
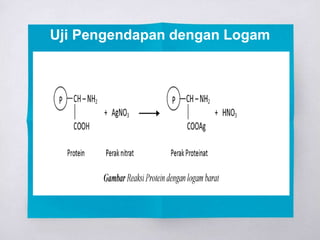
Dokumen ini membahas berbagai metode uji untuk mendeteksi keberadaan protein dan asam amino, termasuk uji xantoproteat, Millon, biuret, ninhidrin, dan uji belerang. Setiap uji memiliki reagen spesifik dan hasil yang memberikan indikasi kualitas dan jenis protein yang ada. Selain itu, dijelaskan juga tentang pengendapan protein dengan ion logam berdasarkan pH larutan.