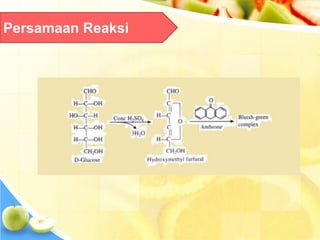
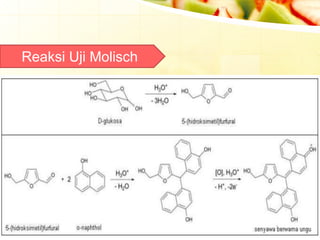
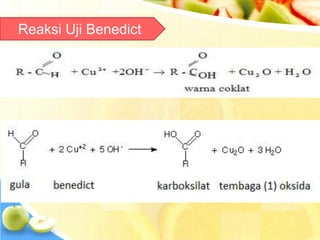
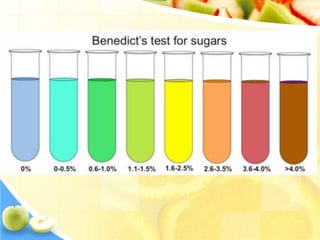
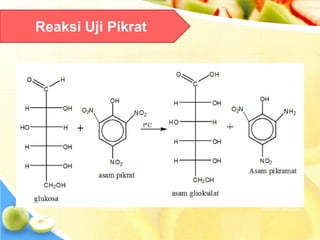
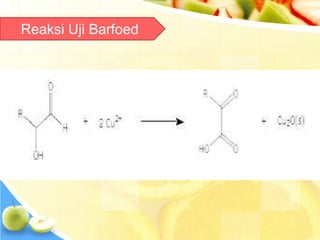
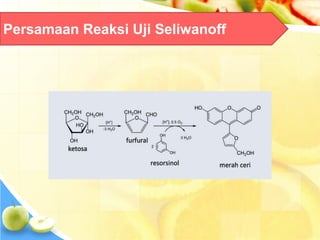
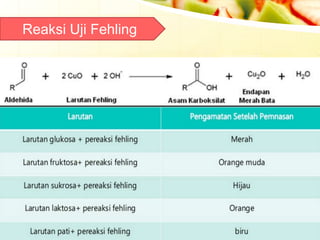
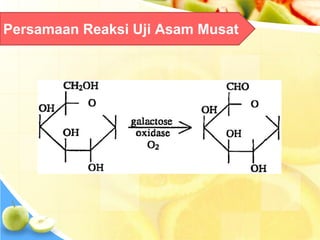
Dokumen tersebut memberikan ringkasan singkat tentang berbagai uji untuk menganalisis karbohidrat, termasuk uji untuk mendeteksi gula, monosakarida, ketosa, aldosa, galaktosa, dan amilum. Berbagai uji tersebut melibatkan reaksi kimia yang menghasilkan perubahan warna yang menunjukkan kehadiran jenis karbohidrat tertentu.