Ankenict
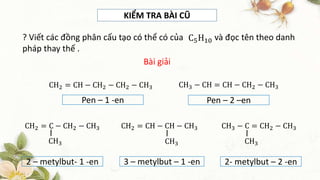
- 1. KIỂM TRA BÀI CŨ ? Viết các đồng phân cấu tạo có thể có của và đọc tên theo danh pháp thay thế . C5H10 CH2 = CH − CH2 − CH2 − CH3 Bài giải CH3 − CH = CH − CH2 − CH3 Pen – 1 -en Pen – 2 –en 2 – metylbut- 1 -en 3 – metylbut – 1 -en 2- metylbut – 2 -en CH2 = C − CH2 − CH3 CH3 CH2 = CH − CH − CH3 CH3 CH3 − C = CH2 − CH3 CH3
- 2. BÀI 40: ANKEN TÍNH CHẤT, ĐIỀU CHẾ VÀ ỨNG DỤNG
- 3. II III I TÍNH CHẤT VẬT LÍ TÍNH CHẤT HÓA HỌC ĐIỀU CHẾ VÀ ỨNG DỤNG NỘI DUNG BÀI HỌC
- 4. I. TÍNH CHẤT VẬT LÍ 1. Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng CH2 = CH2 CH2 = CH − CH3 CH2 = CH − CH2 − CH3 CH3 − CH2 − CH2 − CH3 CH3 − CH2 − CH3 CH3 − CH3 C3H6 C4H8 C5H10 CH2 = CH − CH2 − CH2 − CH3 CH3 − CH2 − CH2 − CH2 − CH3 ANKEN XICLOANKANANKAN Điểm giống về cấu tạo của anken so với các hidrocacbon đã học?
- 5. I. TÍNH CHẤT VẬT LÍ 1. Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng Tăng theo khối lượng mol phân tử. Không khác nhiều so với ankan tương ứng. Thường nhỏ hơn xicloankan có cùng số C. Nhẹ hơn nước.
- 6. I. TÍNH CHẤT VẬT LÍ 2. Tính tan và màu sắc Trình bày tính tan và màu sắc của anken? Không tan trong nước. Tan tốt trong dầu mỡ. Không màu.
- 7. II. TÍNH CHẤT HÓA HỌC Đặc điểm cấu tạo của anken? 𝜋 σ Dự đoán tính chất hóa học của anken?
- 8. II. TÍNH CHẤT HÓA HỌC → −C − C − 𝐑 𝟏 𝐑 𝟐 𝐑 𝟒 𝐑 𝟑 Phản ứng hóa học đặc trưng của anken như phản ứng cộng, phản ứng trùng hợp và phản ứng oxi hóa.
- 9. II. TÍNH CHẤT HÓA HỌC 1. Phản ứng cộng halogen Quan sát thí nghiệm giữa khí etilen và dung dịch brom.
- 11. II. TÍNH CHẤT HÓA HỌC 1. Phản ứng cộng halogen −C − C − 𝐑 𝟏 𝐑 𝟐 𝐑 𝟒 𝐑 𝟑 + Br - Br Br Br→
- 12. II. TÍNH CHẤT HÓA HỌC 1. Phản ứng cộng halogen CH2 = CH2 + Br2→BrCH2– CH2Br CH2 = CH − CH3 + Br2→BrCH2– CHBr − CH3 Phương trình tổng quát: CnH2n + X2→CnH2nX2 Chú ý: Anken làm mất màu của nước brom, do đó người ta thường sử dụng nước brom hoặc dung dịch brom trong CCl4 để nhận biết anken.
- 13. II. TÍNH CHẤT HÓA HỌC 2. Phản ứng cộng hidro CH2 = CH2 + H2 Ni,to CH3– CH3 CH2 = CH − CH3 + H2 Ni,to CH3– CH2 − CH3 Phương trình tổng quát: CnH2n + H2 Ni,to CnH2n+2 Anken phản ứng với H2 khi có mặt xúc tác như Ni, Pt, Pd ở nhiệt độ thích hợp.
- 14. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước a) Cộng axit Cơ chế phản ứng cộng axit vào anken C = C + 𝐇 − 𝐀 → C − C H − + − −A− GĐ 1
- 15. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước a) Cộng axit Cơ chế phản ứng cộng axit vào anken GĐ 2 C − C H − + − + A− → C − C H − − A
- 16. C = C + 𝐇 − 𝐀 → C − C H − − II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước a) Cộng axit A CH2 = CH2 + H − Cl → CH3 − CH2 − Cl CH2 = CH2 + H − OSO3H → CH3 − CH2− OSO3H Ví dụ:
- 17. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước b) Cộng nước CH2 = CH2 + H − OH H+,t0 HCH2 − CH2OH Ví dụ
- 18. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước c) Hướng của phản ứng cộng axit và cộng nước vào anken CH2 = CH − CH3 + 𝐇 − 𝐂𝐥 → CH2 − CH − CH3 CH2 − CH − CH3+ HCl ClH H CH2 = C − CH3 + 𝐇 − 𝐎𝐇 H+,t0 CH2 − C − CH3 CH2 − C − CH3+ OH H OHCH3 CH3CH3 Làm thế nào để xác định được sản phẩm chính và sản phẩm phụ trong hỗn hợp sản phẩm trên?
- 19. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước c) Hướng của phản ứng cộng axit và cộng nước vào anken Trong phản ứng cộng axit hoặc nước (kí hiệu chung là HA) vào liên kết đôi C=C của anken, nguyên tử H (phần tử mang điện tích dương) ưu tiên cộng vào C mang nhiều H hơn (cacbon bậc thấp hơn), còn A (phần mang điện tích âm) ưu tiên cộng vào C có ít H hơn (cacbon bậc cao hơn). Quy tắc Mac – côp – nhi – côp
- 20. II. TÍNH CHẤT HÓA HỌC 3. Phản ứng cộng axit và cộng nước c) Hướng của phản ứng cộng axit và cộng nước vào anken CH2 = CH − CH3 + 𝐇 − 𝐂𝐥 → CH2 − CH − CH3 CH2 − CH − CH3+ HCl ClH H CH2 = C − CH3 + 𝐇 − 𝐎𝐇 H+,t0 CH2 − C − CH3 CH2 − C − CH3+ OH H OHCH3 CH3CH3 SP chính SP chínhSP phụ SP phụ
- 21. II. TÍNH CHẤT HÓA HỌC 4. Phản ứng trùng hợp Phản ứng trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành những phân tử rất lớn gọi là polime. nCH2 = CH2 → 100 atm Peeoxit,100−3000C ( )CH2 − CH2 n nCH2 = CH CH3 𝑡0,𝑥𝑡 ( CH2 − CH ) CH3 n Polietilen Polipropilen
- 23. II. TÍNH CHẤT HÓA HỌC 5. Phản ứng oxi hóa Anken làm mất màu dung dịch Phản ứng đốt cháy KMnO4 3CH2 = CH2 + 2KMnO4 + 4H2O → 3HOCH2 − CH2OH + 2MnO2 + 2KOH Phản ứng làm mất màu thuốc tím của dung dịch được dùng để nhận biết sự có mặt của liên kết đôi anken KMnO4 CnH2n + 3n 2 O2 → nCO2 + nH2O
- 25. III. ĐIỀU CHẾ VÀ ỨNG DỤNG 1. Điều chế CH3CH2OH H2SO4,1700C CH2 = CH2 + H2O • Phản ứng điều chế etilen trong phòng thí nghiệm • Trong công nghiệp, etilen, propilen, butilen được điều chế bằng phản ứng tách hidro từ ankan tương ứng hoặc phản ứng crăckinh.
- 27. III. ĐIỀU CHẾ VÀ ỨNG DỤNG 2. Ứng dụng ANKEN
- 28. CỦNG CỐ VÀ DẶN DÒ Câu 1: Dẫn từ từ 6,72 lit (đktc) hỗn hợp X gồm etilen và propilen và dung dịch brom, dung dịch brom bị nhạt màu, và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tắng 9,8 gam. Thành phần phần trăm theo thể tích của etilen trong X là A.50,00% B. 66,67% C. 57,14% D. 28,57% Câu 2: Trùng hợp m tấn etilen thu được 1 tấn polietilen (PE) với hiệu suất phản ứng bằng 80%. Giá trị của m là A.1,25 B. 0,80 C. 1,80 D. 2,00
- 29. CỦNG CỐ VÀ DẶN DÒ HS về nhà học bài và làm bài tập trong SGK, chuẩn bị bài mới cho tiết học sau.