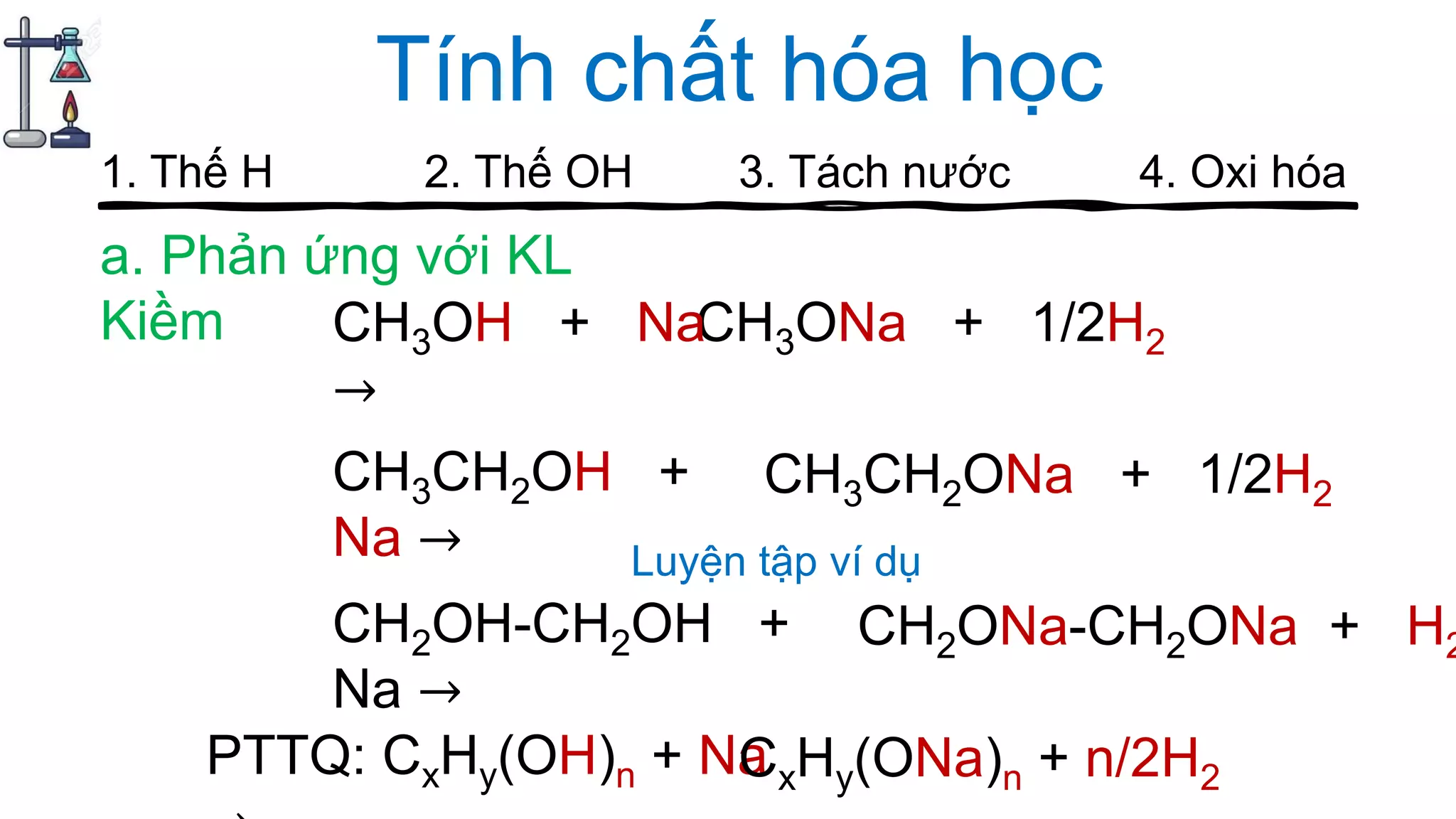
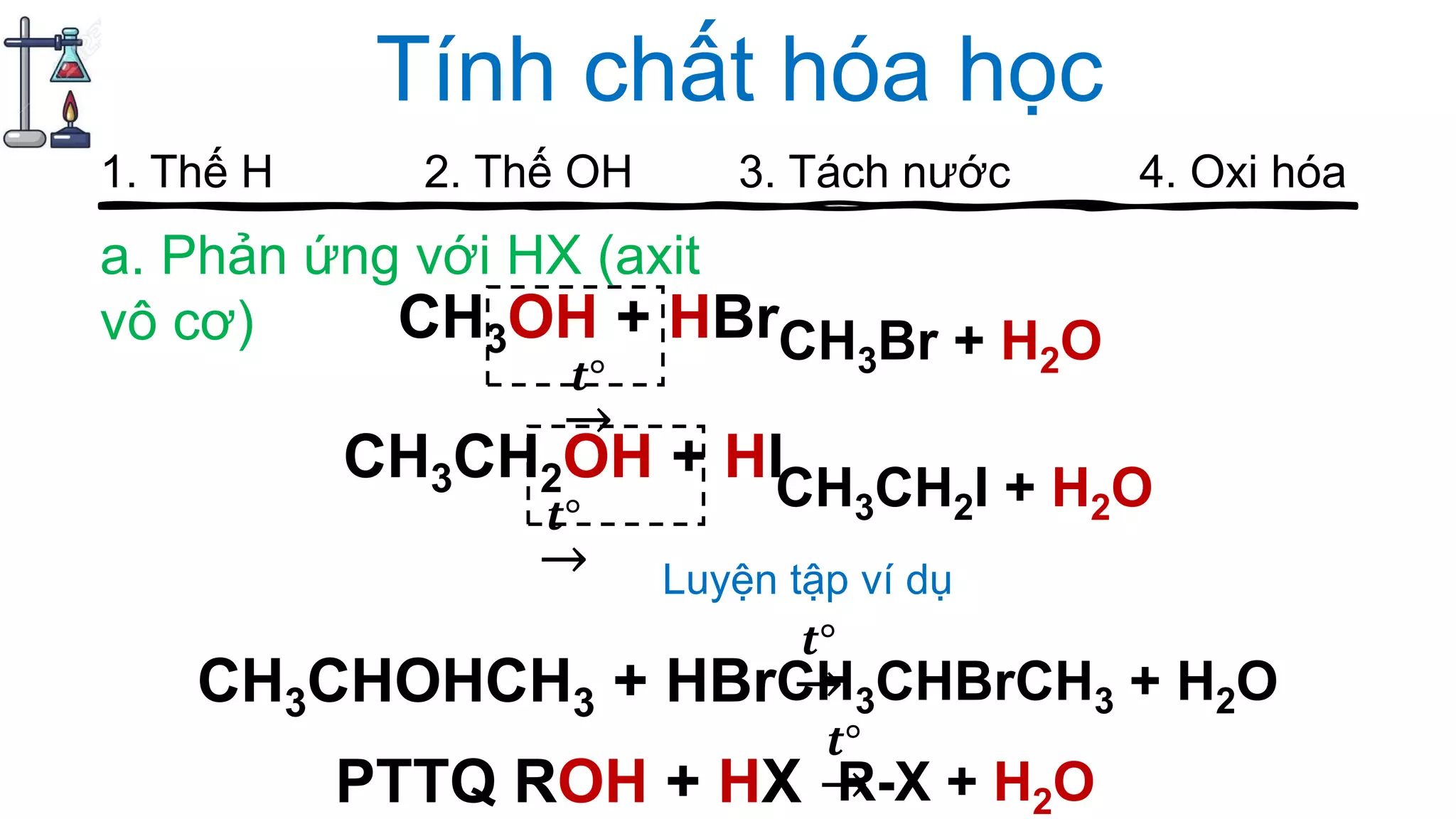
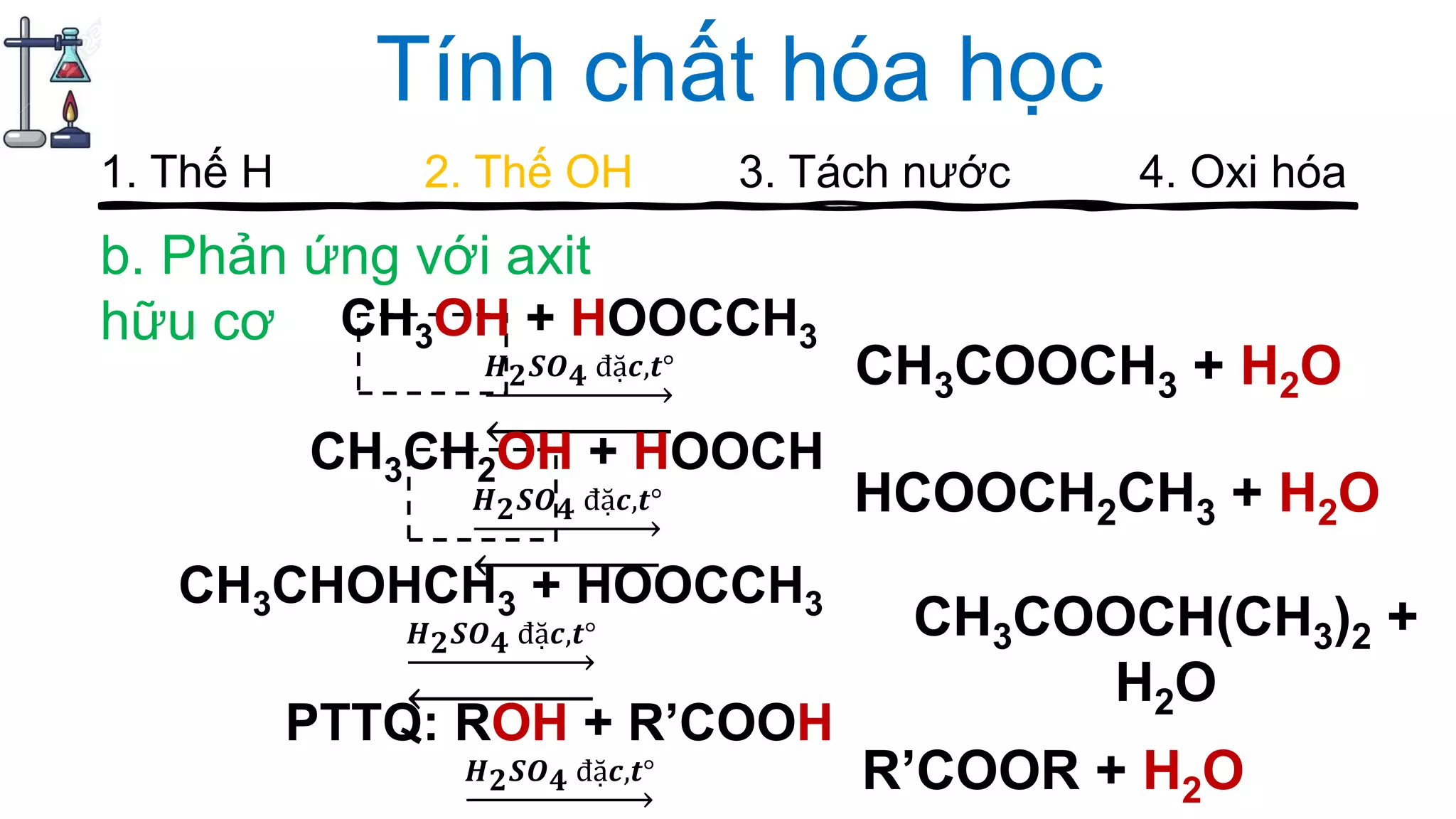
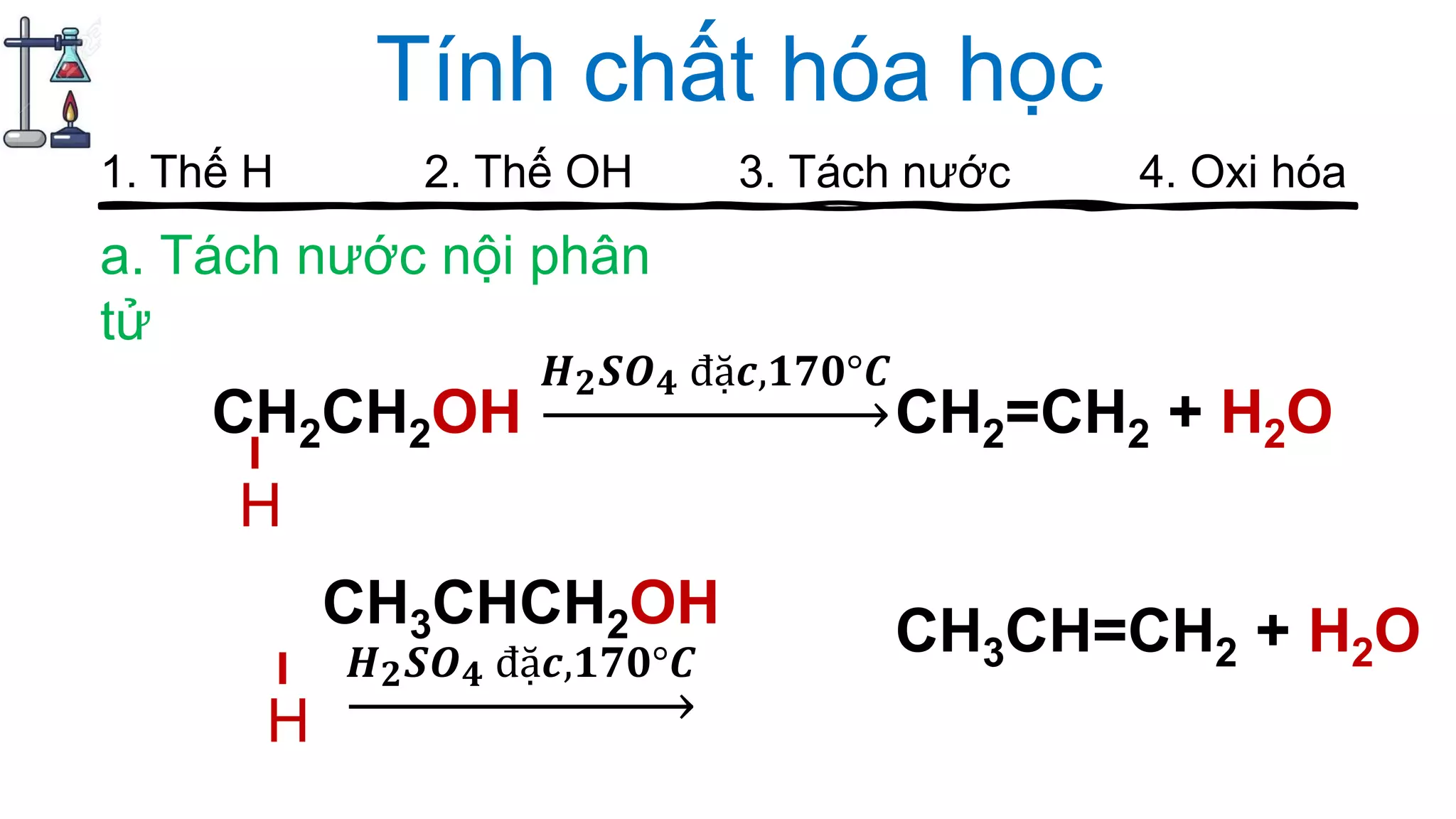
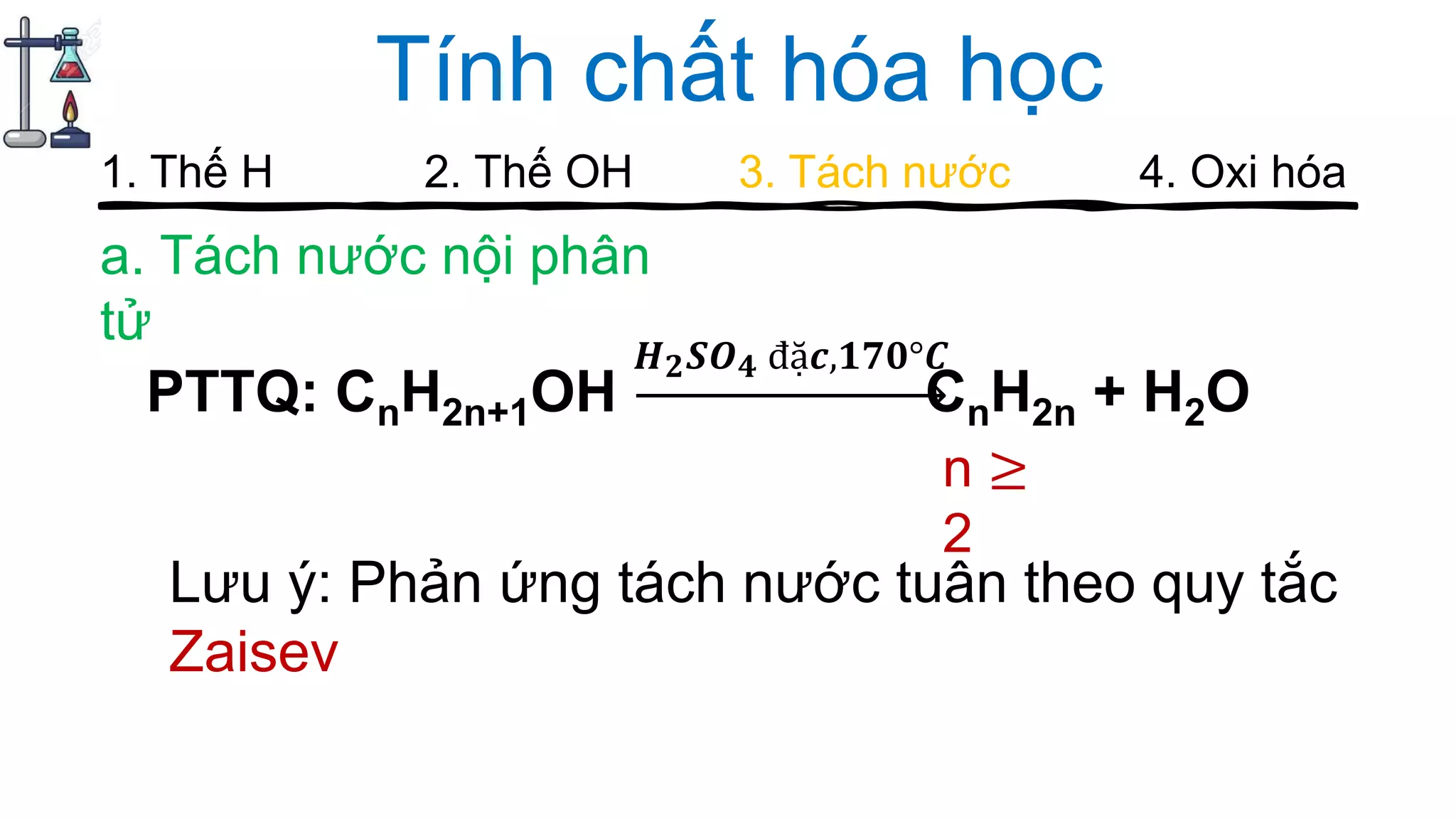
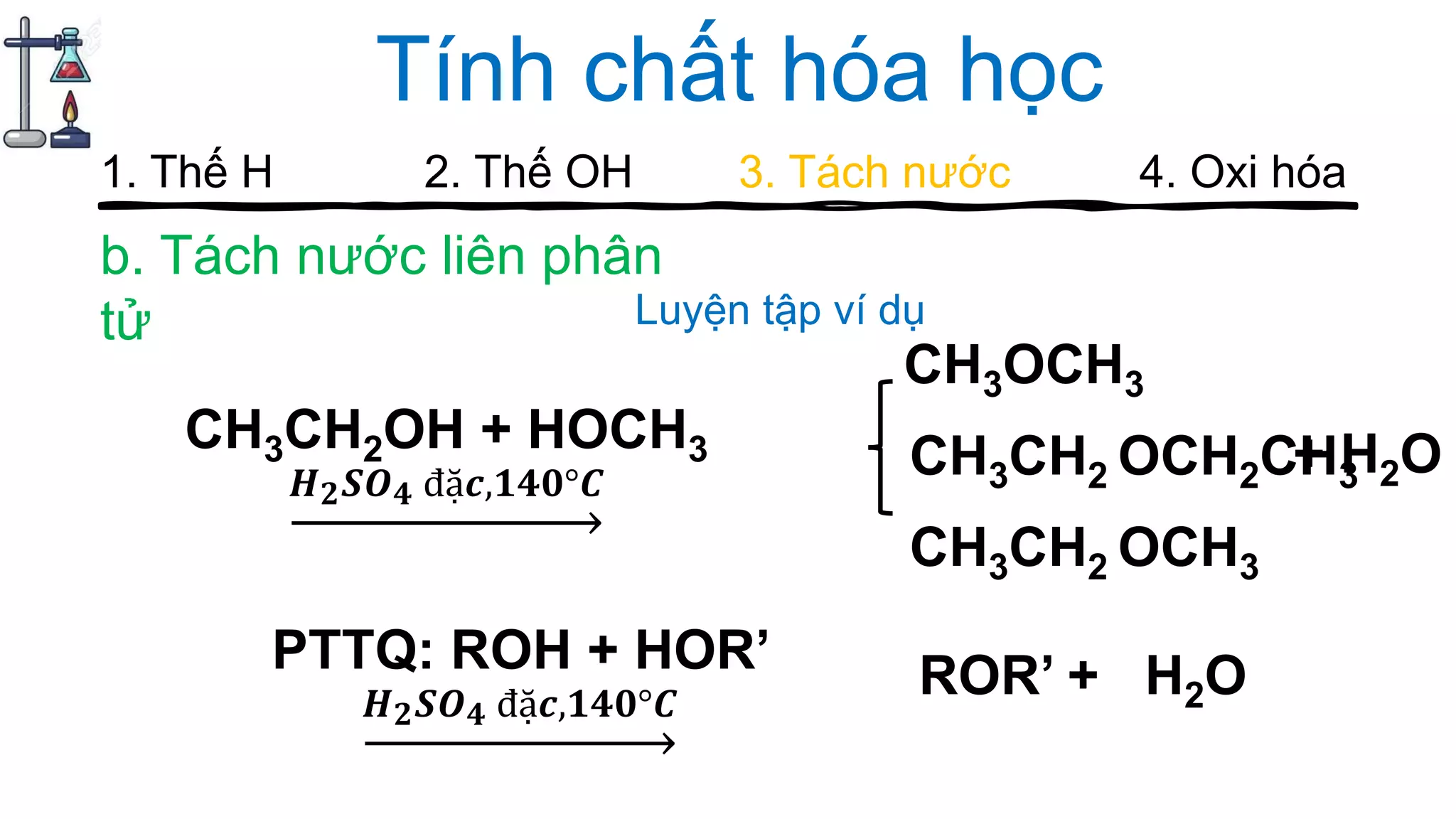
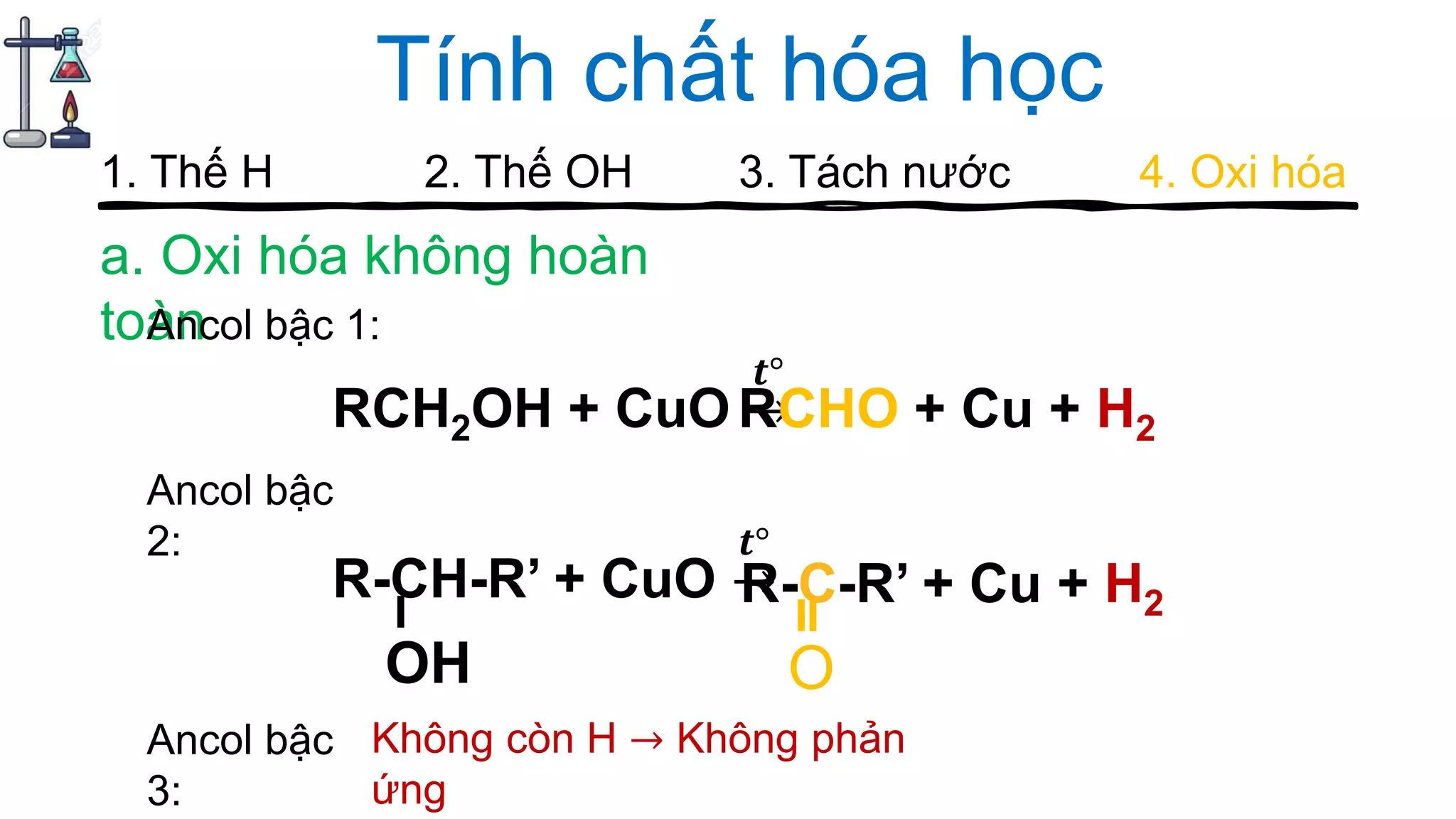
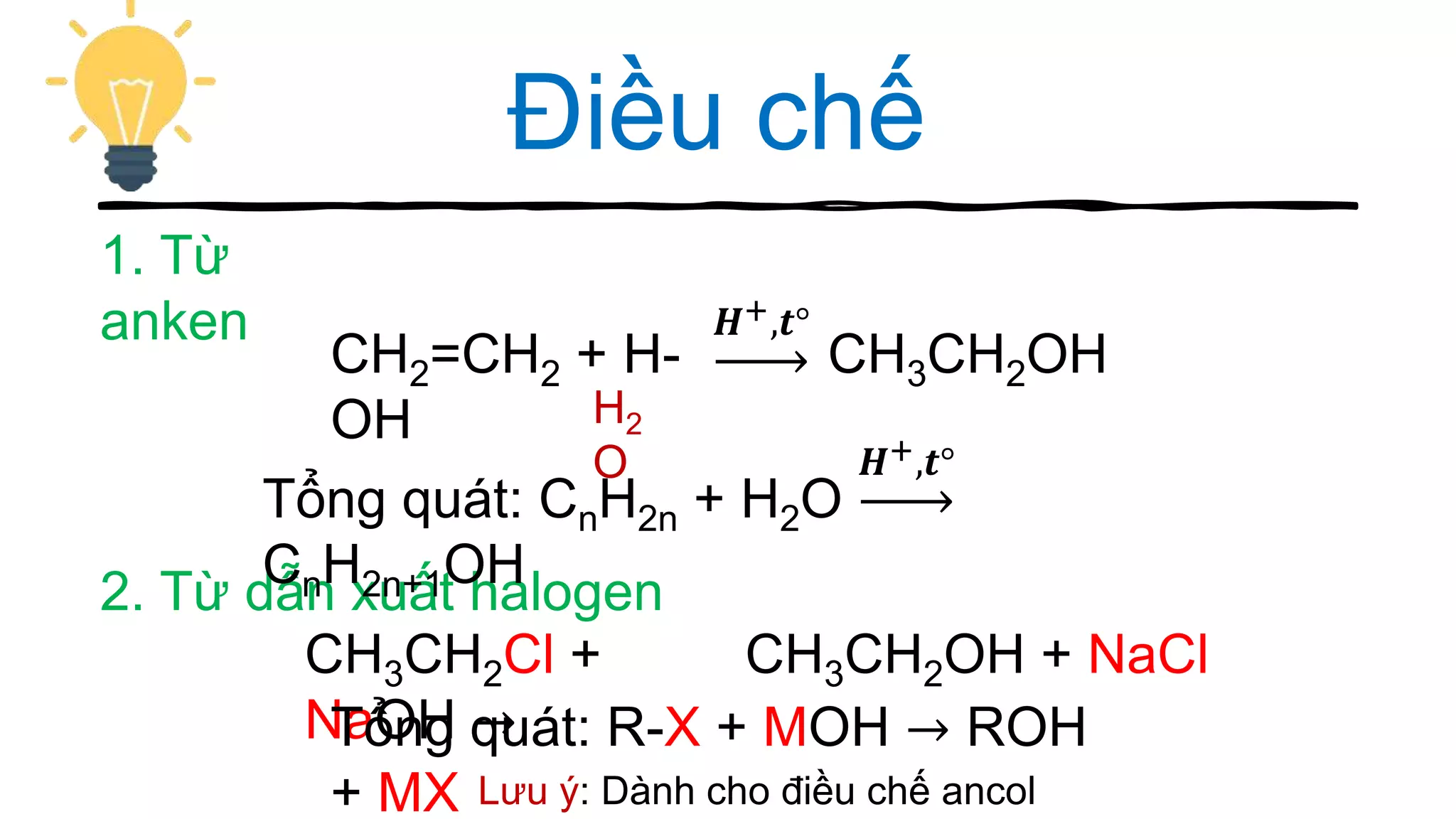
Tài liệu cung cấp hướng dẫn về cách chơi và các câu hỏi liên quan đến ancol trong hóa học, bao gồm các vấn đề như điểm số, cấu trúc, tính chất hóa học, đồng phân và các phương pháp điều chế ancol. Nội dung bao gồm các phản ứng hóa học, các thuật ngữ hóa học, cũng như ứng dụng của ancol trong thực tế như trong sản xuất đồ uống. Các tranh luận và thảo luận được khuyến khích trong quá trình chơi để ghi nhận thông tin và điểm số cao nhất.