Recommended
PDF
PDF
PPTX
DOCX
PDF
กระบวนการเปลี่ยนเเปลงลมฟ้าอากาศ
PPTX
PDF
แผนการจัดการเรียนรู้ เรื่อง แบบจำลองอะตอมของดอลตันและทอมสัน
PDF
PDF
PPTX
PDF
PDF
PDF
เอกสารประกอบการสรุปเข้ม O
PDF
เคมีสิ่งแวดล้อม (Environmental Chemistry)
PDF
PDF
ใบงานที่ 2 การจัดเรียงอิเล็กตรอน
PDF
PDF
PDF
PDF
เชื้อเพลิงซากดึกดำบรรพ์ (Fossil fuels
PPTX
Ep03 บวก ลบ คูณ หาร เลขนัยสำคัญ (เรียนฟิสิกส์กับครูอุ๋ย)
PDF
มวลอะตอม มวลโมเลกุล มวลไอออน
PDF
พันธะโคเวเลนต์ Covalent Bond
PDF
PDF
ระบบไหลเวียนเลือด (Circulatory System)
PDF
PPTX
PPTX
PDF
PDF
บทที่ 2 โครงสร้างของของแข็ง the structure of solid
More Related Content
PDF
PDF
PPTX
DOCX
PDF
กระบวนการเปลี่ยนเเปลงลมฟ้าอากาศ
PPTX
PDF
แผนการจัดการเรียนรู้ เรื่อง แบบจำลองอะตอมของดอลตันและทอมสัน
PDF
What's hot
PDF
PPTX
PDF
PDF
PDF
เอกสารประกอบการสรุปเข้ม O
PDF
เคมีสิ่งแวดล้อม (Environmental Chemistry)
PDF
PDF
ใบงานที่ 2 การจัดเรียงอิเล็กตรอน
PDF
PDF
PDF
PDF
เชื้อเพลิงซากดึกดำบรรพ์ (Fossil fuels
PPTX
Ep03 บวก ลบ คูณ หาร เลขนัยสำคัญ (เรียนฟิสิกส์กับครูอุ๋ย)
PDF
มวลอะตอม มวลโมเลกุล มวลไอออน
PDF
พันธะโคเวเลนต์ Covalent Bond
PDF
PDF
ระบบไหลเวียนเลือด (Circulatory System)
PDF
PPTX
PPTX
Viewers also liked
PDF
PDF
บทที่ 2 โครงสร้างของของแข็ง the structure of solid
PDF
PDF
บทที่ 7 สสารในสนามแม่เหล็ก
PPT
PPT
บทที่ 1 โครงสร้างผลึกของแข็ง
PDF
PDF
สหวิทยาการของนาโนเทคโนโลยี
Similar to Chap 5 chemical bonding
PDF
พันธะเคมี Part ionic bonds
PDF
พันธะเคมี - Chemical bonds
PDF
พันธะเคมี-(Chemical Bonding)มทร.ล้านนา.pdf
PPT
PDF
PDF
PDF
PPT
PDF
วิชาเคมี ม.ปลาย เรื่องตารางธาตุ
PDF
PPT
PPT
PPT
PPTX
PPT
PPTX
PDF
SLIDE-01403117-CH02-CHEMICALBOND-FULL.pdf
PPT
PDF
PDF
More from Gawewat Dechaapinun
PPTX
Chapter 4 properties of glazes and control
PDF
PPTX
Chapter 1.3 properties of glass crystalline mixtures
PDF
PPTX
Chapter 2.1 glaze classifications
PPTX
PPTX
บทที่ 2 ประเภทของบทเรียนคอมพิวเตอร์
PPTX
PDF
Chapter 2.3 glaze calculations
DOCX
บทที่ 8 แนวคิดและความเชื่อเรื่องผีในคัมภีร์พระพุทธศาสนาเถร
DOCX
บทที่ 8 แนวคิดและความเชื่อเรื่องผีในคัมภีร์พระพุทธศาสนาเถร
PPTX
PPTX
PPTX
PPTX
PDF
Chapter 3 glaze manufacturing
PPT
เน€เธ—เธเนเธเนเธฅเธขเธตเธเธฑเธเนเธฅเธฐเธเธฅเนเธกเน
PPTX
Chapter 3 glaze manufacturing
PPTX
Chapter 3 glaze manufacturing
PDF
เน€เธ—เธเนเธเนเธฅเธขเธตเธเธฑเธเนเธฅเธฐเธเธฅเนเธกเน
Chap 5 chemical bonding 1. 2. อะตอมของธาตุต่าง ๆ จะรวมกันเป็นโมเลกุลของ
สารประกอบได้นั้น จะต้องมีแรงยึดเหนี่ยวระหว่าง
อะตอมให้อยู่ด้วยกัน แรงยึดเหนี่ยวนี้เรียกว่า พันธะเคมี
โมเลกุลหลาย ๆ โมเลกุลมารวมกันเป็นกลุ่มก้อน
ได้นั้น จะต้องมีแรงยึดเหนี่ยวกันระหว่างแต่ละโมเลกุล
แรงยึดเหนี่ยวนี้เรียกว่า แรงยึดเหนี่ยวระหว่างโมเลกุล
5-2
ความหมายของพันธะเคมี
3. พันธะเคมี แบ่งออกเป็น
1. พันธะไอออนิก (ionic bond)
2. พันธะโคเวเลนต์(covalent bond)
3. พันธะโคออร์ดิเนตโคเวเลนต์(coordinate
covalent bond)
4. พันธะโลหะ (metallic bond)
5-3
ชนิดของพันธะเคมี
4. 5. กฎออกเตต (Octet Rule)
ในการเกิดสารประกอบ ส่วนใหญ่อะตอมของธาตุ
ต่าง ๆ จะรวมกันด้วยสัดส่วนที่ทาให้อะตอมเหล่านั้นมี
อิเล็กตรอนวงนอกสุดครบแปด ซึ่งเหมือนกับโครงสร้าง
อะตอมของแก๊สเฉื่อย ทาให้มีความเสถียรเป็นพิเศษ
กฎออกเตต เป็นกฎทั่ว ๆ ไป สารประกอบบางตัว
อาจเสถียรโดยไม่เป็นไปตามกฎนี้
5-5
6. 7. 7
ไอออนบวก : อะตอมสูญเสีย e-
11
23 Na
-1e-
Na+
จานวน p > e- 1 อนุภาค
: การจัดเรียง e- : 2 8
Mg(2 8 2) -2e-
Mg2+(2 8)
จานวน p > e-
: การจัดเรียง e- : 2 8 1
5-7
8. 8
ไอออนลบ : อะตอมรับ e- เพิ่ม
1735Cl ( 2 8 7) +1e-
Cl- (2 8 8)
จานวน e- > p 1 อนุภาค
816O (2 6)
+2e-
O2- (2 8)
จานวน e- > p
5-8
9. 10. 11. 1. สารประกอบไอออนิก : เป็นของแข็งที่เป็นผลึก
2. จุดหลอมเหลวสูง
CCZr
COMg
CClNa
o44
o22
o
3500=mp.
2640=mp.
801=mp.
ขึ้นกับแรงยึดเหนี่ยว
ระหว่างประจุและขนาด
ของไอออนหรือระยะห่าง
ระหว่างไอออน
มาก
สมบัติทั่วไป
5-11
สารประกอบไอออนิก (Ionic compound)
12. 3. โครงผลึกเป็นกลางทางไฟฟ้ าเพราะ เป็นการ
จัดเรียงของไอออนบวกและลบซึ่งล้อมรอบ
ซึ่งกันและกันอย่างสมมาตรในโครงผลึก 3 มิติ
จึง เป็นพันธะที่ไม่มีทิศทาง
เรียกโครงสร้างแบบ rock salt (NaCl-st)
6 : 6
จานวน Cl- ที่ล้อมรอบ Na+ “ด้วยระยะทางที่เท่ากันและใกล้ที่สุด”
จานวน Na+ ที่ล้อมรอบ Cl-
Na+ Cl- Na+ Cl-
Cl- Na+ Cl- Na+
Na+ Cl- Na+ Cl-
Na+Cl--st.
ต.ย.
5-12
13. Cs+Cl- -st. ล้อมรอบซึ่งกันและกัน = 8 : 8 เป็นต้น
: สารประกอบไอออนิกจะมีโครงสร้างแบบใด
ขึ้นกับอัตราส่วนรัศมีระหว่างไอออนบวกและไอออนลบ
5. ไม่นาไฟฟ้ า ยกเว้น เมื่อหลอมเหลว/ ละลายน้า
เพราะ……….…….....................................................................
6. แข็งแต่เปราะ เพราะ…………............................................
……………………………………………………………….
d
-
H Hd
+
NaCl Na+
(aq)+ Cl-
(aq)
H2O
d
+
4. ส่วนใหญ่ละลายน้าได้
เมื่อมีแรงมากระทบ ทาให้ระนาบใดระนาบหนึ่ง
ของผลึกเลื่อนไป เป็นผลทาให้ประจุชนิดเดียวกันอยู่ใกล้กัน ทาให้เกิดแรงผลัก
ระหว่างระนาบสูง ---> เปราะ
ไอออนบวกและลบในสภาวะของแย็ง ไม่สามารถเคลื่อนที่ได้อย่างอิสระ
5-13
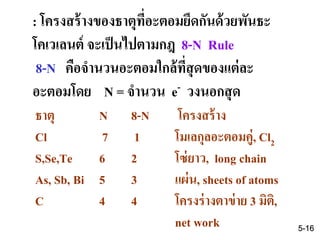
14. 15. 16. 17. ธาตุที่มี N < 4 ไม่สามารถเกิดพันธะ
โคเวเลนต์ได้ สรุป เฉพาะ C เท่านั้น
(เพชร, mp = 3500oC) ที่ให้โครงสร้าง
3 มิติโดยทุกพันธะเป็นโคเวเลนต์ ซึ่งจัด
เป็น พวกโครงร่างตาข่าย ดังนั้นพันธะ
โคเวนเลนต์ : เป็นพันธะที่แข็งแรงมาก
ถ้าเกิดทุกทิศทางใน 3 มิติ
5-17
18. พันธะโคเวเลนต์แบบมีขั้ว พันธะที่เกิดจากอะตอมที่มี
ค่า electronegativity (EN) ต่างกัน หมอกอิเล็กตรอน
จะหนาแน่นบริเวณใกล้อะตอมหนึ่งมากกว่าอีกอะตอม
หนึ่ง ทาให้อะตอมหนึ่งมีประจุค่อนข้างไปทางลบ
เล็กน้อย อีกอะตอมหนึ่งมีประจุค่อนข้างไปทางบวก
เล็กน้อย พันธะแบบนี้เรียกว่าพันธะโคเวเลนต์แบบมี
ขั้ว (polar covalent bond หรือ polar bond) เช่น HCl
5-18
พันธะโคเวเลนต์แบบมีขั้วและแบบไม่มีขั้ว
19. 20. 21. 22. 23. พันธะโลหะ (Metallic Bond)
1. free - electron theory (e- sea model)
2. ทฤษฎีแถบพลังงาน (bond theory)
: เป็นทฤษฏีที่อธิบายพันธะเคมีและสมบัติต่าง ๆ ของโลหะได้ดี
โลหะ : เป็นผลึก (Metallic crystal)
อนุภาคของโลหะจัดเรียงตัวเป็นระเบียบและยึดกัน
ด้วยพันธะโลหะ
พันธะโลหะ : เป็นแรงดึงดูดระหว่าง ไอออนบวก
ของโลหะกับทะเล e- ซึ่งมีประจุลบ e- เหล่านี้
ถูกดึง (ionized) ออกมาจากแต่ละอะตอมของโลหะ
5-23
24. : เป็นแรงยึดเหนี่ยวที่แข็งแรง & ไม่มีทิศทาง
ฉะนั้นพวกโลหะจึงแข็ง มี mp & bp สูง
(โดยทั่วไปสูงกว่า สารประกอบไอออนิก)
: e- เหล่านี้เคลื่อนที่อย่างอิสระตลอดเวลาเรียก
ทะเล e-
: พันธะไม่ได้อยู่ที่อะตอมคู่ใดคู่หนึ่ง เป็นแรงดึงดูด
ที่เกิดขึ้นทั้งหมดไปทั้งโครงผลึก ซึ่งต่างจากพันธะ
โคเวเลนต์
5-24
25. +
+ + + + + + +
+ + + + + + +
++ + + + +
+ + + + + + +
: แรงนี้จะมากหรือน้อยขึ้นกับปริมาณ e- ในโครงผลึก
ขนาดของประจุบวกและขนาดของอะตอม
ฉะนั้น โลหะแทรนซิชัน เช่น Fe จึงแข็งกว่าโลหะ
หมู่ 1, 2 และโลหะหมู่ 2 (เช่น Be, Mg) จะแข็งกว่า
โลหะหมู่ 1 (เช่น Na, Li)
5-25
26. ทฤษฏีนี้ สามารถอธิบายสมบัติต่างๆ
ของโลหะ ได้ดังนี้
1. นาความร้อนได้ดี เพราะจากการสั่นอย่างต่อเนื่อง
ระหว่าง e- ที่อยู่ถัดกัน ทาให้พลังงานความร้อน
กระจายผ่านโครงผลึกอย่างรวดเร็ว
2. นาไฟฟ้ าได้ดี เพราะ…….……….......................................ทะเล e- (ซึ่งเป็นอนุภาคที่มีประจุ) เคลื่อนที่ตลอดเวลา
5-26
27. 3. มันวาว (high reflectivity) เพราะ e- ดูดกลืน
พลังงานแสงทาให้ e- เหล่านี้ถูกกระตุ้นไปอยู่
ระดับพลังงานสูงขึ้นซึ่งไม่เสถียร จึงกลับลงมา
ที่สภาวะเดิมพร้อมกับคายพลังงานออกมา
จึงเห็นแสงสะท้อนจากผิวโลหะตลอดเวลา
4. มีความแข็งแกร่ง แต่ไม่เปราะและดึง ยืดเป็น
แผ่นบาง ๆ ได้ เพราะ………………...................................ถึงแม้ระนาบของผลึกเลื่อนไป เนื่องจากแรงกระทบ
ก็ไม่มีผลต่อแรงยึดเหนี่ยวเนื่องจาก ทะเล e- เคลื่อนที่ไปได้ทุก ๆ
ระนาบที่เลื่อนไป
5-27
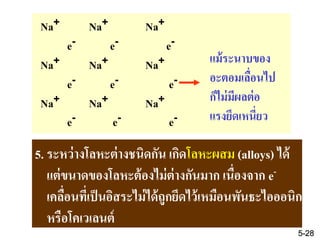
28. Na+ Na+ Na+
e- e- e-
Na+ Na+ Na+
e- e- e-
Na+ Na+ Na+
e- e- e-
แม้ระนาบของ
อะตอมเลื่อนไป
ก็ไม่มีผลต่อ
แรงยึดเหนี่ยว
5. ระหว่างโลหะต่างชนิดกัน เกิดโลหะผสม (alloys) ได้
แต่ขนาดของโลหะต้องไม่ต่างกันมาก เนื่องจาก e-
เคลื่อนที่เป็นอิสระไม่ได้ถูกยึดไว้เหมือนพันธะไอออนิก
หรือโคเวเลนต์
5-28
29. 2. ทฤษฎีแถบพลังงาน (Band theory) : ทฤษฎีนี้
อาศัยพื้นฐานของทฤษฎีโมเลกุลาร์ออร์บิทัล คือ ถ้ามี 2
อะตอมมิกออร์บิทัลรวมกันก็จะได้สองโมเลกุลาร์
ออร์บิทัล โดยออร์บิทัลหนึ่งมีพลังงานสูงเป็ นแบบ
ต้านพันธะ (AMO) อีกอันหนึ่งมีพลังงานต่าเป็นแบบ
มีพันธะ (BMO) แต่ละโมเลกุลาร์ออร์บิทัลสามารถ
บรรจุอิเล็กตรอนได้ไม่เกิน 2 อิเล็กตรอนโดยมีสปิ น
ตรงข้ามกัน
5-29
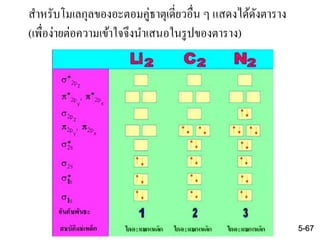
30. เมื่อมีอะตอมมากขึ้นและจานวน MO มากขึ้น ระดับพลังงานของ
MO จะต่างกันน้อยลง ระดับพลังงานที่ใกล้ชิดกันมากนี้จะดูเสมือน
เป็นแถบต่อเนื่องกัน จึงเรียกว่าแถบพลังงาน (energy band) กรณี
ของ Li แถบพลังงานได้มาจาก 2s orbital จะเรียกว่าแถบ 2s
ตัวอย่าง การบรรจุอิเล็กตรอนของโลหะลิเทียม
5-30
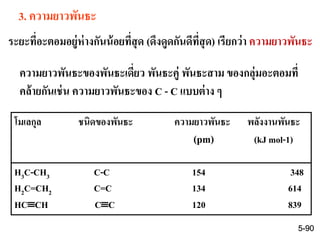
31. 32. 33. 34. 35. 36. พันธะเดี่ยวเกิดจากพันธะซิกมา 1 พันธะ พันธะคู่เกิดจาก
พันธะซิกมา 1 พันธะ และพันธะไพ 1 พันธะ พันธะสามเกิดจาก
พันธะซิกมา 1 พันธะ และพันธะไพ 2 พันธะ จะเห็นว่าพันธะคู่
และพันธะสามมีการสร้างพันธะทั้งพันธะซิกมาและไพ จึง
แข็งแรงกว่าพันธะเดี่ยว อย่างไรก็ตามพันธะสามมีการสร้าง
พันธะซิกมาเท่ากับพันธะคู่แต่มีพันธะไพมากกว่า ดังนั้น
จึงแข็งแรงกว่า
5-36
37. 38. 5-38
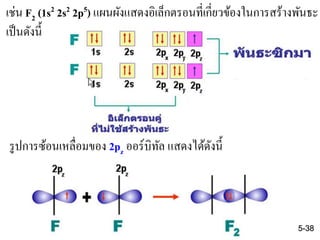
เช่น F2 (1s2 2s2 2p5) แผนผังแสดงอิเล็กตรอนที่เกี่ยวข้องในการสร้างพันธะ
เป็นดังนี้
รูปการซ้อนเหลื่อมของ 2pz ออร์บิทัล แสดงได้ดังนี้
39. ไฮบริไดเซชัน (Hybridization)
ไฮบริไดเซซัน คือ ปรากฎการณ์ที่ออร์บิทัลในอะตอม
เดียวกัน ที่มีระดับพลังงานใกล้เคียงกันเกิดการรวมกันเกิด
เป็นไฮบริดออร์บิทัล (hybrid orbital) ซึ่งแต่ละไฮบริด-
ออร์บิทัลจะครอบครองพื้นที่เท่ากัน และอยู่ห่างกันมาก
ที่สุดเพื่อทาให้พลังงานรวมของออร์บิทัลมีพลังงานน้อย
ที่สุด ผลที่เกิดขึ้นก็คือ เกิดไฮบริดออร์บิทัลมีรูปร่างต่าง ๆ
กันไป และพลังงานรวมของไฮบริดออร์บิทัลน้อยกว่า
ผลรวมพลังงานทั้งหมดของออร์บิทัลอะตอมก่อนการเกิด
ไฮบริไดเซซัน
5-39
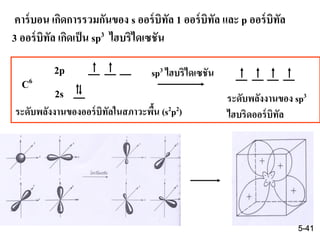
40. เช่น
C6
2p
2s
พบว่าอะตอมคาร์บอนมี e- เดี่ยวใน 2p ออร์บิทัล 2 ตัว ดังนั้นควร
เกิดพันธะโคเวเลนต์กับอะตอมอื่นได้เพียง 2 พันธะเท่านั้น แต่ความจริง
แล้วคาร์บอนสามารถเกิดได้ 4 พันธะ โดยพิจารณาจากการผสมกันของ
s และ p ออร์บิทัลเข้าด้วยกัน เรียก ไฮบริดออร์บิทัล
ไฮบริดออร์บิทัล จะมีลักษณะ สมบัติ และระดับพลังงานเท่ากัน
ทุกประการ 5-40
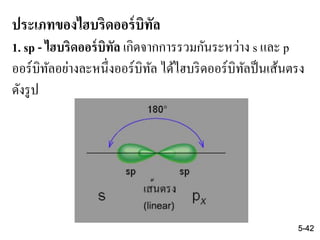
41. 42. 43. ตัวอย่างของ sp - ไฮบริดออร์บิทัล เช่น BeCl2, C2H2
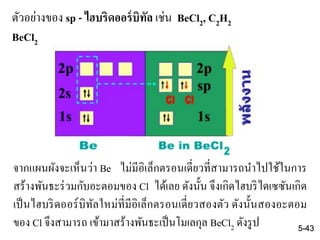
BeCl2
จากแผนผังจะเห็นว่า Be ไม่มีอิเล็กตรอนเดี่ยวที่สามารถนาไปใช้ในการ
สร้างพันธะร่วมกับอะตอมของ Cl ได้เลย ดังนั้น จึงเกิดไฮบริไดเซซันเกิด
เป็นไฮบริดออร์บิทัลใหม่ที่มีอิเล็กตรอนเดี่ยวสองตัว ดังนั้นสองอะตอม
ของ Cl จึงสามารถ เข้ามาสร้างพันธะเป็นโมเลกุล BeCl2 ดังรูป 5-43
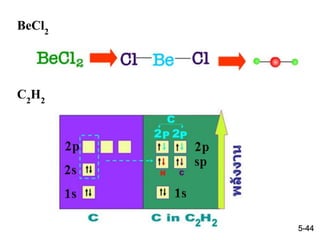
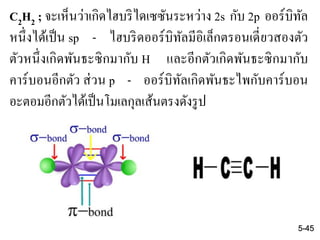
44. 45. C2H2 ; จะเห็นว่าเกิดไฮบริไดเซซันระหว่าง 2s กับ 2p ออร์บิทัล
หนึ่งได้เป็น sp - ไฮบริดออร์บิทัลมีอิเล็กตรอนเดี่ยวสองตัว
ตัวหนึ่งเกิดพันธะซิกมากับ H และอีกตัวเกิดพันธะซิกมากับ
คาร์บอนอีกตัว ส่วน p - ออร์บิทัลเกิดพันธะไพกับคาร์บอน
อะตอมอีกตัวได้เป็นโมเลกุลเส้นตรงดังรูป
5-45
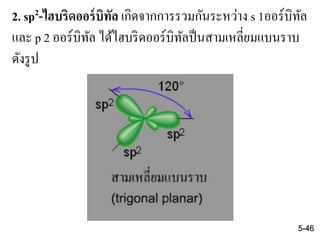
46. 47. ตัวอย่างของ sp2 - ไฮบริดออร์บิทัล เช่น C2H4, BF3
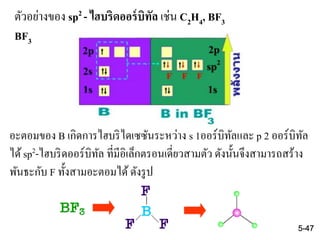
BF3
อะตอมของ B เกิดการไฮบริไดเซซันระหว่าง s 1ออร์บิทัลและ p 2 ออร์บิทัล
ได้sp2-ไฮบริดออร์บิทัล ที่มีอิเล็กตรอนเดี่ยวสามตัว ดังนั้นจึงสามารถสร้าง
พันธะกับ F ทั้งสามอะตอมได้ดังรูป
5-47
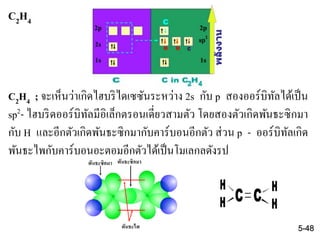
48. C2H4
C2H4 ; จะเห็นว่าเกิดไฮบริไดเซซันระหว่าง 2s กับ p สองออร์บิทัลได้เป็น
sp2- ไฮบริดออร์บิทัลมีอิเล็กตรอนเดี่ยวสามตัว โดยสองตัวเกิดพันธะซิกมา
กับ H และอีกตัวเกิดพันธะซิกมากับคาร์บอนอีกตัว ส่วน p - ออร์บิทัลเกิด
พันธะไพกับคาร์บอนอะตอมอีกตัวได้เป็นโมเลกุลดังรูป
5-48
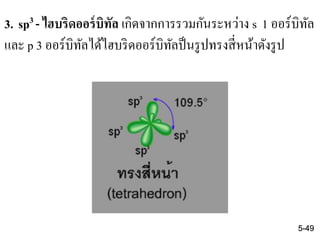
49. 3. sp3 - ไฮบริดออร์บิทัล เกิดจากการรวมกันระหว่าง s 1 ออร์บิทัล
และ p 3 ออร์บิทัลได้ไฮบริดออร์บิทัลป็นรูปทรงสี่หน้าดังรูป
5-49
50. 5-50
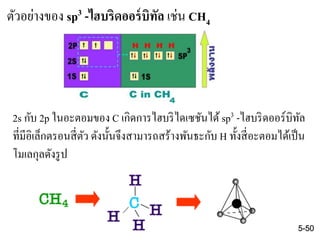
ตัวอย่างของ sp3 -ไฮบริดออร์บิทัล เช่น CH4
2s กับ 2p ในอะตอมของ C เกิดการไฮบริไดเซชันได้ sp3 -ไฮบริดออร์บิทัล
ที่มีอิเล็กตรอนสี่ตัว ดังนั้นจึงสามารถสร้างพันธะกับ H ทั้งสี่อะตอมได้เป็น
โมเลกุลดังรูป
51. 4. sp3d - ไฮบริดออร์บิทัล เกิดจากการรวมกันระหว่าง s ออร์บิทัล
1 ออร์บิทัล, d ออร์บิทัล 1 ออร์บิทัลและ p ออร์บิทัล 3 ออร์บิทัล
ได้ไฮบริดออร์บิทัลป็นรูปคู่พีระมิดร่วมฐานสามเหลี่ยม (trigonal
bipyramid) ดังรูป
5-51
52. 5-52
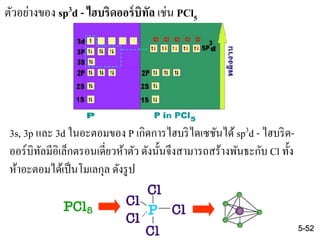
ตัวอย่างของ sp3d - ไฮบริดออร์บิทัล เช่น PCl5
3s, 3p และ 3d ในอะตอมของ P เกิดการไฮบริไดเซชันได้ sp3d - ไฮบริด-
ออร์บิทัลมีอิเล็กตรอนเดี่ยวห้าตัว ดังนั้นจึงสามารถสร้างพันธะกับ Cl ทั้ง
ห้าอะตอมได้เป็นโมเลกุล ดังรูป
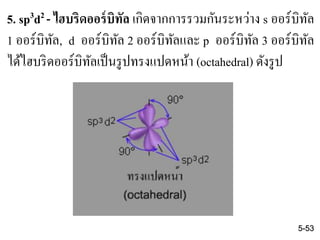
53. 5. sp3d2 - ไฮบริดออร์บิทัล เกิดจากการรวมกันระหว่าง s ออร์บิทัล
1 ออร์บิทัล, d ออร์บิทัล 2 ออร์บิทัลและ p ออร์บิทัล 3 ออร์บิทัล
ได้ไฮบริดออร์บิทัลเป็นรูปทรงแปดหน้า (octahedral) ดังรูป
5-53
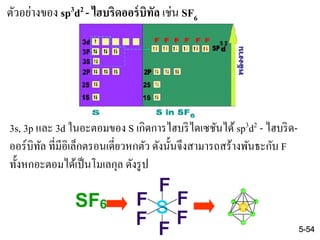
54. ตัวอย่างของ sp3d2 - ไฮบริดออร์บิทัล เช่น SF6
5-54
3s, 3p และ 3d ในอะตอมของ S เกิดการไฮบริไดเซชันได้ sp3d2 - ไฮบริด-
ออร์บิทัล ที่มีอิเล็กตรอนเดี่ยวหกตัว ดังนั้นจึงสามารถสร้างพันธะกับ F
ทั้งหกอะตอมได้เป็นโมเลกุล ดังรูป
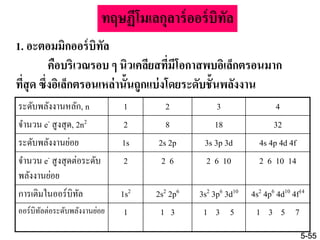
55. ทฤษฏีโมเลกุลาร์ออร์บิทัล
1. อะตอมมิกออร์บิทัล
คือบริเวณรอบ ๆ นิวเคลียสที่มีโอกาสพบอิเล็กตรอนมาก
ที่สุด ซึ่งอิเล็กตรอนเหล่านั้นถูกแบ่งโดยระดับชั้นพลังงาน
ระดับพลังงานหลัก, n 1 2 3 4
จานวน e- สูงสุด, 2n2 2 8 18 32
ระดับพลังงานย่อย 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
จานวน e- สูงสุดต่อระดับ
พลังงานย่อย
2 2 6 2 6 10 2 6 10 14
การเติมในออร์บิทัล 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14
ออร์บิทัลต่อระดับพลังงานย่อย 1 1 3 1 3 5 1 3 5 7
5-55
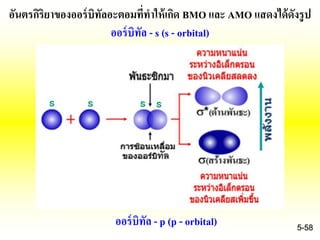
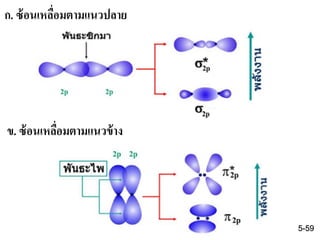
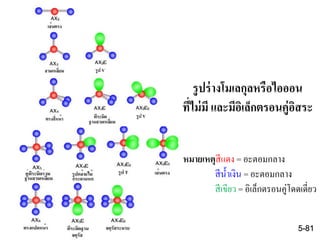
56. 57. 58. 59. 60. จากรูปแสดงการเกิดออร์บิทัลโมเลกุลจากการซ้อนเหลื่อมกันของออร์บิทัล - p
ก.ออร์บิทัล-p ทั้งสองเกิดการซ้อนเหลื่อมตามแนวปลายเกิดเป็นพันธะซิกมา
( σ-bond)
ข.ออร์บิทัล-p ทั้งสองเกิดการซ้อนเหลื่อมตามแนวข้างเกิดเป็นพันธะไพ (p-bond)
จากรูปจะเห็นว่าออร์บิทัลโมเลกุลแบบสร้างพันธะจะมีพลังงานต่ากว่าแบบ
ต้านพันธะเสมอ
(* หมายถึงต้านพันธะ)
BMO และ AMO ที่ได้จากการรวมกันของออร์บิทัล-s จะแทนด้วยสัญลักษณ์ σs
และ σ*s ตามลาดับ
BMO และ AMO ที่ได้จากการรวมกันของออร์บิทัล-p จะแทนด้วยสัญลักษณ์ σz,
σ*z, px, p*x , py , p*y
เมื่อ pz เกิดการซ้อนเหลื่อมตามแนวปลาย px, py เกิดการซ้อนเหลื่อมตามแนวข้าง
5-60
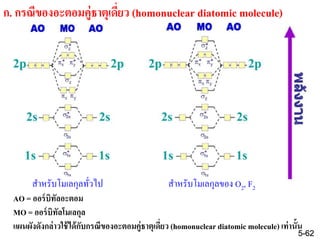
61. 62. AO = ออร์บิทัลอะตอม
MO = ออร์บิทัลโมเลกุล
แผนผังดังกล่าวใช้ได้กับกรณีของอะตอมคู่ธาตุเดี่ยว (homonucleardiatomic molecule)เท่านั้น
5-62
ก. กรณีของอะตอมคู่ธาตุเดี่ยว (homonuclear diatomic molecule)
สาหรับโมเลกุลทั่วไป สาหรับโมเลกุลของ O2, F2
63. 64. H มีเวเลนซ์อิเล็กตรอน 1 ตัว ดังนั้น 2H จึงมีอิเล็กตรอน 2 ตัว จากแผนผังจะเห็นว่า
อิเล็กตรอนทั้งสองถูกบรรจุลงในออร์บิทัลโมเลกุลมีพลังงานต่าสุด
นั่นคือ ออร์บิทัลซิกมา (เกิดพันธะซิกมา) หลังจากที่อิเล็กตรอนทั้งสองมารวมอยู่
ในออร์บิทัลโมเลกุลเกิดเป็น H2 จะเห็นว่ามีพลังงานต่ากว่าที่เป็น H อะตอม
5-64
ตัวอย่างการบรรจุอิเล็กตรอนในออร์บิทัลโมเลกุล
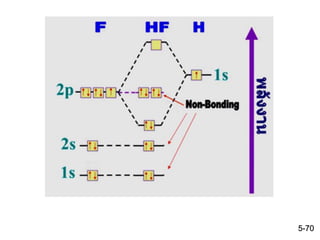
65. 66. 67. 68. 69. ข. ออร์บิทัลโมเลกุลของธาตุต่างชนิดกัน (heteronuclear diatomic
molecule)
โดยทั่วไปแล้วออร์บิทัลอะตอมของอะตอมที่มีค่าอิเล็กโทรเนกาติวิตี
ต่ากว่ามักจะมีค่าพลังงานสูงกว่า ตัวอย่างออร์บิทัลโมเลกุลของธาตุ
ต่างชนิดกัน เช่น HF
HF : H มี 1 เวเลนซ์อิเล็กตรอน และ F มี 7 เวเลนซ์อิเล็กตรอน
จะเห็นว่าอิเล็กตรอนทั้ง 8 ตัวบรรจุอยู่ในออร์บิทัลโมเลกุลทั้งหมด 4
ออร์บิทัล โดยออร์บิทัลที่มีระดับพลังงานสูงสุดที่มีอิเล็กตรอนบรรจุอยู่
เป็นชนิดไพออร์บิทัล ซึ่งอิเล็กตรอนในไพออร์บิทัลจะไม่มีส่วน
เกี่ยวข้องกับ H อะตอม เรียกออร์บิทัลเหล่านี้ว่า non - bonding orbital
ซึ่งแสดงได้ดังรูป
5-69
70. 71. Valence Shell Electron Pair Repulsion Theory
(VSEPR Theory)
เป็นทฤษฎีที่ใช้ทานายรูปทรงเรขาคณิตของโมเลกุลและของ
ไอออน มีใจความว่า “รูปร่างโมเลกุลหรือไอออนของ
สารประกอบโคเวเลนต์จะเป็นอย่างไรนั้น ขึ้นอยู่กับแรงผลัก
ระหว่างคู่อิเล็กตรอนในระดับพลังงานนอกสุดของอะตอมที่
อยู่กลาง โดยอิเล็กตรอนคู่ที่อยู่ล้อมรอบจะจัดเรียงตัวให้อยู่
ห่างกันมากที่สุดเพื่อให้เกิดแรงผลักน้อยที่สุด” ตามทฤษฎีนี้
สามารถเขียนเป็นสูตรทั่วไปสาหรับโมเลกุลได้ดังนี้
5-71
72. AXmEn
เมื่อ A = อะตอมกลาง
X = อะตอมหรือหมู่อะตอมที่ยึดอยู่กับ A โดยใช้พันธะโคเวเลนต์
E = สัญลักษณ์แทนคู่อิเล็กตรอนที่ไม่ใช้สร้างพันธะ
m = จานวนคู่อิเล็กตรอนที่ใช้สร้างพันธะ
n = จานวนคู่อิเล็กตรอนที่ไม่ใช้สร้างพันธะ
5-72
73. เช่น จงเขียนสูตรโมเลกุลแบบ AXmEn ของ SF4 และ ICl4
-
SF4 ICl4
-
จานวนเวเลนซ์อิเล็กตรอนของอะตอมกลาง 6 7
จานวนอิเล็กตรอนที่เข้าร่วมในการสร้างพันธะ 4 4
จานวนอิเล็กตรอนจากประจุ - 1
รวม 10(5) 12(6)
คู่อิเล็กตรอนที่ใช้สร้างพันธะ 4 4
คู่อิเล็กตรอนที่ไม่ใช้สร้างพันธะ 1 2
สูตรโมเลกุลแบบ AXmEn AX4E1 AX4E2
F
SF4 S
..
F
F
F
ICl4
-
ICl Cl
ClCl
..
..
5-73
74. สรุปใจความสาคัญของทฤษฎี VSEPR
1. รูปร่างของโมเลกุลหรือไอออนที่ยึดกันด้วยพันธะโคเวเลนต์ขึ้นกับ
ค่า m และ n ทั้งหมดที่มีอยู่ในวงเวเลนซ์ คู่อิเล็กตรอนเหล่านี้จะมีการ
จัดเรียงตัวให้อยู่ห่างกันมากที่สุด เพื่อให้เกิดแรงผลักกันน้อยที่สุด
2. การผลักกันของคู่อิเล็กตรอนจะลดลงตามลาดับดังนี้
คู่โดดเดี่ยว-คู่โดดเดี่ยว > คู่โดดเดี่ยว-คู่สร้างพันธะ > คู่สร้างพันธะ-คู่สร้างพันธะ
3. สาหรับ multiple bond ให้ถือว่ามีอิเล็กตรอนที่ร่วมสร้างพันธะอยู่เพียง
กลุ่มเดียว
4. การผลักของอิเล็กตรอนต่าง ๆ ต่ออิเล็กตรอนอื่น ๆ
คู่โดดเดี่ยว > พหุพันธะ >คู่สร้างพันธะ> อิเล็กตรอนเดี่ยว
5-74
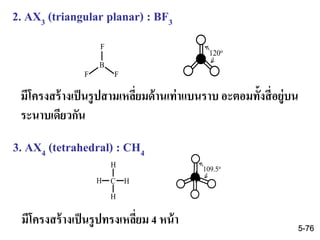
75. 76. 3. AX4 (tetrahedral) : CH4
มีโครงสร้างเป็นรูปทรงเหลี่ยม 4 หน้า
C
H
HH
H
109.5o
2. AX3 (triangular planar) : BF3
B
F
FF
120o
มีโครงสร้างเป็นรูปสามเหลี่ยมด้านเท่าแบนราบ อะตอมทั้งสี่อยู่บน
ระนาบเดียวกัน
5-76
77. 5. AX6 (octahedral) : SF6
มุมพันธะมีค่าเท่ากับ 90o ทุกพันธะบนทรงแปดหน้าถือว่าเหมือนกัน เรา
จึงไม่สามารถใช้คาว่า แนวแกน และแนวระนาบสาหรับโครงสร้างนี้ได้
S
F
F
F
F
F
F
4. AX5 (trigonal bipyramidal) : PCl5
อะตอมที่อยู่ด้านบนด้านบนและด้านล่างระนาบ 3 เหลี่ยม เรียกว่า อยู่
ในแนวแกน (axial) ส่วนอีก 3 อะตอมที่อยู่ในระนาบ 3 เหลี่ยม เรียกว่า
อยู่ในแนวระนาบ (equatorial)
P
Cl
Cl
Cl
Cl
Cl
90o
120o
5-77
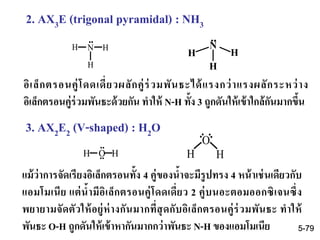
78. 79. 2. AX3E (trigonal pyramidal) : NH3
อิเล็กตรอนคู่โดดเดี่ยวผลักคู่ร่วมพันธะได้แรงกว่าแรงผลักระหว่าง
อิเล็กตรอนคู่ร่วมพันธะด้วยกัน ทาให้ N-H ทั้ง 3 ถูกดันให้เข้าใกล้กันมากขึ้น
3. AX2E2 (V-shaped) : H2O
แม้ว่าการจัดเรียงอิเล็กตรอนทั้ง 4 คู่ของน้าจะมีรูปทรง 4 หน้าเช่นเดียวกับ
แอมโมเนีย แต่น้ามีอิเล็กตรอนคู่โดดเดี่ยว 2 คู่บนอะตอมออกซิเจนซึ่ง
พยายามจัดตัวให้อยู่ห่างกันมากที่สุดกับอิเล็กตรอนคู่ร่วมพันธะ ทาให้
พันธะ O-H ถูกดันให้เข้าหากันมากกว่าพันธะ N-H ของแอมโมเนีย
N HH
H
..
H O H
..
..
..
O
H H
..
N
H
H
H
..
5-79
80. 4. AX4E (square pyramidal or distorted tetrahedral) : SF4
S
F
F
F
F
..
S
..
F
F
F
F
ทรงเหลี่ยมสี่หน้าเบี้ยว โดยอิเล็กตรอนคู่อิสระเลือกที่จะอยู่ใน
แนวระนาบ เนื่องจากมุมในแนวระนาบมีค่า 120o ซึ่งเมื่อจัด
เรียงตัวแล้วเกิดแรงผลักกันน้อยที่สุด
5-80
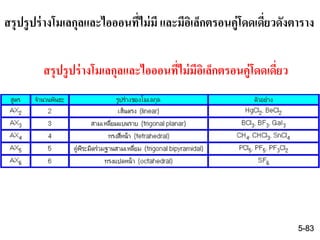
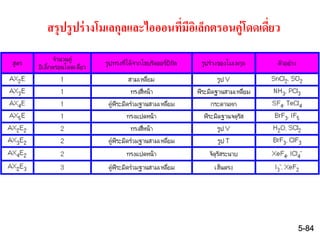
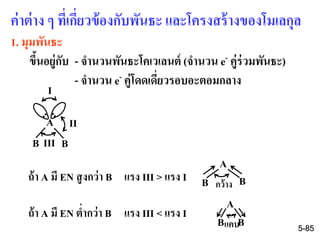
81. 82. 83. 84. 85. ค่าต่าง ๆ ที่เกี่ยวข้องกับพันธะ และโครงสร้างของโมเลกุล
1. มุมพันธะ
ขึ้นอยู่กับ - จานวนพันธะโคเวเลนต์ (จานวน e- คู่ร่วมพันธะ)
- จานวน e- คู่โดดเดี่ยวรอบอะตอมกลาง
A
B B
I
II
III
ถ้า A มี EN สูงกว่า B แรง III > แรง I
ถ้า A มี EN ต่ากว่า B แรง III < แรง I
A
B Bกว้าง
A
B Bแคบ 5-85
86. ธาตุ F O N Cl Br I S C H P
EN 4.0 3.5 3.0 3.2 2.8 2.5 2.5 2.5 2.1 2.1
จากค่าตัวเลข EN Cl > N แต่เมื่อคานึงถึงขนาดอะตอม Cl > N
ดังนั้น EN ของ N > Cl
ค่า EN ของธาตุบางตัวที่ควรรู้จัก
จงเรียงมุมพันธะของโมเลกุลต่อไปนี้จากโมเลกุลที่มีมุมพันธะ
กว้างที่สุดไปยังแคบที่สุด ?
SbH3 PH3 NH3 AsH3
5-86
87. 2. สภาพขั้ว
การบอกสภาพขั้ว - พันธะ (พันธะมีขั้ว พันธะไม่มีขั้ว)
- โมเลกุล (โมเลกุลมีขั้ว โมเลกุลไม่มีขั้ว)
อาศัยผลต่างของ EN (EN)
H H
EN 2.1 2.1
EN = 0
พันธะไม่มีขั้ว โมเลกุลไม่มีขั้ว
2.1 โมเลกุลที่ประกอบด้วยอะตอมของธาตุเดียวกัน
5-87
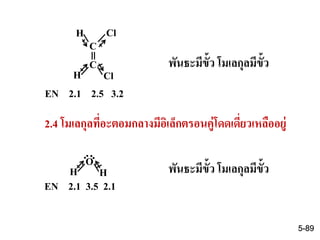
88. 89. C
C
H
H
Cl
Cl
EN 2.1 2.5 3.2
พันธะมีขั้ว โมเลกุลมีขั้ว
2.4 โมเลกุลที่อะตอมกลางมีอิเล็กตรอนคู่โดดเดี่ยวเหลืออยู่
O
H H
EN 2.1 3.5 2.1
พันธะมีขั้ว โมเลกุลมีขั้ว
5-89
90. 91. 92. 93. 94. สาหรับโมเลกุลที่มีขั้ว : จะเกิด dipole - dipole
interaction ระหว่างโมเลกุลที่มีขั้วถาวร
H Cl Cl H Cl
d d d d d d
......... .........H
: ขั้วถาวรเหล่านี้จะยึดกันไปเรื่อย ๆ ระหว่าง
โมเลกุลจึงเป็นแรงที่ไม่มีทิศทาง
5-94
95. 96. 97. : การกระจายของกลุ่มหมอก e- ในชั่ววินาทีหนึ่ง
รอบ ๆ อะตอมไม่สมมาตร (ประจุของ e- รอบ ๆ
อะตอมไม่สมมาตร) ดังนั้นชั่วขณะหนึ่ง ๆ สนาม
ไฟฟ้ าสถิตรอบอะตอมจะเปลี่ยนแปลงตลอดเวลา
ทาให้เกิดขั้วขึ้นชั่วขณะและขั้วมีการเปลี่ยนแปลง
ตลอดเวลา เรียกว่า dynamic dipole อะตอมหรือ
โมเลกุลที่มีขั้วนั้นก็จะเหนี่ยวนาอะตอมข้างเคียง
ให้เกิดขั้วขึ้น อะตอมทั้ง 2 จึงเกิดแรงดึงดูดกัน
สาหรับโมเลกุลไม่มีขั้ว : แรงยึดเหนี่ยวระหว่าง
โมเลกุลที่ไม่มีขั้วนี้เกิดขึ้นได้อย่างไร ?
5-97
98. 99. 100. แรงดึงดูดระหว่างโมเลกุล - ไอออน
(Molecule - ion attraction)
ที่เรียกว่าแรงดึงดูดระหว่างโมเลกุลและไอออนนั้น
เพราะว่าโมเลกุล เช่น น้า ดึงดูดกับไอออนของ Na+ และ
Cl- ของเกลือ
เกลือละลายน้าได้อย่างไร
โมเลกุลของน้าเข้ามาแทรกในโมเลกุลของผลึก โดยที่น้า
บางโมเลกุลเข้าล้อมรอบไอออนบวกโดยหันด้านที่เป็ น
ขั้วลบเข้าหา น้าบางโมเลกุลเข้าล้อมรอบไอออนลบโดย
หันด้านที่เป็นขั้วบวกเข้าหา
5-100
101. 102.