Recommended
PDF
สมบัติบางประการของสารละลาย
PDF
กรด เบสและสมดุลไอออน - Ion Equilibrium
PDF
วิทยาศาสตร์กายภาพ 1 เรื่อง อากาศ
PDF
ปริมาณสารสัมพันธ์ - Stoichiometry
PDF
PDF
การสำรวจพฤติกรรมการใช้โทรศัพท์ชั้นมัธยมศึกษาปีที่ 4
PPT
PDF
บทที่ 20 ฟิสิกส์นิวเคลียร์ แก้ไขครั้งที่ 1
PDF
พื้นฐานทฤษฎีอะตอมและโครงแบบอิเล็กตรอน
DOCX
แบบฝึกหัดแรงและการเคลื่อนที่
PDF
แผนการจัดการเรียนรู้ที่ 3
PDF
PDF
การคำนวณพลังงานของปฏิกิริยา
PDF
การแปรผันทางพันธุกรรม (Genetic variation)
PDF
ชุดกิจกรรมการเรียนรู้ เรื่องอัตราการเกิดปฏิกิริยาเคมี
PDF
เอกสารประกอบการเรียน เรื่อง อัตราการเกิดปฏิกิริยาเคมี
PPT
PDF
แนวคิดเกี่ยวกับการเกิดปฏิกิริยาเคมี เล่ม3
PDF
หน่วยที่ 4 สูตรเคมี (point)
PDF
PDF
50 ตรีโกณมิติ ตอนที่7_กราฟของฟังก์ชันตรีโกณมิติ
PDF
PDF
PDF
ฟิสิกส์ 5 ไฟฟ้าสถิตย์ ตอนที่ 4
PDF
มวลอะตอม มวลโมเลกุล มวลไอออน
PDF
ตะลุยโจทย์ข้อสอบ งานและพลังงาน
PDF
เล่ม 5 ปฏิกิริยาเคมีในชีวิตประจำวัน
PDF
PPT
PPT
More Related Content
PDF
สมบัติบางประการของสารละลาย
PDF
กรด เบสและสมดุลไอออน - Ion Equilibrium
PDF
วิทยาศาสตร์กายภาพ 1 เรื่อง อากาศ
PDF
ปริมาณสารสัมพันธ์ - Stoichiometry
PDF
PDF
การสำรวจพฤติกรรมการใช้โทรศัพท์ชั้นมัธยมศึกษาปีที่ 4
PPT
PDF
บทที่ 20 ฟิสิกส์นิวเคลียร์ แก้ไขครั้งที่ 1
What's hot
PDF
พื้นฐานทฤษฎีอะตอมและโครงแบบอิเล็กตรอน
DOCX
แบบฝึกหัดแรงและการเคลื่อนที่
PDF
แผนการจัดการเรียนรู้ที่ 3
PDF
PDF
การคำนวณพลังงานของปฏิกิริยา
PDF
การแปรผันทางพันธุกรรม (Genetic variation)
PDF
ชุดกิจกรรมการเรียนรู้ เรื่องอัตราการเกิดปฏิกิริยาเคมี
PDF
เอกสารประกอบการเรียน เรื่อง อัตราการเกิดปฏิกิริยาเคมี
PPT
PDF
แนวคิดเกี่ยวกับการเกิดปฏิกิริยาเคมี เล่ม3
PDF
หน่วยที่ 4 สูตรเคมี (point)
PDF
PDF
50 ตรีโกณมิติ ตอนที่7_กราฟของฟังก์ชันตรีโกณมิติ
PDF
PDF
PDF
ฟิสิกส์ 5 ไฟฟ้าสถิตย์ ตอนที่ 4
PDF
มวลอะตอม มวลโมเลกุล มวลไอออน
PDF
ตะลุยโจทย์ข้อสอบ งานและพลังงาน
PDF
เล่ม 5 ปฏิกิริยาเคมีในชีวิตประจำวัน
PDF
Similar to chemical bonding
PPT
PPT
PDF
PDF
PDF
พันธะโคเวเลนต์ Covalent Bond
PDF
PPT
PPT
PDF
PPT
PDF
PDF
พันธะเคมี-(Chemical Bonding)มทร.ล้านนา.pdf
PDF
PDF
PDF
SLIDE-01403117-CH02-CHEMICALBOND-FULL.pdf
PPT
PDF
PDF
PDF
PDF
chemical bonding 1. โรงเรียนมหิดลวิทยานุสรณ
(โรงเรียนวิทยาศาสตร)
พันธะเคมี
(Chemical Bond)
นายสุนทร พรจําเริญ
ครูชํานาญการ สาขาวิชาเคมี
โรงเรียนมหิดลวิทยานุสรณ
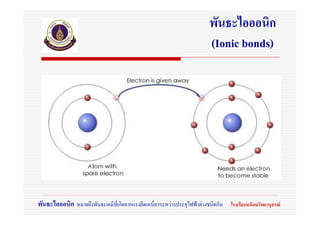
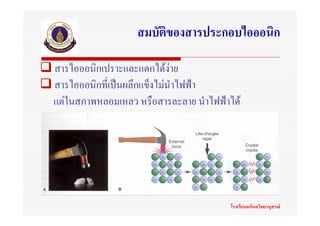
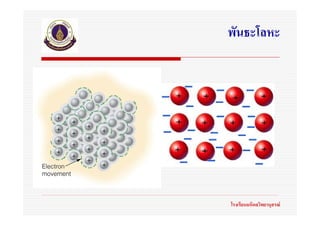
2. พันธะไอออนิก
(Ionic bonds)
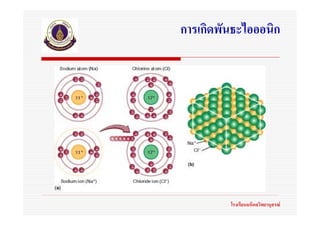
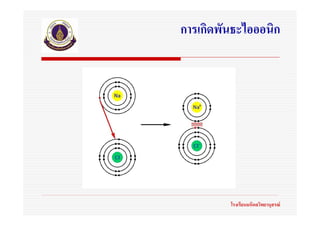
พันธะไอออนิก หมายถึงพันธะเคมีที่เกิดจากแรงยึดเหนี่ยวระหวางประจุไฟฟาตางชนิดกัน โรงเรียนมหิดลวิทยานุสรณ
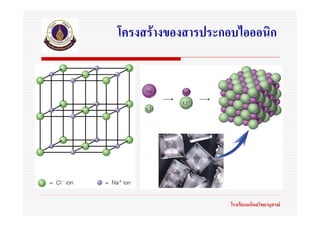
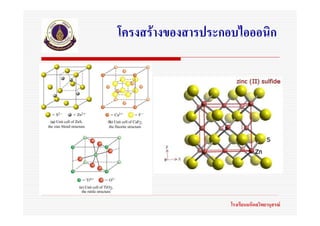
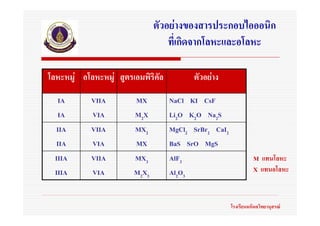
3. 4. 5. 6. 7. 8. ตัวอยางของสารประกอบไอออนิก
ที่เกิดจากโลหะและอโลหะ
โลหะหมู อโลหะหมู สูตรเอมพิริคัล ตัวอยาง
IA VIIA MX NaCl KI CsF
IA VIA M2X Li2O K2O Na2S
IIA VIIA MX2 MgCl2 SrBr2 CaI2
IIA VIA MX BaS SrO MgS
IIIA VIIA MX3 AlF3 M แทนโลหะ
IIIA VIA M2X3 Al2O3 X แทนอโลหะ
โรงเรียนมหิดลวิทยานุสรณ
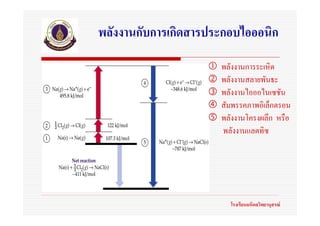
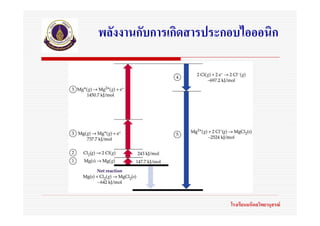
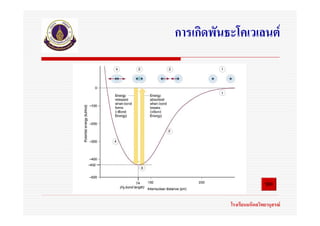
9. พลังงานกับการเกิดสารประกอบไอออนิก
พลังงานการระเหิด
พลังงานสลายพันธะ
พลังงานไอออไนเซชัน
สัมพรรคภาพอิเล็กตรอน
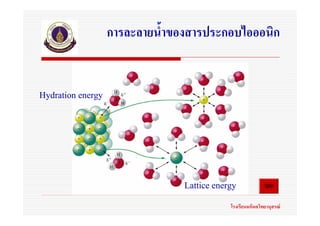
พลังงานโครงผลึก หรือ
พลังงานแลตทิซ
โรงเรียนมหิดลวิทยานุสรณ
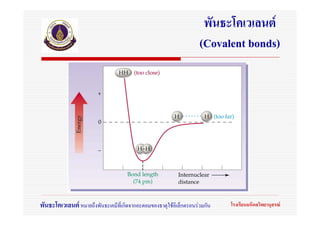
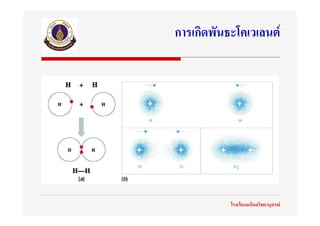
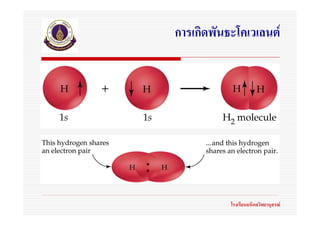
10. 11. 12. 13. 14. พันธะโคเวเลนต
(Covalent bonds)
พันธะโคเวเลนต หมายถึงพันธะเคมีที่เกิดจากอะตอมของธาตุใชอิเล็กตรอนรวมกัน โรงเรียนมหิดลวิทยานุสรณ
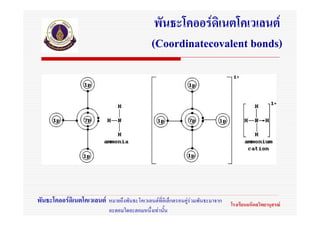
15. 16. 17. 18. 19. 20. 21. 22. 23. พันธะโคออรดิเนตโคเวเลนต
(Coordinatecovalent bonds)
พันธะโคออรดิเนตโคเวเลนต หมายถึงพันธะโคเวเลนตที่อิเล็กตรอนคูรวมพันธะมาจาก โรงเรียนมหิดลวิทยานุสรณ
อะตอมใดอะตอมหนึ่งเทานั้น
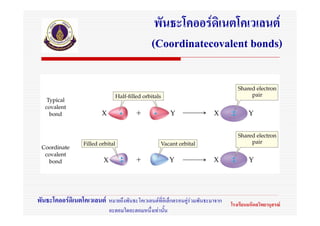
24. พันธะโคออรดิเนตโคเวเลนต
(Coordinatecovalent bonds)
พันธะโคออรดิเนตโคเวเลนต หมายถึงพันธะโคเวเลนตที่อิเล็กตรอนคูรวมพันธะมาจาก โรงเรียนมหิดลวิทยานุสรณ
อะตอมใดอะตอมหนึ่งเทานั้น
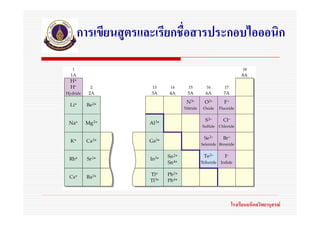
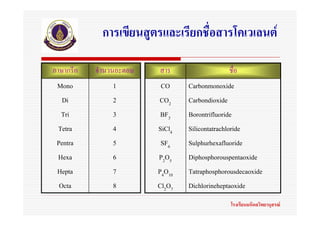
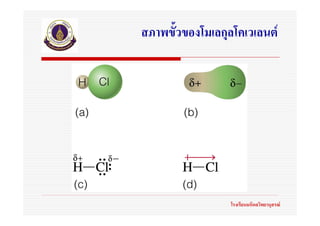
25. การเขียนสูตรและเรียกชื่อสารโคเวเลนต
ภาษากรีก จํานวนอะตอม สาร ชื่อ
Mono 1 CO Carbonmonoxide
Di 2 CO2 Carbondioxide
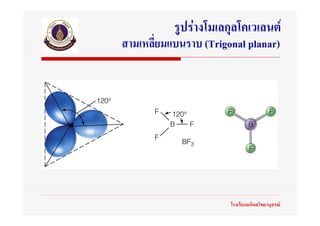
Tri 3 BF3 Borontrifluoride
Tetra 4 SiCl4 Silicontatrachloride
Pentra 5 SF6 Sulphurhexafluoride
Hexa 6 P2O5 Diphosphorouspentaoxide
Hepta 7 P4O10 Tatraphosphorousdecaoxide
Octa 8 Cl2O7 Dichlorineheptaoxide
โรงเรียนมหิดลวิทยานุสรณ
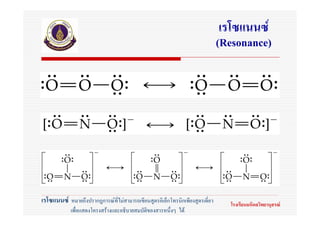
26. 27. 28. 29. 30. เรโซแนนซ
(Resonance)
เรโซแนนซ หมายถึงปรากฎการณที่ไมสามารถเขียนสูตรอิเล็กโทรนิกเพียงสูตรเดี่ยว โรงเรียนมหิดลวิทยานุสรณ
เพื่อแสดงโครงสรางและอธิบายสมบัติของสารหนึ่งๆ ได
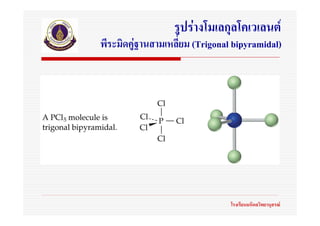
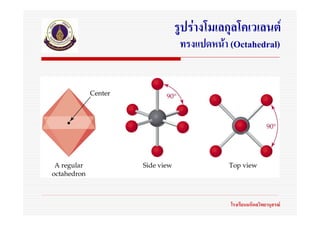
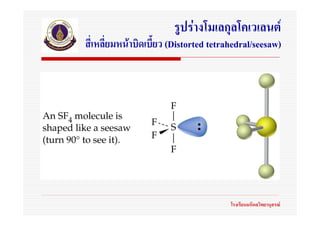
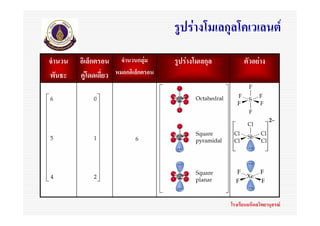
31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. ทฤษฎี VSEPR
(Valence Shell Electron Pair Repulsion)
อะตอมตางๆ ในโมเลกุลเกิดพันธะกันดวยคูอิเล็กตรอน
วงนอกสุดเรียกวา อิเล็กตรอนคูสรางพันธะ(bonding pair)
โดยอะตอมอาจยึดกันดวยอิเล็กตรอนคูสรางพันธะ 1 คู
(พันธะเดี่ยว) หรือ มากกวา (พหุพันธะ)
ทฤษฎี VSEPR หมายถึงทฤษฎีการผลักกันของคูอเิ ล็กตรอนวงนอกสุด โรงเรียนมหิดลวิทยานุสรณ
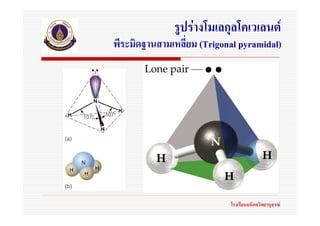
50. ทฤษฎี VSEPR
(Valence Shell Electron Pair Repulsion)
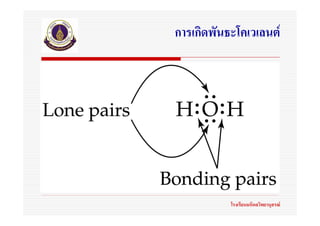
อะตอมบางอะตอมในโมเลกุลอาจมีอิเล็กตรอน
คูที่ไมสรางพันธะ(nonbonding pair)หรืออิเล็กตรอน
คูโดดเดี่ยว(lone pair)
ทฤษฎี VSEPR หมายถึงทฤษฎีการผลักกันของคูอเิ ล็กตรอนวงนอกสุด โรงเรียนมหิดลวิทยานุสรณ
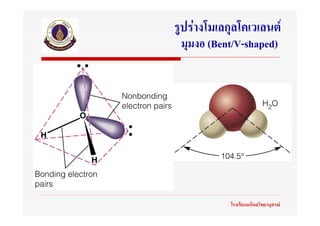
51. ทฤษฎี VSEPR
(Valence Shell Electron Pair Repulsion)
อิเล็กตรอนคูสรางพันธะและอิเล็กตรอนคูโดดเดี่ยว
รอบอะตอมใดๆ ในโมเลกุลเปนกลุมหมอกอิเล็กตรอน
ที่มีประจุลบ จึงพยายามอยูหางกันใหมากที่สุดเพื่อใหมี
แรงผลักซึ่งกันและกันของอิเล็กตรอนเหลานีนอยที่สุด
้
และพลังงานของโมเลกุลมีคานอยที่สุด
ทฤษฎี VSEPR หมายถึงทฤษฎีการผลักกันของคูอเิ ล็กตรอนวงนอกสุด โรงเรียนมหิดลวิทยานุสรณ
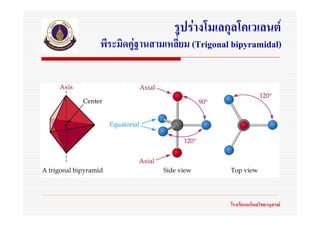
52. ทฤษฎี VSEPR
(Valence Shell Electron Pair Repulsion)
อิเล็กตรอนคูโดดเดี่ยวครอบครองที่วางมากกวา
อิเล็กตรอนคูสรางพันธะ
อิเล็กตรอนที่สรางพหุพนธะครอบครองที่วาง
ั
มากกวาอิเล็กตรอนที่สรางพันธะเดี่ยว
ทฤษฎี VSEPR หมายถึงทฤษฎีการผลักกันของคูอเิ ล็กตรอนวงนอกสุด โรงเรียนมหิดลวิทยานุสรณ
53. ทฤษฎีพันธะเวเลนต
(Valence bond theory)
พันธะโคเวเลนตเกิดขึ้นโดยออรบิทัลอะตอม
(Atomic orbital:AO) วงนอกสุดที่มีอิเล็กตรอนบรรจุอยู
เพียงตัวเดียวซอน(Overlap) กับออรบิทัลอะตอมวง
นอกสุดที่มีอิเล็กตรอนเพียงตัวเดียวของอีกอะตอมหนึ่ง
และอิเล็กตรอนทั้งสองจะจัดตัวใหมีสปนตรงกันขาม
อยูในออรบิทัลนี้
ทฤษฎีพนธะเวเลนต หมายถึงทฤษฎีที่ใชอธิบายการเกิดพันธะโคเวเลนต
ั โรงเรียนมหิดลวิทยานุสรณ
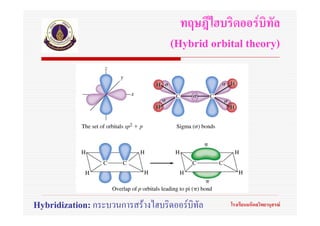
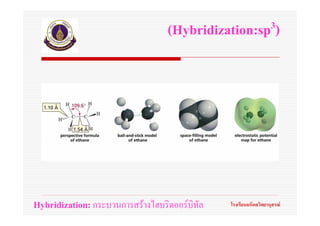
54. ทฤษฎีไฮบริดออรบิทัล
(Hybrid orbital theory)
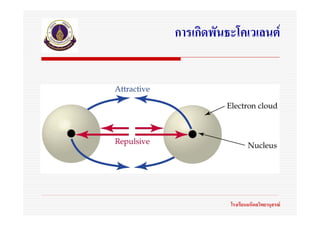
กลาววา “เมื่ออะตอม 2 อะตอมเขาใกลกันอิทธิพลของ
นิวเคลียสของอะตอมทั้งสองจะทําใหพฤติกรรมของอิเล็กตรอน
ในแตละอะตอมเปลี่ยนแปลงไป ดังนันออรบิทลของอะตอมที่
้ ั
เกิดพันธะจะแตกตางไปจากออรบิทัลอะตอมในอะตอมเดี่ยว
เวเลนตออรบทัลที่มีพลังงานใกลเคียงกันของอะตอมเดียวกันจะ
ิ ่
เขามารวมกันเกิดเปนออรบทัลอะตอมใหมซงมีรูปราง ทิศทาง
ิ ึ่
และพลังงานเปลี่ยนไปจากเดิม”
Hybridization: กระบวนการสรางไฮบริดออรบิทัล โรงเรียนมหิดลวิทยานุสรณ
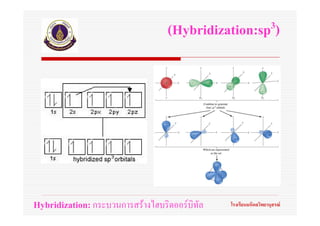
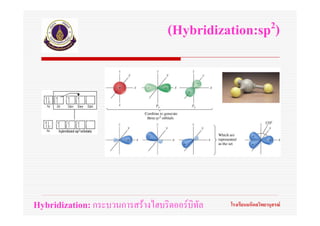
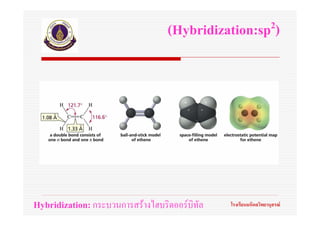
55. ทฤษฎีไฮบริดออรบิทัล
(Hybrid orbital theory)
ออรบทัลอะตอมที่เกิดขึ้นใหมเรียกวา ไฮบริดออรบิทัลอะตอม
ิ
(Hybrid atomic orbital) หรือ ไฮบริดออรบิทัล(Hybrid orbitals)
จํานวนไฮบริดออรบิทลที่ไดนี้จะเทากับจํานวนออรบิทัลอะตอม
ั
ที่มารวมกัน
Hybridization: กระบวนการสรางไฮบริดออรบิทัล โรงเรียนมหิดลวิทยานุสรณ
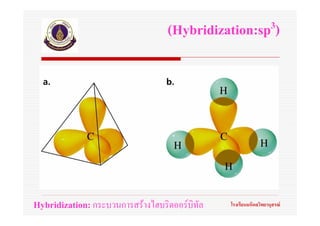
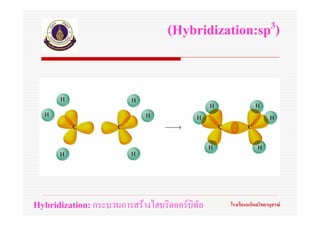
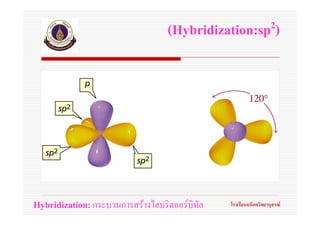
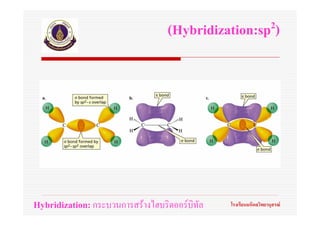
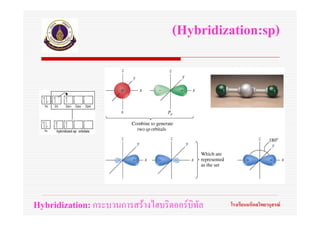
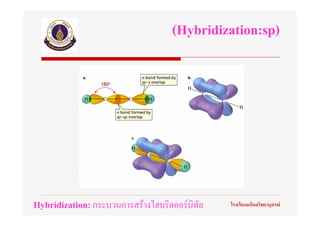
56. ทฤษฎีไฮบริดออรบิทัล
(Hybrid orbital theory)
Hybridization: กระบวนการสรางไฮบริดออรบิทัล โรงเรียนมหิดลวิทยานุสรณ
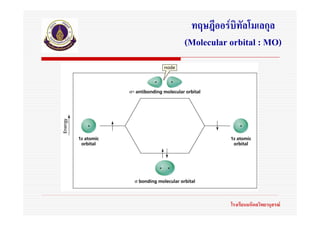
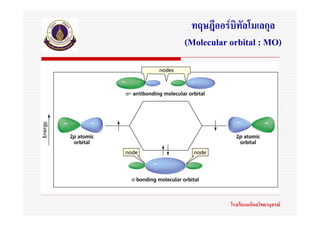
57. 58. 59. 60. 61. 62. 63. 64. 65. 66. 67. 68. 69. 70. 71. ทฤษฎีออรบิทัลโมเลกุล
(Molecular orbital : MO)
มีสมมุติฐานเกี่ยวกับการเกิดพันธะ ดังนี้
เมื่ออะตอมเขาใกลกัน ออรบิทลอะตอมของอิเล็กตรอน
ั
วงนอกสุดจะรวมกันเกิดเปน ออรบทัลโมเลกุล(Molecular
ิ
Orbital) ซึ่งแสดงลักษณะเฉพาะของทั้งโมเลกุลไมไดเปน
ของอะตอมใดอะตอมหนึงในโมเลกุล โดยจํานวนออรบทัล
่ ิ
ในโมเลกุลที่เกิดขึ้นเทากับจํานวนออรบิทลอะตอมที่มารวม
ั
กัน
โรงเรียนมหิดลวิทยานุสรณ
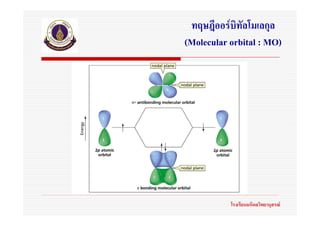
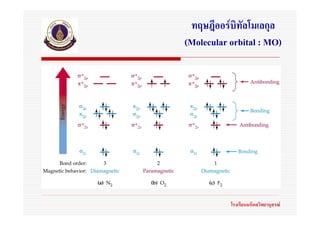
72. ทฤษฎีออรบิทัลโมเลกุล
(Molecular orbital : MO)
ออรบิทัลโมเลกุลจะจัดเรียงตัวตามลําดับพลังงานที่เพิ่มขึน
้
พลังงานสัมพัทธของออรบิทัลในโมเลกุลเหลานี้สรุปไดจากการ
ทดลองเกี่ยวกับสเปกตรัมและสมบัติแมเหล็กของโมเลกุล
เวเลนตอิเล็กตรอนในโมเลกุลจะบรรจุอยูในออรบทัล
ิ
โมเลกุล ตามหลักกีดกันของเพาลีและเปนไปตามกฎของฮุนด
โรงเรียนมหิดลวิทยานุสรณ
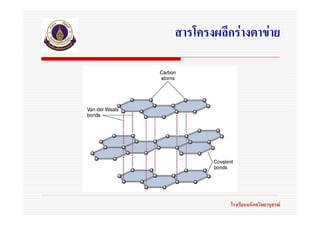
73. 74. 75. 76. 77. 78. 79. 80. 81. 82. 83. 84. 85. 86. 87. แรงยึดเหนี่ยวระหวางโมเลกุล
(Intermolecular force)
แรงแวนเดอรวาลส(Van der Waals’force)
แรงลอนดอน(London force หรือ dispersion force)
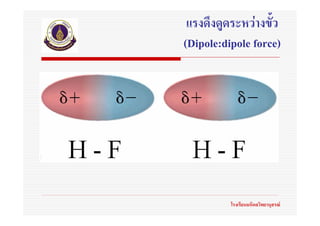
แรงดึงดูดระหวางขั้ว(Dipole:dipole force)
พันธะไฮโดรเจน(Hydrogen bond)
โรงเรียนมหิดลวิทยานุสรณ
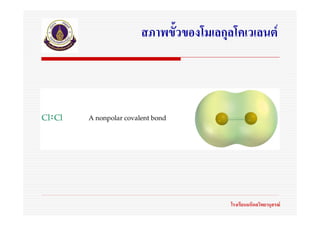
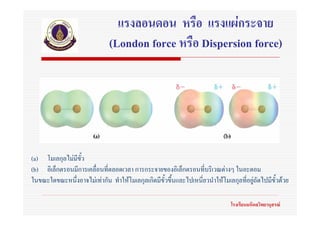
88. 89. แรงลอนดอน หรือ แรงแผกระจาย
(London force หรือ Dispersion force)
(a) โมเลกุลไมมีขั้ว
(b) อิเล็กตรอนมีการเคลื่อนที่ตลอดเวลา การกระจายของอิเล็กตรอนทีบริเวณตางๆ ในอะตอม
่
ในขณะใดขณะหนึงอาจไมเทากัน ทําใหโมเลกุลเกิดมีขั้วขึนและไปเหนี่ยวนําใหโมเลกุลที่อยูถัดไปมีขวดวย
่ ้ ั้
โรงเรียนมหิดลวิทยานุสรณ
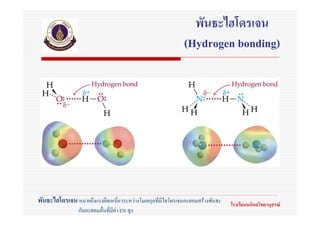
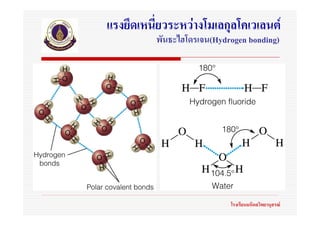
90. พันธะไฮโดรเจน
(Hydrogen bonding)
พันธะไฮโดรเจน หมายถึงแรงยึดเหนี่ยวระหวางโมเลกุลทีมีไฮโดรเจนอะตอมสรางพันธะ
่ โรงเรียนมหิดลวิทยานุสรณ
กับอะตอมอื่นที่มีคา EN สูง
91. 92. 93. 94. 95. 96. 97. 98.