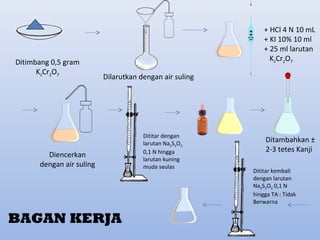
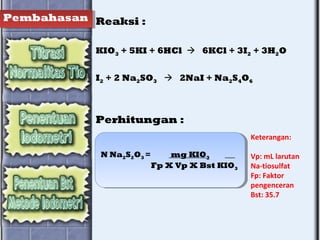
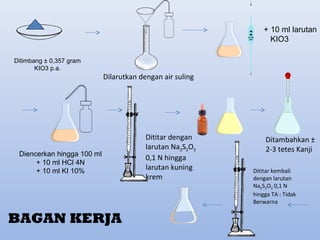
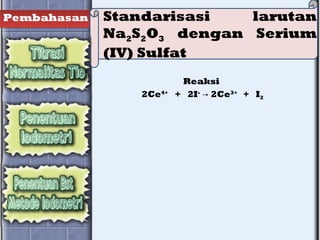
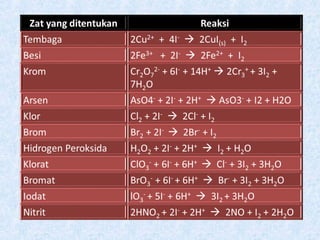
Dokumen tersebut membahas beberapa metode analisis volumetri yaitu yodometri untuk menentukan kadar zat oksidator seperti besi dan tembaga dengan cara memanfaatkan reaksi oksidasi-reduksi antara zat tersebut dengan larutan kalium iodida yang menghasilkan iod bebas yang kemudian dititrasi dengan larutan natrium tiosulfat. Metode lain seperti penggunaan kalium kromat, kalium iodat, dan larutan iod stand













![Pembahasan Penentuan Kadar Cu(II) dalam
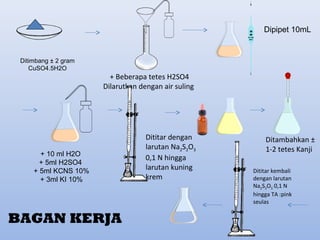
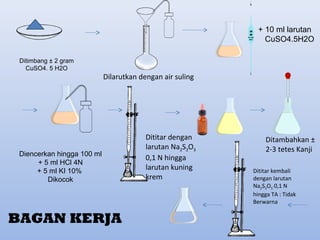
Terusi (CuSO4. 5H2O) Cara
Brunns
Dasar :
Dalam suasana asam, Cu2+
akan
bereaksi dengan KCNS sehingga akan
menghasilkan tembaga (II) rodanida
[Cu(CNS)2]. Kemudian Cu(CNS)2 akan
mengoksidasikan KI sehingga
menghasilkan I2 bebas. I2 bebas akan
dititar dengan Na2S2O3 yang dengan
penambahan indikator kanji akan
mencapai TA yaitu larutan tidak
berwarna dan endapan berwarna
lembayung dari Cu(CNS)2](https://image.slidesharecdn.com/tugaskimiaanalisiskelompok2-kelasxi-4sabrihudaalainaamaliaadisetyanurghaffarjelitahelianisa-150214193213-conversion-gate02/85/Metode-Yodometri-dan-Penentuan-Bst-22-320.jpg)