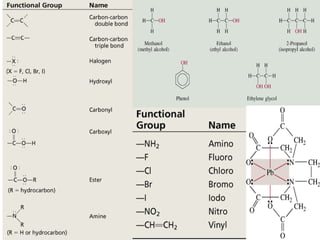
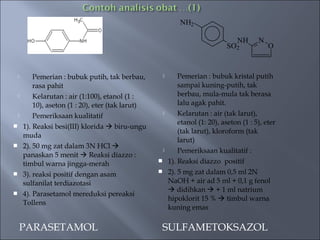
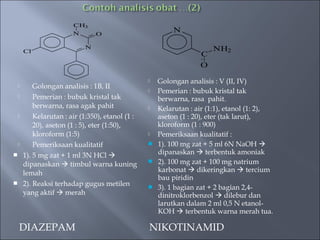
Dokumen ini menjelaskan berbagai teknik dan reaksi analisis untuk mengidentifikasi senyawa obat dan bahan kimia, termasuk deteksi senyawa nitrogen, sulfida, dan halogen. Metode yang digunakan meliputi uji larutan, pemisahan, dan pemeriksaan organoleptik, serta reaksi kimia spesifik seperti reaksi idioform dan reaksi Schiff. Berbagai senyawa dan hasil reaksinya dicatat untuk analisis lebih lanjut dalam konteks kimia farmasi.

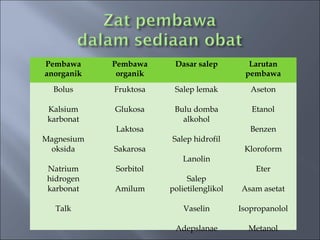







![ Senyawa Nitrogen terdapat dalam bentuk nitrat dan nitrit;
sebagai senyawa nitro; amin primer, sekunder, atau tersier
yang bersifat basa; sebagai amonium kuartener; golongan
amin aromatik; asam amida netral; asam amino; dan dalam
bentuk lain.
Semua nitrat larut dalam air, dengan menambahkan FeSO4
dan H2SO4 pekat terbentuk cincin berwarna coklat.
Pemeriksaan Senyawa nitro aromatik (niklosamida,
nitrazepam, kloramfenikol)
50 mg zat dalam 3 ml etanol 4 ml air + 200 mg Zn + 3 ml
HCl encer dipanaskan 2 ml filtrat + 2 tetes pereaksi
diazzo I + diazzo II terbentuk endapan jingga
[pereaksi Diazzo I ( 10 g NaNO2 dalam 100 ml aquadest),
pereaksi Diazzo II (0,25 g 2-naftol dalam 100 ml 3N NaOH)]](https://image.slidesharecdn.com/analisissenyawaobat-121214100645-phpapp02/85/Analisis-senyawa-obat-10-320.jpg)