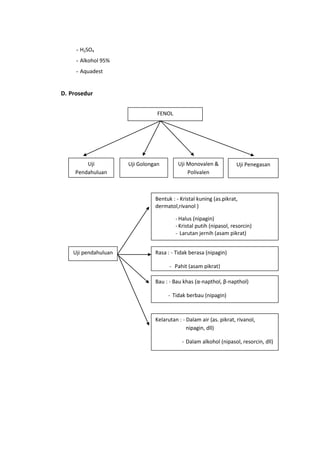
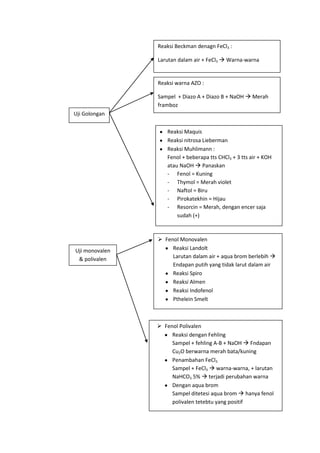
Laporan ini memberikan ringkasan dari praktikum analisis kualitatif senyawa fenol. Dua sampel diuji untuk menentukan jenis fenolnya. Sampel pertama diidentifikasi sebagai rivanol berdasarkan hasil uji organoleptik, golongan, dan penegasan. Sampel kedua diidentifikasi sebagai β-naphtol melalui serangkaian uji serupa. Laporan ini berisi tujuan, teori dasar, alat dan bahan, prosedur