bioavailabilitas.pptx
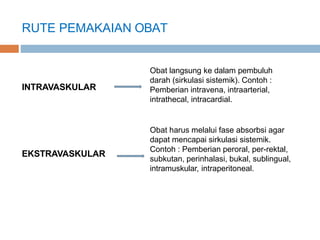
- 1. RUTE PEMAKAIAN OBAT INTRAVASKULAR Obat langsung ke dalam pembuluh darah (sirkulasi sistemik). Contoh : Pemberian intravena, intraarterial, intrathecal, intracardial. Obat harus melalui fase absorbsi agar dapat mencapai sirkulasi sistemik. Contoh : Pemberian peroral, per-rektal, subkutan, perinhalasi, bukal, sublingual, intramuskular, intraperitoneal. EKSTRAVASKULAR
- 2. Tablet/ Kapsul Granul/ Agregat Partikel Halus Obat dlm larutan (invivo/invitro Obat dlm darah, cairan dan jaringan lain Kadar obat dlm reseptor Respon farmakologi Respon klinik/terapeutik Absorpsi (in vivo) Disolusi Disolusi (mayor) Dosolusi Disintegrasi Disintegrasi BIOFARMA- MASETIKA FARMA- KOKINETIKA FARMA- SETIKA FARMAKO- DINAMIKA Penentuan aktifitas obat mulai dari bentuk sediaan sampai memberi respon. Contoh untuk pemberian per-oral
- 3. Plasma concentration time profile concentration Cmax AUC Tmax
- 4. Important Pharmacokinetic Parameters AUC : area under the concentration-time curve measure of the extent of bioavailability Cmax : the observed maximum concentration of drug measure of both the rate of absorption and the extent of bioavailability Tmax : the time after administration of drug at which Cmax is observed measure of the rate of absorption
- 5. BIOAVAILABILITAS o Jumlah obat yang terabsorpsi dari bentuk sediaan farmasetiknya disebut sebagai bioavailablitas produk tersebut. o Penentuan bioavailabilitas suatu produk sangat penting untuk mengetahui jumlah serta kecepatan suatu obat diabsorpsi. Hal ini akan menggambarkan besarnya availabilitas sistemik dari suatu bentuk sediaan obat. o Availabilitas sistemik suatu obat dicerminkan oleh luasnya area di bawah kurva kadar obat (AUC).
- 6. Bioavailabilitas (ketersediaan hayati) ialah jumlah relatif (persentase) dari obat yang masuk ke sirkulasi sistemik sesudah pemberian obat dalam sediaan tertentu, serta kecepatan peningkatan kadar obat dalam sirkulasi sistemik. BIOAVAILABILITAS
- 7. BIOAVAILABILITAS Bila pada absorpsi sempurna (F=1,0), availabilitas sistemik dari dosis oral ialah 100 %, dimana luas AUC-nya sama dengan luas AUC pada pemberian IV. Dalam hal ini obat secara sempurna, terserap melalui saluran cerna, dan tidak mengalami biotransformasi yang berarti pada saat ‘first pass’ melalui hati.
- 8. Which formulation has higher bioavailability ?
- 9. Area di bawah kurva konsentrasi obat-waktu dari (AUC) berguna total obat yang sebagai ukuran utuh tidak berubah jumlah yang mencapai sirkulasi sistemik. F . Do AUC = Ke . Vd F = Fraksi dosis terabsorpsi BIOAVAILABILITAS
- 10. Setelah pemberian intavena (IV), F = 1 , karena seluruh dosis segera terdapat dalam sirkulasi sistemik. Oleh karena itu obat dianggap tersedia sempurna setelah pemberian intravena (IV). Setelah pemberian obat secara oral F dapat berbeda mulai dari F = 0 (obat tidak terabsorpsi sempurna) sampai F = 1 (obat terabsorpsi sempurna). BIOAVAILABILITAS
- 11. Kecepatan bioavailabilitas membandingkan (Tmax dan dapat diukur T lag), sedangkan dengan derajat bioavailabiitas dapat dibandingkan dengan mengukur (Cmax danAUC). Nilai Ka tidak pernah digunakan kecepatan bioavailabilitas. Sedangkan sebagai nilai Kel parameter dan t1/2 harus menunjukkan nilai yang sama pada saat perbandingan dilakukan. BIOAVAILABILITAS
- 12. Bioavilabilitas Absolut Bioavailabilitas absolut yaitu suatu angka yang menunjukkan rasio ketersediaan hayati suatu obat yang diberikan ekstravaskular terhadap intravaskular, membandingkan dapat AUC diukur produk setelah pemberian dengan yang oral dan bersangkutan intavena (iv)
- 13. Bioavailabilitas Absolut Dari data plasma ditentukan sebagai berikut : Dari data urine ditentukan sebagai berikut :
- 14. 15 IV bolus 0 5 10 20 25 30 0 15 Time 40 20 60 100 80 Concentration Area under concentration curve (AUC)
- 15. 16 0 5 10 20 25 30 0 15 Time 40 20 60 100 80 Concentration Oral dosage form (product A) Area under concentration curve (AUC)
- 16. 17 Absolute bioavailability 0 5 10 20 25 30 0 15 Time 20 40 60 80 100 Concentration For the same dose (IV vs. Oral), the bioavailability is given by: IV AUC F AUCoral
- 17. Relative bioavailability The relative bioavailability is the systemic availability of a drug from one drug product (A) compared to another drug product (B)
- 18. 19 0 5 10 20 25 30 0 15 Time 40 20 60 100 80 Concentration Oral dosage form (product A) Area under concentration curve (AUC)
- 19. 20 0 5 10 20 25 30 0 15 Time 40 20 60 100 80 Concentration Oral dosage form (product B) Area under concentration curve (AUC)
- 20. 21 0 5 10 20 25 30 0 15 Time 20 40 60 80 100 Concentration Relative bioavailability For the same dose AUCoral (B) (IV vs. Oral), the bioavailability is given by: F AUCoral (A)
- 21. Bioavailabilitas Relatif Bioavailabilitas relatif adalah suatu ukuran yang menunjukkan perbandingan kecepatan dan derajat suatu sediaan obat mencapai sirkulasi sistemik terhadp sediaan lain yang digunakan sebagai pembanding.
- 22. Bioavailabilitas Relatif Dari data plasma ditentukan sebagai berikut : Dari data urine ditentukan sebagai berikut : Adalah jumlah total obat yang dieksresikan dalam urin
- 23. Bioekivalensi Studi bioekivalensi dilakukan karena banyak produk obat yang dianggap ekivalen farmasetik tidak memberi efek terapetik yang sebanding pada penderita.
- 24. Pharmaceutical Equivalents Possible Differences Drug particle size Excipients Manufacturing Equipment or Process Site of manufacture T est Reference Could lead to differences in product performance in vivo Possible Bioinequivalence
- 25. Bioekivalensi Dua sediaan dikatakan bioekivalen apabila nilai parameter-parameter farmakokinetika yang dibandingkan tidak menunjukkan perbedaan yang bermakna secara statistik, terutama Cmax, Tmax dan AUC, ataupun kalau ada perbedaan tersebut tidak lebih dari 20 %.
- 26. Bioekivalensi Biokivalensi juga mencakup pengertian kemanfaatan atau efek suatu produk obat. Namun ketersediaan hayati tidak selalu identik dengan kemanfaatan hayati obat, oleh karena pada uji ketersediaan hayati, yang diukur adalah parameter-parameter jumlah atau kadar obat, bukan parameter-parameter efek obat.
- 27. Contoh Uji Bioekivalensi OBAT UJI T max (jam) Cmax (µg/ml) AUC (mg/ml.jam) Generik 0,8 ± 0,1 2,0 ± 0,1 5,8 ± 0,7 Non Generik/Pembanding Tabel : Uji Bioekivalensi dar 1,0 ± 0,0 i Furosemid Gener 2,4 ± 0,2 ik dan Non Gene 6,9 ± 0,8 rik
- 28. Contoh Uji Bioekivalensi Dari data uji bioekivalensi di atas dapat disimpulkan sebagai berikut : menunjukkan pembanding cenderung Nilai ketiga parameter ketersediaan hayati mem- berikan derajat ketersediaan hayati yang sedikit lebih baik. Ini dapat dilihat dari C max dan AUCo yang sedikit lebih tinggi. Tetapi nilai ini tidak mencapai kebermaknaan statistik. (digunakan uji t-pasangan, p > 0,05).
- 29. Dari segi kecepatan (rate), generik nampaknya sedikit lebih baik, ditunjuk-kan dengan nilai T max Tetapi perbedaan yang inipun lebih juga singkat. tidak bermakna secara statistik. eliminasi kedua Kecepatan didapatkan sama, sediaan waktu paro eliminasi adalah 1,8 ± 0,2 jam dan 1,9 ± 0,3 jam untuk Generik dan Non Generik. Lanjutan Contoh Uji Bioekivalensi
- 30. Contoh Uji Bioekivalensi Profil kadar Furosemid kedua sediaan menunjukkan kurva yang identik
Editor's Notes
- daerah di bawah kurva konsentrasi-waktu mengukur tingkat bioavailabilitas konsentrasi maksimum obat yang diamati ukuran laju absorpsi dan tingkat bioavailabilitas waktu setelah pemberian obat di mana Cmax diamati mengukur tingkat penyerapan