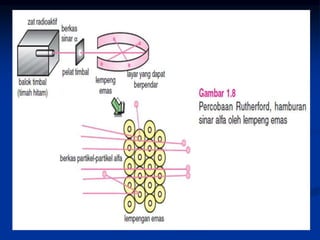
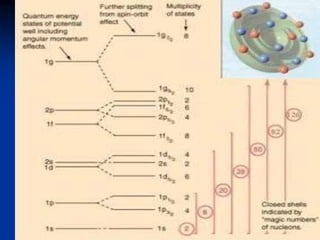
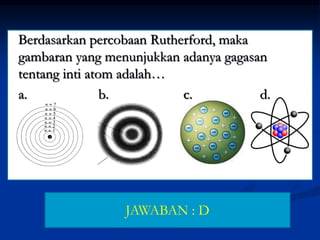
Dokumen tersebut merangkum penjelasan tentang model-model inti atom, dimulai dari penemuan inti atom oleh Rutherford pada tahun 1911 melalui eksperimen hamburan partikel alfa oleh lempeng emas. Kemudian dijelaskan model tetes cairan dan model kulit inti sebagai model-model yang digunakan untuk mewakili struktur inti atom, beserta rumus yang terkait seperti rumus massa semi empiris. Perubahan sifat-sifat inti