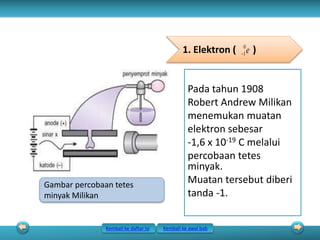
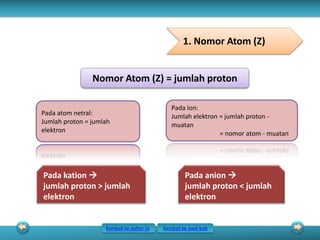
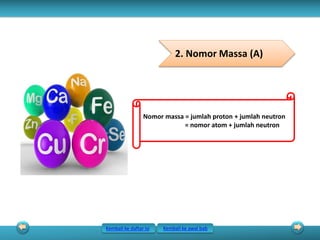
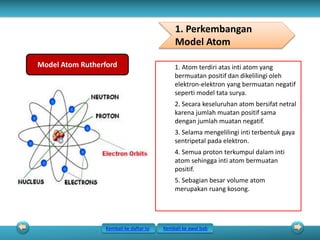
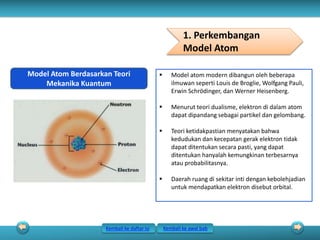
Bab ini membahas tentang struktur atom, yang terdiri dari partikel-partikel penyusun atom seperti elektron, proton, dan neutron. Juga dibahas mengenai nomor atom, nomor massa, dan konsep isotop, isoton, isobar, dan isoelektron. Selanjutnya dijelaskan perkembangan model-model atom seperti model Dalton, Thomson, Rutherford, Bohr, hingga model atom modern berdasarkan mekanika kuantum.