More Related Content
Similar to ใบความรู้ เรื่อง แอลเคน
Similar to ใบความรู้ เรื่อง แอลเคน (16)
ใบความรู้ เรื่อง แอลเคน
- 1. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
แอลเคน (alkane) หรือ พาราฟิน
เป็นสารประกอบไฮโดรคาร์บอนชนิดอิ่มตัว สูตรโมเลกุลทั่วไปของแอลเคน คือ CnH2n+2 เมื่อ n คือ
จานวนอะตอมของคาร์บอน
การเรียกชื่อแอลเคน แบ่งเป็น 2 ชนิด
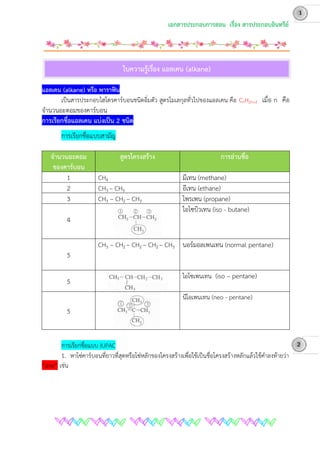
การเรียกชื่อแบบสามัญ
จานวนอะตอม
ของคาร์บอน
สูตรโครงสร้าง การอ่านชื่อ
1 CH4 มีเทน (methane)
2 CH3 – CH3 อีเทน (ethane)
3 CH3 – CH2 – CH3 โพรเพน (propane)
4
ไอโซบิวเทน (iso - butane)
5
CH3 – CH2 – CH2 – CH2 – CH3 นอร์มอลเพนเทน (normal pentane)
5
ไอโซเพนเทน (iso – pentane)
5
นีโอเพนเทน (neo - pentane)
การเรียกชื่อแบบ IUPAC
1. หาโซ่คาร์บอนที่ยาวที่สุดหรือโซ่หลักของโครงสร้างเพื่อใช้เป็นชื่อโครงสร้างหลักแล้วใช้คาลงท้ายว่า
“ane” เช่น
ใบความรู้เรื่อง แอลเคน (alkane)
1
2
- 2. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
อ่านว่า hexane
อ่านว่า octane
2. เมื่อมีหมู่แทนที่ (substituent groups) เกาะอยู่บนโครงร้างหลัก ให้อ่านชื่อหมู่แทนที่นั้นๆ เป็นคา
นาหน้า โดยให้ตาแหน่งของคาร์บอนของโซ่หลักที่หมู่แทนที่นั้นๆ เกาะอยู่โดยเป็นตัวเลขที่น้อยที่สุด ชื่อของหมู่
แทนที่และชื่อโครงสร้างหลักจะเขียนติดกัน แต่ตาแหน่งของหมู่แทนที่จะคั่นด้วยเครื่องหมาย “-” นาหน้าชื่อหมู่
แทนที่นั้น เช่น
2 – methylhexane 3 – ethylhexane
(isoheptane)
3. กรณีที่มีหมู่แทนที่มากกว่า 1 หมู่ ให้ตาแหน่งหมู่แทนที่ในทิศทางที่ให้ผลรวมของตาแหน่งของหมู่
แทนที่มีค่าน้อยที่สุด เรียกหมู่แทนที่เรียงตามอักษรภาษาอังกฤษ เช่น
4 – ethyl – 2 – methylhexane
4. กรณีที่มีหมู่แทนที่ซ้าๆ กัน ใช้อักษณกรีกที่แสดงถึงจานวนหมู่แทนที่ที่ซ้ากันนาหน้าชื่อหมู่แทนที่นั้น
โดยที่ di หมายความว่า มีหมู่แทนที่นั้น 2 หมู่
tri หมายความว่า มีหมู่แทนที่นั้น 3 หมู่
trata หมายความว่า มีหมู่แทนที่นั้น 4 หมู่
3
- 3. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
2,2 – dimethylbutane 2,2,4 - trimethylpentane
2,2,5 – triethyl – 5 – methylheptane
5. เมื่อให้ตาแหน่งหมู่แทนที่แล้วทาให้ตาแหน่งเหมือนกันทั้งสองทิศทาง ให้หมู่ที่ต้องอ่านชื่อก่อน มี
ตาแหน่งที่ต่ากว่า เช่น
3 – bromo – 5 – chloroheptane
6. กรณีที่โครงสร้างหลักมีจานวนคาร์บอนอะตอมที่ยาวที่สุดมากกว่า 1 สายโซ่ ให้เลือกโซ่ที่มีจานวนหมู่
แทนที่มากกว่าเป็นโครงสร้างหลัก
3 – ethyl – 2 – methylhexane
ชนิดของคาร์บอนและไฮโดรเจนในสารประกอบ
สามารถจาแนกชนิดของคาร์บอนของสารประกอบแอลเคนได้เป็น 4 ประเภท ขึ้นอยู่กับจานวนพันธะที่
คาร์บอนดังกล่าวเกิดพันธะกับคาร์บอนอื่นๆ
4
- 4. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
ชนิดของไฮโดรเจนสามารถจาแนกตามชนิดของคาร์บอนอะตอมไฮโดรเจนนั้นเกาะอยู่
สารประกอบไซโคลแอลเคน (Cycloalkane)
ไซโคลแอลเคน คือ แอลเคนที่มีโครงสร้างเป็นวง (cyclic compounds) ไซโคลแอลเคนจึงมีสูตรทั่วไป
เป็น CnH2n การอ่านชื่อเติมคานาหน้าสารว่า “cyclo” ก่อนชื่อของแอลเคนที่แสดงถึงจานวนคาร์บอนในวงและ
เขียนติดกัน เช่น
การเขียนโครงสร้างของไซโคลแอลเคน นิยมเขียนสูตรโครงสร้างแบบโครงมากกว่า เนื่องจากจะทา
ให้โครงสร้างดูเข้าใจง่ายขึ้น
การอ่านชื่อสารประกอบไซโคลแอลเคน
ใช้กฎเกณฑ์คล้ายกับการอ่านชื่อของแอลเคนที่ไม่เป็นวง คือ
1. ถ้าวงไซโคลแอลเคนนั้นมีหมู่แทนที่ให้อ่านวงไซโคลแอลเคนเป็นโครงสร้างหลัก ไม่ต้องแสดงตาแหน่ง
หมู่แทนที่ถ้ามีหมู่แทนที่เพียง 1 หมู่ ถ้าหมู่แทนที่เป็นหมู่ของคาร์บอนที่มีจานวนคาร์บอนอะตอมมากกว่าจานวน
คาร์บอนอะตอมในวงไซโคลแอลเคน ให้อ่านวงไซโคลแอลเคนเป็นหมู่แทนที่ของไฮโดรคาร์บอนหลัก
5
- 5. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
2. การที่มีหมู่แทนที่มากกว่า 1 หมู่ ให้อ่านตามลาดับตัวอักษรภาษาอังกฤษและให้หมู่แทนที่ที่มี
ลาดับอักษรเป็นตาแหน่งที่ 1
3. กรณีที่มีหมู่แทนที่มากกว่า 2 หมู่ขึ้นไป ให้อ่านตามลาดับตัวอักษร หมู่แทนที่ในตาแหน่งที่ 1
จะต้องทาให้หมู่แทนที่อื่นที่อยู่ถัดไปมีตาแหน่งน้อยที่สุด
สมบัติทางกายภาพของแอลเคน
1. มีได้ทั้ง 3 สถานะ คือ แก๊ส (C1 – C4) ของเหลว (C5 – C20) และของแข็ง (C21 ขึ้นไป)
2. เป็นสารประกอบที่ไม่มีสีและไม่มีกลิ่น ดังนั้นเมื่อนามาใช้เป็นเชื้อเพลิงจึงต้องใส่สารที่มีกลิ่นไป
ด้วย เช่น butyl mercaptan เพื่อเป็นตัวบอกให้ทราบว่ามีก๊าซรั่วหรือไม่
3. เป็นโมเลกุลโคเวเลนต์ชนิดไม่มีขั้วจึงไม่ละลายในตัวทาละลายที่มีขั้ว เช่น น้า แต่ละลายได้ดีใน
ตัวทาละลายที่ไม่มีขั้ว เช่น เบนซีน โทลูอีน
4. ไม่นาไฟฟ้าทุกสถานะ
5. สาหรับแอลเคนที่เป็นไอโซเมอร์กัน ชนิดที่เป็นโซ่ตรงจะมีจุดเดือดสูงกว่าชนิดที่เป็นโซ่กิ่ง
เนื่องจากชนิดที่เป็นโซ่ตรงมีพื้นที่ผิวของโมเลกุล ซึ่งจะก่อให้เกิดแรงยึดเหนี่ยงระหว่างโมเลกุลมากกว่าชนิด
ที่เป็นโซ่กิ่ง ยิ่งมีสาขามากเท่าใด จะยิ่งมีจุดเดือดต่าลงเท่านั้น
6. มีความหนาแน่นน้อยกว่าน้า ความหนาแน่นมากที่สุดประมาณ 0.8 g/cm3
ดังนั้นแอลเคนจึง
ลอยน้า แอลเคนที่มีโครงสร้างในลักษณะเดียวกัน เมื่อ C ในโมเลกุลเพิ่มขึ้นความหนาแน่นจะเพิ่มขึ้น
7. ติดไฟง่ายไม่มีเขม่า
8. จุดหลอมเหลวและจุดเดือดเพิ่มขึ้น เมื่อจานวนอะตอมของคาร์บอนเพิ่มขึ้น
6
- 6. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
ปฏิกิริยาของแอลเคน
1. ปฏิกิริยาการเผาไหม้ (combustion oxidation)
CxHy + ( x + 4
y
)O2 xCO2 + 2
y
H2O
ตัวอย่าง C5H12 + 8O2 5CO2 + 6H2O + heat
2C2H6 + 7O2 4CO2 + 6H2O + heat
2.ปฏิกิริยาการแทนที่ (substitution reaction)
หมายถึง ปฏิกิริยาที่ ไฮโดรเจน ในแอลเคนถูกแทนที่ด้วยอะตอมหรือกลุ่มอะตอมอื่นๆ ถ้าถูกแทนที่
ด้วยธาตุเฮโลเจน เช่น Cl2, Br2 จะเรียกว่าปฏิกิริยา ฮาโลจิเนชัน (halogenation) โดยถ้าใช้ Cl2 จะเรียกเป็นชื่อ
เฉพาะว่าปฏิกิริยา คลอริเนชัน (chlorination) และถ้าใช้ Br2 จะเรียกปฏิกิริยา โบรมิเนชัน (bromination)
สาหรับ F2 ไม่ใช้เพราะเกิดปฏิกิริยารุนแรง I2 ไม่ใช้เพราะเป็นของแข็งซึ่งไม่ไวต่อการเกิดปฏิกิริยาทั้งนี้ปฏิกิริยาที่
จะเกิดขึ้นได้ต้องมีแสงสว่างเป็นตัวช่วย
ในปฏิกิริยาฮาโลจิเนชันของแอลเคนจะได้ผลิตภัณฑ์เป็น อัลคิลเฮไลด์ (alkyl halide) และก๊าซ
ไฮโดรเจนเฮไลด์ เขียนเป็นสมการทั่วๆ ไปดังนี้
CnH2n +2 + X2 แสง CnH2n + 1X + HX
แอลเคน ฮาโลเจน อัลคิลเฮไลด์ ไฮโดรเจนเฮไลด์
ตัวอย่างเช่น
CH4 + Cl2 แสง CH3 - Cl + HCl
มีเทน เมทิลคลอไรด์ ไฮโดรเจนคลอไรด์
ในกรณีที่ใช้ก๊าซ Cl2 จานวนมากเกินพอจะเกิดปฏิกิริยาแทนที่ต่อเนื่องกันไปดังนี้
CH4 + Cl2 แสง CH3 - Cl + HCl
7
- 7. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
CH3 - Cl + Cl2 แสง CH2-Cl2 + HCl
เมทิลลีนคลอไรด์
CH2 -Cl2 + Cl2 แสง CHCl3 + HCl
คลอโรฟอร์ม
CHCl3 + Cl2 แสง CCl4 + HCl
คาร์บอนเตตระคลอไรด์
ดังนั้นเมื่อต้องการให้เกิดปฏิกิริยาแทนที่เพียงขั้นตอนเดียว จะใช้แอลเคนกับเฮโลเจนในปริมาณเท่าๆ
กัน หรือใช้เฮโลเจนน้อยกว่าเล็กน้อย
สาหรับก๊าซอื่นๆ ก็เกิดปฏิกิริยาในทานองเดียวกัน
เช่น ปฏิกิริยาระหว่างอีเทนกับ Br2
CH3CH3 + Br2 แสง CH3CH2Br + HBr
อย่างไรก็ตามถ้าแอลเคนมีคาร์บอนๆ เช่น CH4 และ CH2CH3 เมื่อเกิดปฏิกิริยาจะได้แอลคิลเฮไลด์
เพียงชนิดเดียว แต่ถ้ามีคาร์บอนตั้งแต่ 3 อะตอมขึ้นไป คือตั้งแต่โพรเพนเป็นต้นไป เมื่อเกิดปฏิกิริยาฮาโลจิเนชัน
(เฮโลจิเนชัน) จะได้ผลิตภัณฑ์เป็นแอลคิลเฮไลด์มากกว่า 1 ชนิด เช่น
CH3-CH2-CH3 2Cl,แสง
CH3 - CH - CH 3
CH3
Cl
CH3 - CH - CH 2 CH3 - C - CH 3+
Cl
32 % 68 %
Cl2
light
CH3 CH3
ปฏิกิริยาโบรมีเนชันจัดว่าเป็นปฏิกิริยาที่สาคัญของแอลเคน เนื่องจากใช้เป็นปฏิกิริยาทดสอบแอลเคนได้
เมื่อหยด Br2 หรือ Br2/CCl4 ลงในแอลเคน ถ้าทดลองในที่มืดจะไม่เกิดปฏิกิริยาแต่ถ้าทดลองในที่มีแสงสว่างจะมี
ปฏิกิริยาเกิดขึ้น สังเกตได้จากสีของ Br2 จะถูกฟอกจางหายไปพร้อมทั้งเกิดฟองก๊าซไฮโดรเจนไฮโดรเจนโบรไมด์
ขึ้น ซึ่งเมื่อใช้กระดาษลิตมัสสีน้าเงินชุบน้าไปอังเหนือหลอดทดลองกระดาษลิตมัสจะเปลี่ยนจากสีน้าเงินเป็นสี
แดง เพราะมีกรดเกิดขึ้น เช่น
C6H14 + Br2/CCl4 แสง C6H13Br + HBr
3.ปฏิกิริยาการแตกสลาย (cracking or pyrolysis)
เป็นปฏิกิริยาที่ทาให้แอลเคนโมเลกุลใหญ่ๆสลายตัวกลายเป็นโมเลกุลที่เล็กลงโดยการเผา
แอลเคนในภาชนะที่อุณหภูมิประมาณ 400-600 0
C พร้อมทั้งมีตัวเร่งปฏิกิริยา เช่น
CH3-CH2-CH2-CH3 C600-400 0
C4H8 + C3H6 + C2H6 + C2H4 + CH4 + H2
Al2O3-SiO2
52 %48 %
Cl
+ CH3 - CH - CH 2CH3 - CH2 - CH2
Cl
8
- 8. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
ยิ่งโมเลกุลมีขนาดใหญ่ผลิตภัณฑ์ที่เกิดจากการแตกสลายจะยิ่งมีมากมายหลายชนิด ขบวนการนี้ใช้ประ
โยนช์ทางด้านอุตสาหกรรมน้ามัน เพราะเป็นขบวนการเพิ่มเลขออกเทนของน้ามันทาให้คุณภาพของน้ามันดีขึ้น
รวมทั้งผลิตภัณฑ์ส่วนที่เป็นแอลคีนโมเลกุลเล็กๆ สามารถแยกออก นาไปใช้เป็นสารตั้งต้นในอุตสาหกรรม
พลาสติกได้
การเตรียมแอลเคน
1. เตรียมได้จากแหล่งกาเนิดในธรรมชาติ
แหล่งกาเนิดของแอลเคนในธรรมชาติได้แก่ ปิโตรเลียม และก๊าซธรรมชาติ ซึ่งขนาดของโมเลกุล
นั้นมีตั้งแต่คาร์บอน 1 อะตอม ถึง 40 อะตอม ในก๊าซธรรมชาติส่วนใหญ่จะเป็นแอลเคนที่กลายเป็นไอได้ง่าย
มวลโมเลกุลค่อนข้างต่า ประกอบด้วยมีเทน 70 – 90 อีเทน 13 – 15 นอกจากนั้นเป็นโพรเพน และบิวเทน
และบางส่วนของสารที่โมเลกุลขนาดใหญ่แต่กลายเป็นไอได้ง่ายปนอยู่ด้วย สาหรับปิโตรเลียมส่วนใหญ่
ประกอบด้วยไฮโดรคาร์บอนที่เป็นของเหลว และของแข็งปนกัน การแยกแอลเคนเหล่านี้ออกจากกันจะใช้การ
กลั่นลาดับส่วน
2. เตรียมจากการสังเคราะห์ โดยเตรียมในห้องปฏิบัติการ
2.1 เตรียมจากแอลคีน (catalytic reduction of alkene) โดยนาแอลคีนมาเติม H2 โดย
มีคะตะไลส์ เช่น Ni หรือ Pt เรียกปฏิกิริยานี้ว่า ไฮโดรจิเนชัน (hydrogeantion)
CH3 - CH = CH2 + H2 Pt
CH3 - CH2 - CH3
2.2 เตรียมจากปฏิกิริยาระหว่าง อัลคิลเฮไลด์ (alkyl halide) กับโลหะและกรด เช่น
CH3 - CH2 - Cl + Zn + H+
CH3 - CH3 + Zn2+
+ Cl-
2.3 เตรียมจากปฏิกิริยาระหว่างอัลคิลเฮไลด์ (alkyl halide) กับ Na ซึ่งเรียกว่า
Wurtz reaction เช่น
2CH3 - Cl + 2Na CH3 - CH3 + 2NaCl
2.4 การเตรียมมีเทนในห้องปฏิบัติการใช้ปฏิกิริยาระหว่างอลูมิเนียมคาร์ไบต์ (Al4C3) กับน้าอุ่น
หรือกรด HCl เจือจาง
Al4C3 + 12H2O 4Al(OH)3 + 3CH4
Al4C3 + 12HCl 4AlCl3 + 3CH4
ประโยชน์และโทษของแอลเคน
แอลเคนขนาดโมเลกุลเล็กๆ เช่น CH4 ซึ่งพบในก๊าซธรรมชาติ ใช้เป็นเชื้อเพลิงสาหรับเครื่องทาความร้อน
หม้อต้มน้าร้อน โพรเพน และบิวเทนใช้เป็นก๊าซหุงต้มตามบ้านเรือน ก๊าซปิโตรเลียมเหลว (แอลพีจี) เป็นก๊าซที่ได้
จากการกลั่นปิโตรเลียม แล้วบรรจุในถังเหล็กภายใต้ความดันสูงทาให้ได้เป็นของเหลวก็ใช้เป็นก๊าซหุงต้ม เช่น
เดียวกัน นอกจากนี้ ยังใช้แอลเคนเป็นสารตั้งต้นในอุตสาหกรรมหลายชนิด เช่นอุตสาหกรรมสารซักฟอก เส้นใย
สารเคมีทางการเกษตรและยาปราบศัตรูพืช แอลเคนชนิดเหลวใช้เป็นตัวทาละลาย พวกโมเลกุลขนาดใหญ่ใช้ทา
น้ามันหล่อลื่น
9
- 9. เอกสารประกอบการสอน เรื่อง สารประกอบอินทรีย์
นอกจากจะมีประโยชน์แล้ว แอลเคนก็มีโทษเช่นเดียวกัน เนื่องจากสามารถละลายสารอินทรีย์ไม่มีขั้ว
เช่น ไขมันและน้ามันได้ เมื่อสูดดมไอของแอลเคนเข้าไปจะทาให้เป็นอันตรายกับเนื้อเยื่อปอด เพราะไปละลาย
ไขมันในผนังเซลล์ที่ปอด นอกจากนี้แอลเคนบางชนิดที่ใช้เป็นตัวทาละลาย เช่น เอกเซน ทาให้ผิวหนังแห้งเจ็บ
คันและแตก เพราะไปละลายน้ามันที่ผิวหนัง ทาให้ผิวหนังขาดความชุ่มชื้นจึงแห้งและแตก