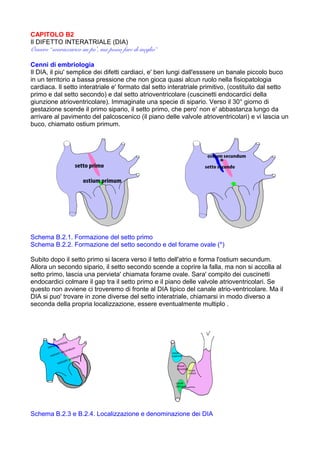
Il difetto interatriale (DIA) è un'anomalia cardiaca congenita che deriva da discontinuità nel setto interatriale, comportando variazioni nel flusso sanguigno tra gli atri e potenziali sovraccarichi cardiaci. La diagnosi avviene spesso incidentalmente in bambini asintomatici, mentre il trattamento può includere approcci percutanei o chirurgici, a seconda delle caratteristiche e della dimensione del difetto. Dopo la chiusura, i pazienti generalmente possono condurre una vita normale, ma richiedono monitoraggio per eventuali complicazioni e seguono un protocollo di follow-up regolare.