Recommended
PPT
PDF
PDF
PPT
PDF
PDF
PPT
PDF
Isomers [compatibility mode]
PDF
แก๊ส ของแข็ง ของเหลวและสารละลาย - Gas Solid Liquid and Solution
PDF
PDF
PPTX
Carboxylic acid analysis, synthesis and other
PPS
PDF
PDF
จลนศาสตร์เคมี (Kinetics Chemistry)
PPTX
PPT
PDF
PDF
PPTX
PPT
Group theory and symmetry
PDF
การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี
PPTX
บทที่ 8 ความร้อนและอุณหพลศาสตร์
PPTX
PDF
PDF
MuleSoft Surat Meetup#40 - Watermarking Concept and Fragments in MuleSoft
PDF
Phase transfer catalyst and ultrasound in organic recation .pdf
PPTX
Stereochemistry by Dr. P. R. Padole
PDF
PDF
More Related Content
PPT
PDF
PDF
PPT
PDF
PDF
PPT
PDF
Isomers [compatibility mode]
What's hot
PDF
แก๊ส ของแข็ง ของเหลวและสารละลาย - Gas Solid Liquid and Solution
PDF
PDF
PPTX
Carboxylic acid analysis, synthesis and other
PPS
PDF
PDF
จลนศาสตร์เคมี (Kinetics Chemistry)
PPTX
PPT
PDF
PDF
PPTX
PPT
Group theory and symmetry
PDF
การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี
PPTX
บทที่ 8 ความร้อนและอุณหพลศาสตร์
PPTX
PDF
PDF
MuleSoft Surat Meetup#40 - Watermarking Concept and Fragments in MuleSoft
PDF
Phase transfer catalyst and ultrasound in organic recation .pdf
PPTX
Stereochemistry by Dr. P. R. Padole
Viewers also liked
PDF
PDF
DOC
PDF
สารประกอบไฮโดรคาร์บอนเคน คีน ไคน์
PDF
PDF
PDF
เคมีอินทรีย์ Organic-chemistry
PPT
Similar to 256121 ch2 hc 1-alkane & cycloalkane
PDF
ปฏิกิริยาเคมีอินทรีย์ (Organic Reactions)
PDF
PPT
PDF
PDF
Alkylhalides-Alcoholsิึิึ้ึ้ึ้ึ้ึ้ึิ้้ึ้ึ้ึ้-Ni.pdf
PDF
PDF
PDF
PDF
7-ปฏิกิริยาของสารประกอบอินทรีย์-ครู-สำหรับ .pdf
PPTX
PDF
PDF
PPT
PDF
PDF
วิทยาศาสตร์ (ฟิสิกส์,เคมี,ชีวะ)
PDF
ติวมาม่า16th วิทยาศาสตร์ O-NET (ครูติ่ง)
PDF
PDF
PDF
Reaction organic สำหรับห้องหนึ่ง
PDF
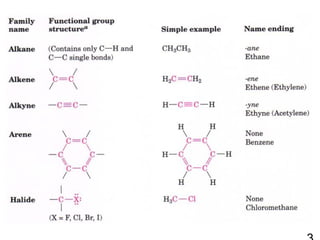
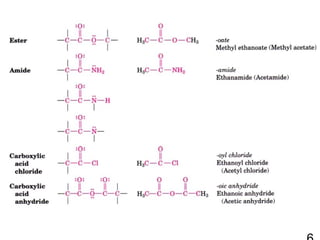
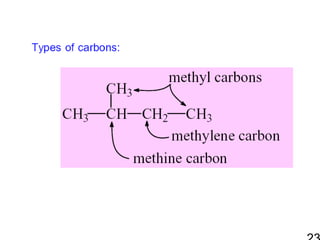
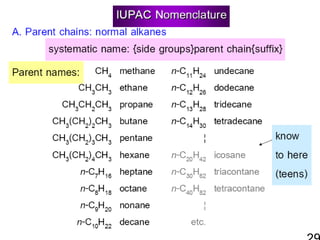
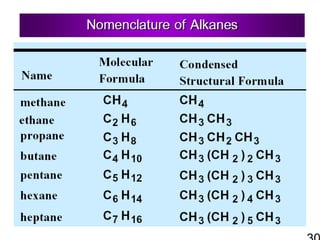
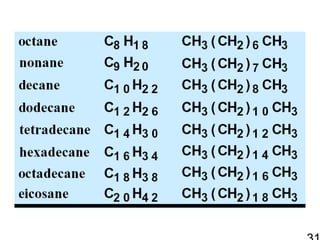
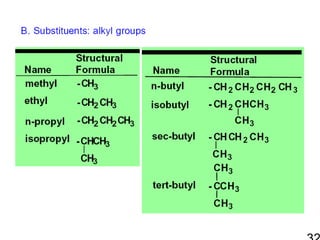
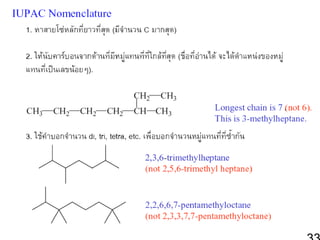
256121 ch2 hc 1-alkane & cycloalkane 1. 2. Functional Group
สามารถจัด แบ่ง หมวดหมู่ข อง
สารประกอบอิน ทรีย ์ต ามโครงสร้า ง
(Structure) ซึ่ง สัม พัน ธ์ก ับ ความว่อ งไวใน
ional Group (หมุฟ ัง ก์ช น , หมู(reactivity)
่
การเกิด ปฏิก ิร ิย ั าเคมี ่ท ำา หน้า ที่)
กลุ่มของอะตอมภายในโมเลกุลซึ่งมีลักษณะเฉพาะที่
แสดงถึงสมบัติทางเคมี
โดยหลักการแล้วโมเลกุลทีมหมูฟงก์ชันประเภทเดียวกัน
่ ี ่ ั
จะสามารถเกิดปฏิกิริยาเคมี
ในลักษณะเดียวกันโดยไม่ข ึ้น กับ ขนาดหรือ ความซับ
ซ้อ นของโมเลกุล
ทังนีไม่ได้หมายรวมถึงความว่องไวในการเกิดปฏิกิริยา
้ ้
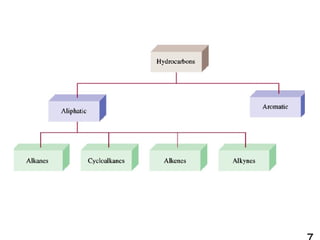
8. สารประกอบไฮโดรคาร์บ อน
Hydrocarbon :
สารประกอบที่ม ี C และ H เป็น
องค์ป ระกอบ ั
อาจจำา แนกได้ด ง นี้
• สารประกอบไฮโดรคาร์บ อนอิ่ม ตัว
(Saturated hydrocarbon) :
สารประกอบไฮโดรคาร์บ อนที่ม พ ัน ธะ
ี
เดี่ย วทั้ง หมด
• สารประกอบไฮโดรคาร์บ อนไม่อ ิ่ม ตัว
(Unsaturated hydrocarbon) :
9. • อัล ลิฟ าติก ไฮโดรคาร์บ อน
(Aliphatic hydrocarbon) :
สารประกอบไฮโดรคาร์บ อนที่
อาจเป็น สายโซ่ เป็น วงอิ่ม
หรือ ไม่อ ิ่ม ตัว แต่ไ ม่ม ีส มบัต ิอ ะโร
มาติก
• อัล เคน (Alkane) : สารประกอบ
• อะโรมาติก ไฮโดรคาร์บ อน
ไฮโดรคาร์บ อนอิ่ม ตัว
(Aromatic hydrocarbon) :
• อัล คีน (Alkene) : สารประกอบ ี
สารประกอบไฮโดรคาร์บ อนที่ม
ไฮโดรคาร์บ อนที่ม ีพ ัน ธะคู่
สมบัต ิอ ะโรมาติก
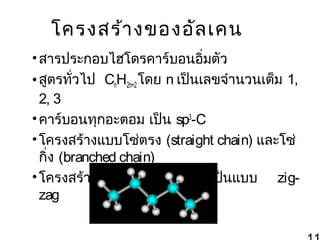
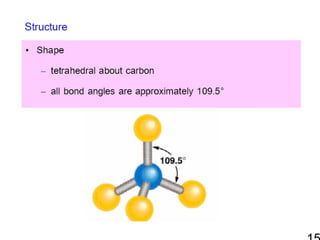
10. 11. โครงสร้า งของอัล เคน
• สารประกอบไฮโดรคาร์บอนอิ่มตัว
• สูตรทั่วไป CnH2n+2 โดย n เป็นเลขจำานวนเต็ม 1,
2, 3
• คาร์บอนทุกอะตอม เป็น sp3-C
• โครงสร้างแบบโซ่ตรง (straight chain) และโซ่
กิ่ง (branched chain)
• โครงสร้างของสายโซ่คาร์บอนเป็นแบบ zigzag
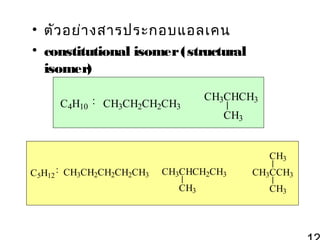
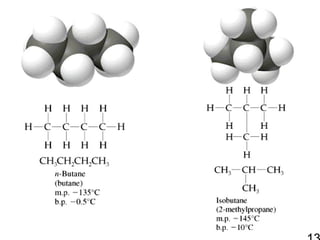
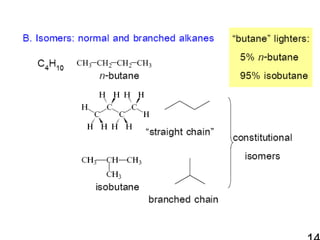
12. • ตัว อย่า งสารประกอบแอลเคน
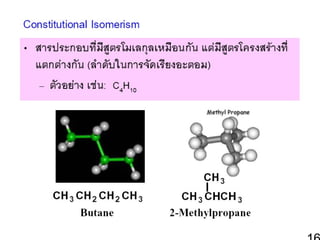
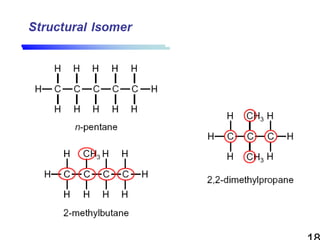
• constitutional isomer (structural
isomer)
C4H10
: CH3CH2CH2CH3
CH3CHCH3
CH3
CH3
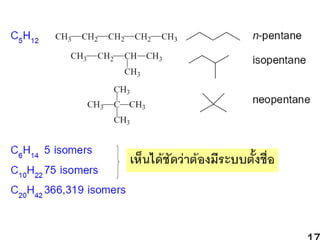
C5H12 : CH3CH2CH2CH2CH3
CH3CHCH2CH3
CH3
CH3CCH3
CH3
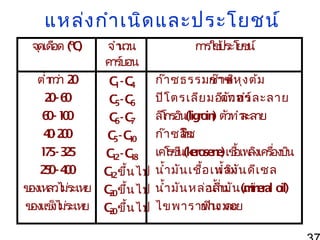
19. 24. 26. 37. แหล่ง กำำ เนิด และประโยชน์
จุ อด (oC
ดเดื
)
จำำ
นวน
คำร์
บอน
ตำ่ำ ำ 2
กว่ 0
C -C
1 4
2 -6
0 0
C -C
5 6
6 -10
0 0
C -C
6 7
4-20
0 0
C - C0
5 1
1 5- 3 5
7 2
C2- C8
1
1
2 0- 4 0
5 0
C2ขึ้น ไป
1
ของเหลวไ
ม่ระเหย C0ขึ้น ไป
2
ข งไ
องแข็ ม่ระเหย C0ขึ้น ไป
2
กำรใ ประโ น์
ช้ ยช
ก๊ำ ซธรรมชำติ ง ต้ม
ก๊ำ ซหุ
ปิโ ตรเลีย มอีตัทอร์ ละลำย
เ ว ทำำ
ลิ กรอิน(lig in ตั ำ
โ
ro ) วทำ ละลำย
ก๊ำ ซโซ
ลี
น
เคโ ซี (k ro e e เชื้ งเครื่ น
ร น e s n ) อเพลิ องบิ
นำ้ำ มัน เชื้อ เพลิมัน ดีเ ซล
นำ้ำ ง
นำ้ำ มัน หล่อ ลื่น น (m ea o
นำ้ำ มั แร่ r l il)
in
ไขพำรำฟิน ตอย
ยำงมะ
38. สมบัต ิท ำงกำยภำพ
• สถำนะ ที่อุณหภูมิห้อง และควำมดัน
1 บรรยำกำศ
– อัลเคนโซ่ตรงที่มีคำร์บอน 1-4 อะตอม
ก๊ำ ซ
– อัลเคนที่มีคำร์บอน 5-17 อะตอม
ของเหลว
– อัลเคนที่มีคำร์บอนมำกกว่ำ 18 อะตอม
ของแข็ง
• ควำมหนำแน่น
39. • จุด เดือ ด
– เพิ่มขึ้นตามจำานวนคาร์บอน
• เพราะโมเลกุลขนาดใหญ่จะมีแรงยึดเหนียว
่
ระหว่างโมเลกุลมากกว่าโมเลกุลขนาดเล็ก
– อัลเคนโซ่กิ่งมีจุดเดือดตำ่ากว่าอัลเคนโซ่
ตรงที่มีคาร์บอนเท่ากัน
• โมเลกุลของอัลเคนโซ่กิ่งจะมีขนาดโมเลกุล
กระทัดรัดกว่าโซ่ตรง ทำาให้พื้นทีผิวสัมผัส
่
ระหว่างโมเลกุลน้อยลง แรง van de Waals
ซึงเป็นแรงระหว่างโมเลกุลจึงน้อยลงด้วย
่
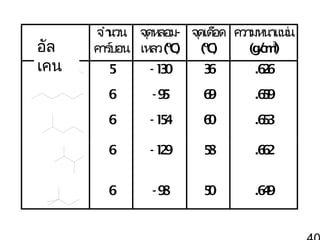
40. อัล
แอลเคน
เคน
จำา
นวน จุ
ดหลอม- จุ อด ความหนาแน่
ดเดื
น
คาร์
บอน เหลว (oC
)
(oC
)
(gcm)
/ 3
5
-10
3
3
6
.6 6
2
6
-9
5
6
9
.6 9
5
6
-14
5
6
0
.6 3
5
6
-19
2
5
8
.6 2
6
6
-9
8
5
0
.6 9
4
41. • จุด หลอมเหลว
– มีแนวโน้มเพิ่มขึ้นตามจำานวนอะตอม
คาร์บอน
• การละลาย
– อัลเคนเป็นสารประกอบไม่มขั้วจึงไม่
ี
ละลายนำ้า
– ละลายในตัวทำาละลายไม่มีขั้วเช่น
ether, benzene
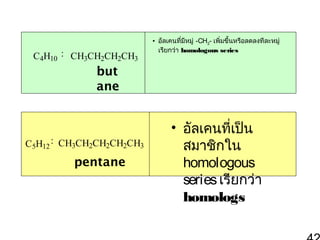
42. C4H10 : CH3CH2CH2CH3
but
ane
C5H12 : CH3CH2CH2CH2CH3
pentane
• อัลเคนที่มีหมู่ -CH2- เพิ่มขึ้นหรือลดลงทีละหมู่
เรียกว่า homologous series
CH3CHCH3
CH3
• อัลเคนที่เป็น CH3
CH3CHCH2CH3 ใน CH3CCH3
สมาชิก
CH3
homologous CH3
series เรียกว่า
homologs
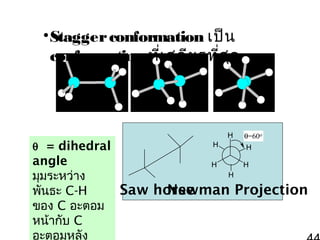
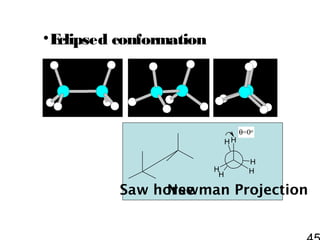
43. 44. • Stagger conformation เป็น
conformation ทีเ สถีย รที่ส ุด
่
θ = dihedral
angle
มุมระหว่าง
พันธะ C-H
ของ C อะตอม
หน้ากับ C
อะตอมหลัง
H
H
θ=60o
H
H
H
H
Saw horse
Newman Projection
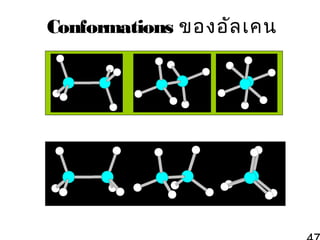
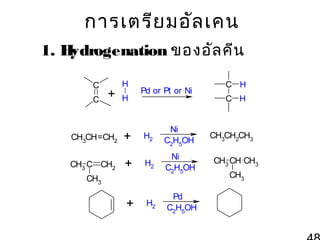
45. 46. 47. 48. การเตรีย มอัล เคน
1. H
ydrogenation ของอัล คีน
C
C
+
CH3CH=CH2
CH3 C CH2
H
H
Pd or Pt or Ni
H2
Ni
C2H5OH
+
H2
Ni
C2H5OH
+
H2
+
CH3
Pd
C2H5OH
C H
C H
CH3CH2CH3
CH3 CH CH3
CH3
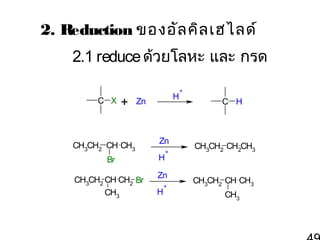
49. 2. Reduction ของอัล คิล เฮไลด์
2.1 reduce ด้วยโลหะ และ กรด
C X
+
H
Zn
CH3CH2 CH CH3
Br
CH3CH2 CH CH2 Br
CH3
Zn
H
+
Zn
H
+
+
C H
CH3CH2 CH2CH3
CH3CH2 CH CH3
CH3
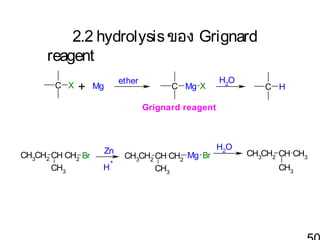
50. 2.2 hydrolysis ของ Grignard
reagent
C X
+
ether
Mg
C Mg X
H2O
C H
Grignard reagent
CH3CH2 CH CH2 Br
CH3
Zn
H
+
CH3CH2 CH CH2 Mg Br
CH3
H2O
CH3CH2 CH CH3
CH3
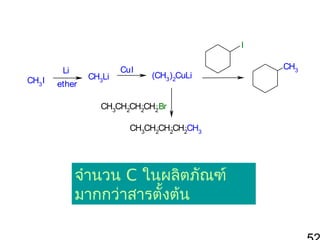
51. 3. Corey-H
ouse synthesis ใช้
lithium dialkylcuprate
R'
X
ควร มูแอลคิลช ดm y 1 หรือoเท่านั้น
มีห ่
นิ eth l, o 2
RX
มีห แอลคิลเป็น นิ ดก็ ด้
มู่
ช ดใ ไ
52. 53. 4. ปฏิก ิร ิย า W
urtz
CH3CH2 Br
CH3
CH3CH2 CH Br
Na
Na
CH3CH2 CH2CH3
CH3 CH3
CH3CH2 CH CH CH2CH3
จำานวน C ในผลิตภัณฑ์เป็น 2
เท่าของสารตั้งต้น
54. ปฏิก ิร ิย าของอัล เคน
1. H
alogenation
C H
+
X2
CH3CH3
+
Cl2
CH3 CH2CH3
+
Cl2
แสงหรือค มร้อน
วา
แสง
hν
CH3CH2 Cl
C X
+
CH3 CH2CH2 Cl
45%
+
H X
H Cl
+
CH3 CH CH3
Cl
55%
ถ้าอัลเคนมี H มากกว่า 1 ชนิดจะได้
ผลิตภัณฑ์มากกว่า 1 ชนิดด้วย
+
H Cl
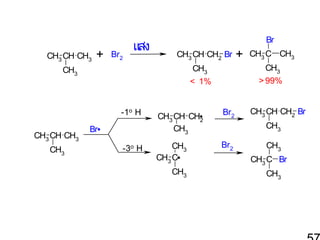
55. 56. 57. CH3 CH CH3
+
Br2
แสง
Br
CH3 CH CH2 Br
< 1%
-1o H
CH3 CH CH3
CH3
Br
-3o H
CH3 CH CH2
CH3
Br2
CH3
CH3 C
Br2
CH3
CH3 C CH3
CH3
> 99%
CH3
CH3
+
CH3 CH CH2 Br
CH3
CH3
CH3 C Br
CH3
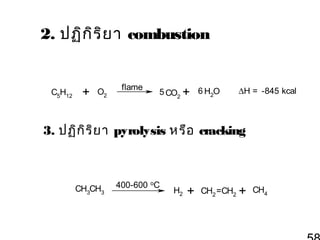
58. 2. ปฏิก ิร ิย า combustion
C5H12
+
O2
flame
5 CO2 + 6 H2O
∆H = -845 kcal
3. ปฏิก ิร ิย า pyrolysis หรือ cracking
CH3CH3
400-600 oC
H2
+
CH2 =CH2 + CH4
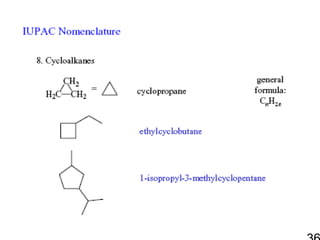
59. โครงสร้า งของไซโคลอัล เคน
• สารประกอบไฮโดรคาร์บอนอิ่มตัวซึ่งมี
โครงสร้างเป็นวง
• สูตรทั่วไป CnH2n โดย n เป็นเลขจำานวน
เต็ม 1, 2, 3
• คาร์บอนทุกอะตอม เป็น sp3-C
CH2
H2C CH2
60. สมบัต ิท างกายภาพ
• คล้ายกับอัลเคน
•
ไซโคลแอลเคนที่มีจำานวนอะตอม
คาร์บอนเท่ากับอัลเคน
จะมีจุดเดือดและความหนาแน่นสูง
กว่า
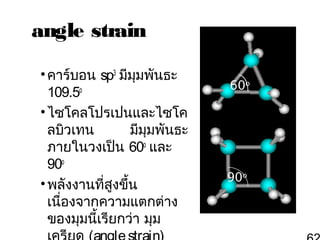
61. 62. angle strain
• คาร์บอน sp3 มีมุมพันธะ
109.5o
• ไซโคลโปรเปนและไซโค
ลบิวเทน
มีมุมพันธะ
ภายในวงเป็น 60o และ
90o
• พลังงานที่สงขึ้น
ู
เนื่องจากความแตกต่าง
ของมุมนี้เรียกว่า มุม
60o
90o
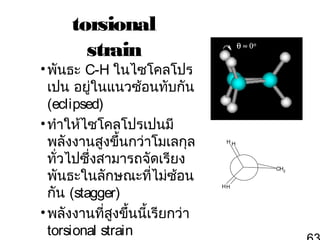
63. torsional
strain
• พันธะ C-H ในไซโคลโปร
เปน อยู่ในแนวซ้อนทับกัน
(eclipsed)
• ทำาให้ไซโคลโปรเปนมี
พลังงานสูงขึ้นกว่าโมเลกุล
ทั่วไปซึ่งสามารถจัดเรียง
พันธะในลักษณะที่ไม่ซ้อน
กัน (stagger)
• พลังงานที่สงขึ้นนี้เรียกว่า
ู
torsional strain
HH
CH2
HH
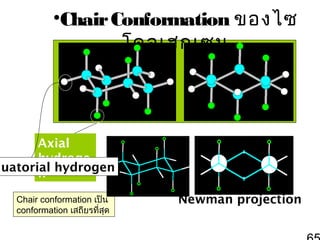
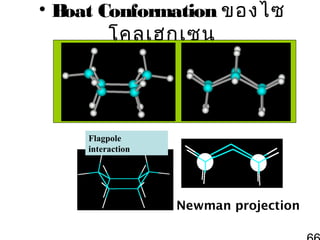
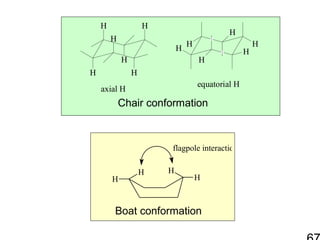
64. 65. 66. 67. 68. Chair conformation เสถียรทีสุดเพราะ
่
• มุมพันธะระหว่างคาร์บอนเป็น 109.5o
• ทุกพันธะอยู่ในตำาแหน่ง stagger
Boat conformation มีพลังงานสูงเพราะ
• มีพันธะอยู่ในลักษณะซ้อนกันแบบ eclipsed ทำาให้
มี torsional strain สูง
• อะตอมไฮโดรเจนบนคาร์บอนอะตอมที่ 1 และ 4
เกิดแรงผลัก van de Waals ซึ่งเรียกว่า flagpole
interaction
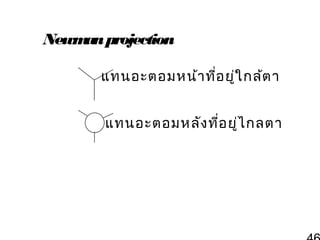
69. ไอโซเมอร์เ ชิง เรขาคณิต
(geometric isomer)
• พันธะในไซโคลอัลเคนเป็นพันธะที่ไม่
สามารถหมุน
ได้อย่างอิสระ
• ถ้ามีหมูแทนที่ในวง 2 หมู่ จะมีไอโซเมอร์
่
เชิงเรขาคณิตได้คอ
ื
– cis- หมู่แทนที่ทั้ง 2 หมู่ชี้ไปด้านเดียวกัน
ของระนาบวง
– trans- หมู่แทนที่ทั้ง 2 หมู่ชไปคนละด้าน
ี้
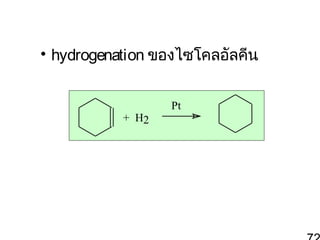
70. 71. การเตรีย มไซโคลอัล เคน
• วิธที่ดัดแปลงจากปฏิกิริยา Wurtz
ี
reaction
BrCH2CH2CH2Br +
Zn
+ ZnBr2
BrCH2CH2CH2CH2Br +
Zn
+
ZnBr2
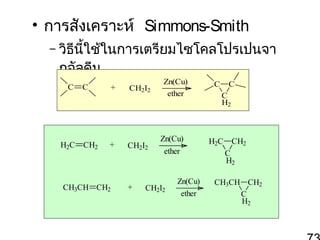
72. 73. • การสังเคราะห์ Simmons-Smith
– วิธีนี้ใช้ในการเตรียมไซโคลโปรเปนจา
กอัลคีน
C
H2C
C
+
CH2
+
CH3CH CH2
CH2I2
CH2I2
+
Zn(Cu)
ether
Zn(Cu)
ether
CH2I2
Zn(Cu)
ether
C
C
C
H2
H2C
CH2
C
H2
CH3CH CH2
C
H2
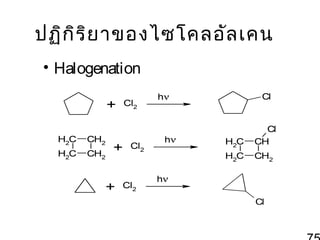
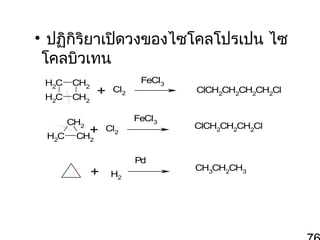
74. ปฏิก ิร ิย าของไซโคลอัล เคน
• ไซโคลอัล เคน วงขนาดใหญ่ท ำา
ปฏิก ิร ิย าเหมือ นอัล เคน
• ไซโคลโปรเปน ไซโคลบิว เทนทำา
ปฏิก ิร ิย าแตกต่า งจากอัล เคน เพราะไม่
เสถีย ร มีค วามเครีย ดวงสูง
75. 76. Editor's Notes #40 <number>
#42 <number>