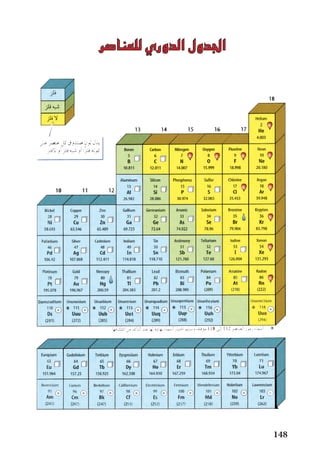
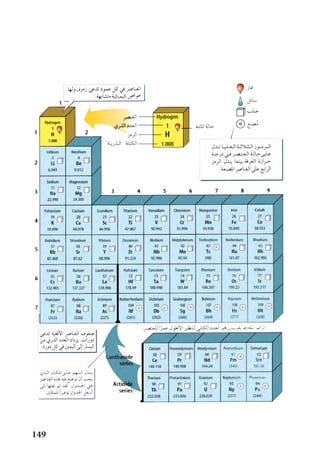
يتناول هذا الوثيقة منهج مادة الكيمياء للصف الثالث المتوسط، حيث يركز على توجيه الطلاب لاختيار تخصصاتهم الدراسية وكيفية تأهيلهم علمياً ونفسياً من خلال محتوى تعليمي متنوع. كما يتضمن دعوة للمدرسين وأولياء الأمور للمشاركة في تطوير الكتاب وتقديم آرائهم لتحسين التجربة التعليمية. تعتمد المضامين التعليمية على إطلاع الطلاب على أحدث التطورات العلمية ورفع مستوى استيعابهم للمفاهيم الكيميائية.













![14
مقدمة 1 - 1
الكيمياءلعلملدراستكالسابقةالسنينفيتعلمتانسبق
صغيرةجسيماتمنتتكونالكونفيالموجودةالموادجميعأن
بالذرات سميت المواد هذه لبناء االساسية الوحدات تشكل
،لالنقسام القابلة غير الالتينية اللغة في تعني والتي )Atoms(
بعدة الماضيين القرنين خالل الذري البناء تفسير مر ولقد
آخر الى الوصول كيفية الفصل هذا في وسندرس نظريات
.الذري البناء لمعرفة الحديثة النظريات
الذري البناء مفهوم تطور 2 - 1
نموذج وكل الذرة لتركيب مختلفة نماذج العلماء اقترح
اخذ والتجارب المالحظات نتيجة ثم ،وقته في االفضل كان
.العلمية الناحية من ًالقبو لالكثر ًالوصو يتطور النموذج
.الزمني تسلسلها حسب النماذج هذه الى وسنتعرف
دالتون منوذج 1 - 2 - 1
الذرة دالتون العالم تصور عشر التاسع القرن بداية في
الشكل[ لالنقسام قابلة غير صلبة دقيقة كرة هيئة على
وان به الخاصة الذرات من معين نوع عنصر لكل ،])1 - 1(
.المركبة الذرات لتكوين بسيطة بطرائق ترتبط الذرات هذه
ثوم�سون منوذج 2 - 2 - 1
ًاتصور ثومسون العالم قدم عشر التاسع القرن نهاية في
أصغر جسيمات من تتكون الذرة ان اكتشافه (بعد ،للذرة آخر
كرة بأنها ،)االلكترونات أسم عليها أطلق سالبة شحنات تحمل
الشحنة السالبة االلكترونات عليها تلتصق الشحنة موجبة
متعادلــة فانهــا لذا للكرة الموجبة الشحنة تعادل التي
.للذرة ثومسون نموذج يبين )2 - 1( والشكــل .الشحنــة
تعلم هل
ليســـت فكرة هـــو الرأي
فأنها النظرية اما مؤكدة
لشـــرح اسباب تستخدم
وبيـــانات مــــالحـــــظات
.مختبرية
الشحنة سالبة الكترونات
موجبة كرة
الشحنة
صلبة كرة
رقيق سطح ذات
)1 - 1( الشكل
.للذرة دالتون نموذج
)2 - 1( الشكل
.للذرة ثومسون نموذج](https://image.slidesharecdn.com/random-161027114933/85/slide-14-320.jpg)
![15
رذرفورد منوذج 3 - 2 - 1
البروتون اكتشاف وبعد العشرين القرن اوائل في
كتلة من بكثير اكبر كتلته الشحنة موجب جسيم هو والذي
البروتونات بأن تصوره رذرفورد العالم قدم .االلكترونات
النواة اسم عليه اطلق الذرة وسط في صغير حجم في متمركزة
تدور االلكترونات وان الذرة كتلة معظم على تحتوي وانها
االلكترونات عدد وان فراغ الذرة حجم اغلب فان لذا حولها
الموجبة الشحنات تعادل النواة حول تدور التي السالبة
وفي كبيرة بسرعة تدور االلكترونات وهذه للبروتونات
حول الكواكب تدور كما النواة عن البعد مختلفة مدارات
في كما الكوكبي بالنموذج النموذج هذا سمي لذا الشمس
.)3 - 1( الشكل
احلديث االلكرتوين البناء اىل مدخل 3 - 1
فلو .الكوكبي رذرفورد لنموذج بالنسبة مشكلة نشأت
فأنها )االول (االفتراض ساكنة السالبة االلكترونات ان فرضنا
ان يجب لذا بالشحنة لها المخالفة النواة الى تنجذب سوف
الشحنات ان وبما )الثاني (االفتراض حركة حالة في تكون
اذن طاقة تطلق جذب قوة تأثير تحت المتحركة الكهربائية
المتحرك االلكترون طاقة في فقدان لذلك نتيجة ينتج سوف
غير يكون وبالتالي ًالولبي يلف يجعله مما حركته فتبطأ
ففي لذا ،النواة في ويسقط النواة جذب مقاومة على قادر
الذرات ان وبما ،تنهار سوف الذرة ان نجد الفرضيتين كلتا
المناقشة حسب خطأ هناك يكون ان بد ال لذلك تنهار ال
.اعاله المذكورة
بور منوذج 1 - 3 - 1
ان 1913 عام دنماركي عالم وهو بور العالم اقترح
طاقة ذات مستويات في النواة حول تدور االلكترونات
طاقة مستوى ولكل ،])4 - 1( الشكل[ محددة اقطار وانصاف
.الرئيســـي الكــــم بعــــدد يسمـــى طاقته ويصف يميزه رقم
الرئيسي الكم عدد يكون االول الطاقة مستوى في فااللكترون
تعلم هل
ذرة حجم ان فرضنا اذا
لكرة ملعب بحجم ما
هذه نواة فأن القدم
سوف المفترضة الذرة
زجاجية كرة بحجم تكون
يلعب كالتي جدا صغيرة
.االطفال بها
)3 - 1( الشكل
.للذرة رذرفورد نموذج
)4 - 1( الشكل
.للذرة بور نموذج
الكترون النواة
الطاقة مستوى
النواة
االلكترونات حركة مدار
الكترونات](https://image.slidesharecdn.com/random-161027114933/85/slide-15-320.jpg)


![18
مما بالنواة ًاارتباط واقلها طاقة اكثرها النواة عن ابعدها
. )6 - 1( الشكل الحظ .فقدانه يسهل
......... 7 = n
......... 6 = n
......... 5 = n
......... 4 = n
......... 3 = n
......... 2 = n
......... 1 = n
الثانوية الطاقة م�ستويات 2 - 4 - 1
)... و N و M و L و K ( الرئيسية الطاقة مستويات تحتوي
d و p و s بالحروف لها يرمز ثانوية طاقة مستويات على
الشكل ناحية من ًاخصوص المستويات هذه وتختلف f و
)s( اوربيتال ان حيث تحتويها التي االلكترونات وعدد
)p( الثانوي المستوى اما .])7 - 1( الشكل[ كروي شكل له
فصين من مكون اوربيتال وكل اوربيتاالت ثالث فله
متعامدة اتجاهات بثالث الفراغ في موزعة متكافئين
.)8 - 1( الشكل في موضحة وكما ،) Pz
و Py
و Px
( لها يرمز
اكثر فراغية اشكال فلهما ) d و f ( الثانويين المستويين اما
.ًاتعقيد
الطاقة
الطاقةفيزيادة
)6 - 1( الشكل
طاقة زادت n قيم زادت كلما
.المستوى
)8 - 1( الشكل
.)p( االوربيتاالت اشـــكال
)7 - 1( الشكل
لالوربيتال الكروي الشـــكل
.)s(
x
Px
Py Pz
xx
yyy
zzz
x
y
z](https://image.slidesharecdn.com/random-161027114933/85/slide-18-320.jpg)

![20
الثانوية امل�ستويات يف وااللكرتونات االوربيتاالت عدد 3-4-1
االوربيتاالتمنمجموعةعلىالثانويةالمستوياتتحتوي
موضح كما بالمربع لها الرمز يمكن التي المختلفة
:ادناه
واحد اوربيتال يوجد s الثانوي المستوى في
اوربيتاالت ثالث يوجد p الثانوي المستوى في
اوربيتاالت خمس يوجد d الثانوي المستوى في
اوربيتاالت سبعة يوجد f الثانوي المستوى في
اقصى كحد فقط اللكترونين الواحد االوربيتال يتسع
الكترون االحيان بعض في االوربيتال يحتوي قد ولكن
المستويات فان االساس هذا وعلى ًافارغ يكون او واحد
من االقصى الحد على تحتوي (اي .كاالتي تتشبع الثانوية
.)االلكترونات
الكترون 2 اقصى كحد يتشبع s الثانوي المستوى
الكترون 6 اقصى كحد يتشبع p الثانوي المستوى
الكترون 10 اقصى كحد يتشبع d الثانوي المستوى
الكترون 14 اقصى كحد يتشبع f الثانوي المستوى
وجودهما حال في االلكترونان يتنافر ان المفترض من ان
،السالبة الشحنة نفس يحمالن النهما واحد اوربيتال في
عند بعضها مع االلكترونات تتنافر ال لماذا فكرت فهل
كل ان هذا تساؤلك عن لالجابة االوربيتال؟ نفس في وجودها
فيه يدور الذي الوقت نفس في محوره حول يبرم الكترون
في الكترونين ازدواج فعند ،]أ )10 - 1( [الشكل النواة حول
محوره حول يبرم سوف احدهما فان واحد اوربيتال
االخر اما الرمز له ويعطى الساعة عقرب دوران باتجاه
الرمــز له ويعطى الساعة عقرب دوران عكس برمه فيكون
تنافرهما يلغي مما االخر عكس يبرم سوف احدهما ان اي
.،]ب )10 - 1( [الشكل
)3 - 1( تمرين
االوربيتاالت عدد ما - أ
الطاقة مستوى من كل في
والثالث؟ االول الرئيسي
االلكترونات عدد ما - ب
الطاقة مستوى من كل في
والثالث؟ الثاني الرئيسي
)10 - 1( الشكل
حول االلكترون دوران - أ
.النواة
حول الكترونين دوران - ب
االوربيتال في محوريهما
.الواحد
) أ (
)(ب](https://image.slidesharecdn.com/random-161027114933/85/slide-20-320.jpg)





![27
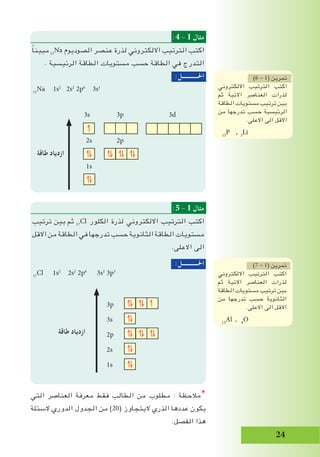
: 8 - 1 مثال
1s2
2s2
2p4
:كاالتي االلكترونات فيها مرتبة عنصر ذرة
الذرة؟ هذه في االلكترونات عدد ما - 1
للعنصر؟ الذري العدد ما - 2
المملوءة الثانوية الطاقة مستويات عدد ما - 3
بااللكترونات؟
المزدوجة؟ غير االلكترونات عدد ما - 4
الذرة؟ لهذه لويس رمز اكتب - 5
:احلـــــــــــل
. 8 يساوي فيها االلكترونات عدد - 1
عدد يساوي ألنه 8 يساوي للعنصر الذري العدد - 2
.االلكترونات
1s 2s 2p - 3
مملوءة 2s الثانوي المستوى وكذلك 1s الثانوي المستوى
عدد يكون لذلك مملوء غير 2p المستوى اما بااللكترونات
.فقط اثنان بااللكترونات المملوءة الثانوية المستويات
2p - 4
.فقط اثنان المزدوجة غير االلكترونات عدد نالحظ
:للعنصر لويس رمز - 5
الدوري اجلدول 7 - 1
)10 - 1( تمرين
: 6 الذري عدده عنصر
االلكتروني الترتيب اكتب - 1
.له
مستـــــويـات عـــدد مـــــــا - 2
المملـــوءة الثانويـــة الطاقة
.بااللكترونات
غير االلكترونات عدد ما - 3
.فيه المزدوجة
لهذه لويس رمز اكتب - 4
.الذرة
9
VIIIB
7
VIIB
6
VIB
5
VB
4
IVB
3
IIIB
2
IIA
1
IA
11
IB
12
IIB
13
IIIA
14
IVA
8 10
15
VA
16
VIA
17
VIIA
18
VIIIA
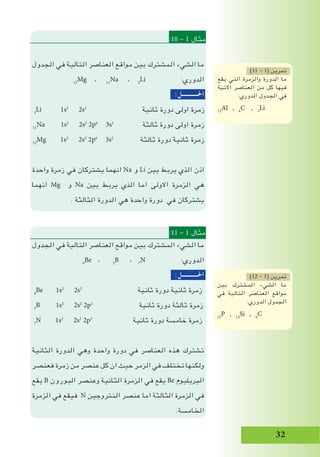
)14 - 1( الشكل
الدوري الجدول من جزء
.عناصر بدون
العنصر
لدارسي اداة أهم الدوري الجدول يعتبر
المتعددة فوائده بين ومن الكيمياء علم
علمت اذا ًالفمث العناصر خواص وفهم توقع
لعنصر والكيميائية الفيزيائية الخواص
حد الى التوقع يمكنك دورة او زمرة في
في تقع التي العناصر خواص وصحيح كبير
.])14 - 1( الشكل [ ،دورته او زمرته](https://image.slidesharecdn.com/random-161027114933/85/slide-27-320.jpg)






![35
فكلما االسفل الى االعلى من الزمر في التأين طاقات تتدرج
بسبب العنصر لهذا التأين طاقة قلت كلما الذري العدد زاد
فقدان يسهل مما النواة عن الخارجية االغلفة الكترونات ابتعاد
كلما للعناصر تزداد التأين طاقات فان الدورات في اما احدهما
ضمن الموجبة الشحنة زيادة بسبب للعنصر الذري العدد زاد
الرئيسي الطاقة مستوى نفس في االلكترونات وبقاء النواة
قبل من االلكترون على الجذب قوة بذلك فتزداد الخارجي
استثناء وهناك ،])20 - 1( الشكل[ للنواة الموجبة الشحنات
ns2
مثل مشبع ثانوي غالف للذرة كان اذا انه وهو الزيادة لهذه
طاقة من اكبر تأينها طاقة فتكون np3
مثل مشبع نصف أو
على 8
O من تأين طاقة أكبر 7
N مثل بعدها التي الذرة تأين
النتروجين ذرة من ذري عدد اكبر االوكسجين ذرة ان من الرغم
طاقة اعلى النبيلة العناصر تمتلك .واحدة دورة في ويقعان
.بسهولة الكتروناتها تفقد ال ألنها تأين
Electron Affinity االلكرتونية االلفة 3 - 10 - 1
المتعادلة الذرة قابلية بانها االلكترونية االلفة تعرف
واحد الكترون اكتساب على الغازية الحالة في ًاكهربائي
.الفلور ذرة في كما ،الطاقة من ًامقدار وتحرير
F + e -
F -
+ طاقة
العدد بزيادة الدورات في للعناصر االلكترونية االلفة تزداد
اضافة صعوبة فتزداد الواحدة الزمرة عناصر في اما لها الذري
الذري العدد زاد فكلما للعنصر الذري العدد بزيادة االلكترون
النبيلة العناصر وتعتبر .االلكترون اضافة صعوبة ازدادت
اضافة الصعوبة من النه الكترونية الفة لها التي العناصر اقل
.اليها الكترونات
Electronegativity الكهر�سلبية 4 - 10 - 1
السالبـــة الشحنــة تكــون المــركبات مــن الكثــير فــي
غيرها دون معينة ذرة من بالقرب مركزة التآصر اللكترونات
وتعرف للمركب الكيميائية الخواص في كبير بشكل يؤثر مما
التآصر الكترونات جذب على الذرة قدرة بانها الكهرسلبية
تعلم هل
خاصيــة هــي الكهرسلبيــة
في الـذرات خـــواص مـــن
طاقـــة بينمــا المركبـــات
االلكترونية وااللفة التأين
للــــذرات خاصيتـــان همـــا
. المفردة بحالتها](https://image.slidesharecdn.com/random-161027114933/85/slide-35-320.jpg)
![36
العناصر اعلى الفلور ان وبما كيميائي مركب اي في نحوها
وحددت للكهرسلبية كقياس 4 الرقم اعطاءه تم فقد كهرسلبية
،الفلور كهرسلبية على ًاقياس العناصر لباقي القيم هذه
.])21 - 1( الشكل[
مع الدورة في الذري العدد زاد كلما الكهرسلبية تزداد
العدد زاد كلما فتقل الزمر في اما االستثناءات بعض وجود
.الذري
ال بعضها الن شاذة فتعتبر النبيلة للغازات وبالنسبة
لكن له الكهرسلبية تعيين يمكن ال وبالتالي مركبات يكون
عالية كهرسلبية ذا فيكون مركبات النبيل الغاز كونُي عندما
.ًاجد
والالفلزية الفلزية اخلوا�ص 5 - 10 - 1
الذري العدد لتغير ًاتبع والالفلزية الفلزية الخواص تتغير
العددازدادفكلما ،الواحدةالدورةلذراتأوالواحدةالزمرةلذرات
وتزداد لتظهر الفلزية الخواص تقل واحدة دورة لذرات الذري
الليثيوم يظهر الثانية الدورة في ،ًالفمث .الالفلزية الخواص
بخواص البورون يأتي ثم الفلزية الخواص والبريليوم
كالكاربون الدورة عناصر بقية تأتي ثم الفلزات أشباه
تعلم هل
كهـرسلبيةاقلالفلـزاتان
ان كما ،الالفلزات مـــن
مـــرتبطــة الكهرســـلبية
صغر فكلما الذرة بحجم
ازدادت الـــــذرة حجــــم
الذرة ان اي كهرسلبيتها
قـــوة تمـــلك الصغيــرة
اللكتروناتها اكبـــر جذب
الــــذرات واللكترونـــــات
.االخرى
)21 - 1( الشكل
لذرات الكهرسلبية تدرج
.العناصر بعض
تارودلا
رمزلا](https://image.slidesharecdn.com/random-161027114933/85/slide-36-320.jpg)

















![58
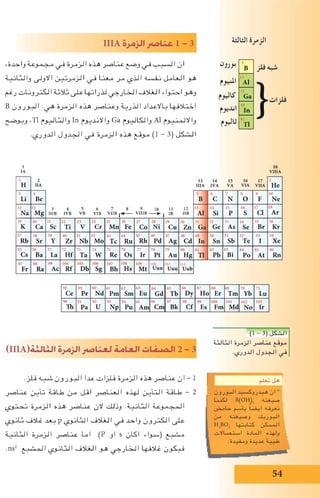
الكيميائية الخواص – 2
االملنيوم في االوكسجني تأثير – أ
يتأكسد الهواء الى االملنيوم تعرض عند بأنه ًاسابق ذكرنا
ًاجد رقيقة بطبقة االملنيوم فيكتسي ،فقط اخلارجي سطحه
وهذا ،الفلز بسطح االلتصاق شديد يكون الذي اوكسيده من
في يحدث ما غير وهذا ،التآكل استمرار من الفلز يقي ما
.احلديد عنصر
ًامحرر ساطع وبلهب بشدة االملنيوم مسحوق يحترق – ب
:االتية املعادلة حسب التفاعل ويحدث عالية طاقة
4Al + 3O2
2Al2
O3
+ طاقة
مسحوق
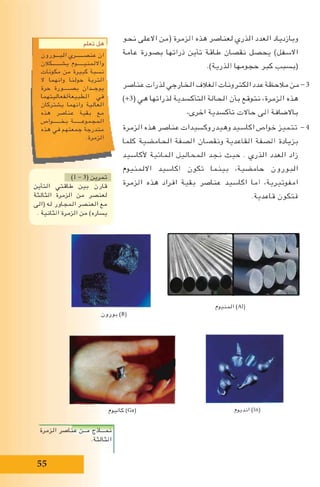
مختزل عامل االلمنيوم - جـ
)III( الحديد واوكسيد االلمنيوم مسحوق من خليط يوضع
شريط يثبت ثم ،رمل فيه وعاء في تثبت بجفنة ) Fe2
O3
(اي
مع الشريط نهاية وتحرق مناسب بطول المغنيسيوم من
مسحوق تفاعل ومالحظة امتار 3 عن تقل ال مسافة االبتعاد
ًامصحوب ًاشديد ًالتفاع )III( الحديد اوكسيد مع االلمنيوم
تطاير مع ساطع وبلهب الحرارة من كبيرة كمية بانبعاث
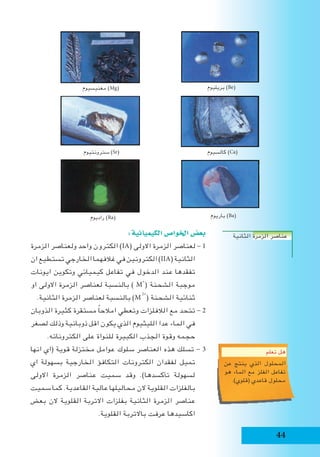
تكون التفاعل هذا عن وينتج .المجاور الشكل في كما شرر
اوكسيد باختزال االلمنيوم قيام نتيجة ،الحديد منصهر
الحرارة بفعل انصهر الذي الحديد وتحرير )III( الحديد
والمعادلة ،الثرميت بتفاعل التفاعل هذا ويسمى ،العالية
.ذلك توضح التالية
الكبيرة الحديدية االجهزة لحيم في التفاعل هذا من ويفاد
يستعمل كما .])3 - 3( الشكل [الحظ .الحديد سكك وقضبان
الموجودة خاماتها من الفلزات بعض الستخالص االلمنيوم
.ًالمختز ًالعام كونه على ًااعتماد اكاسيد هيئة على
2Al + Fe2
O3
Al2
O3
+ 2Fe + عالية حرارية طاقة
االملنيوم مسحوق III احلديد اوكسيد االملنيوم اوكسيد حديد
.الثرميت تفاعل](https://image.slidesharecdn.com/random-161027114933/85/slide-58-320.jpg)



![62
هيدروكسيد مع Al2
(SO4
)3
االلمنيوم كبريتات محلول مثل
:االتية المعادلة في كما البوتاسيوم او الصوديوم
في تذوب ال بيضاء جيالتينية مادة االلمنيوم وهيدروكسيد
.الماء
Al2
O3
االلمنيوم اوكسيد – 2
كما االلمنيوم لهيدروكسيد الشديد التسخين من يحضر
:االتية المعادلة في
∆
2Al (OH)3
Al2
O3
+ 3H2
O
،نقية غير بصورة الطبيعة في االلمنيوم اوكسيد يوجد وقد
.وتلميعها المعادن صقل في تستعمل صلدة مادة شكل وعلى
االحجار من الكثير تركيب في االلمنيوم اوكسيد يدخل كما
تعطيها التي المعادن بعض مع ًامخلوط يكون عندما الكريمة
.جميلة ًاوالوان ًابراق ًامظهر
Alum الشب – 3
كبريتات محلولي من متكافئين مقدارين مزج عند
المحلول وترك المائيين البوتاسيوم وكبريتات االلمنيوم
كبريتات على يحتوي ملح بلورات على نحصل ،ماؤه ليتبخر
بنسبة التبلور ماء وجزيئات البوتاسيوم وكبريتات االلمنيوم
]KAl (SO4
)2
. 12H2
O[ : هي للشب العامة الصيغة و .ثابتة كتلية
.البوتاس شب ًاايض ويسمى
لتعقيم منها متعددة مجاالت في االعتيادي الشب يستخدم
،بسهولة الدم تخثر على يساعد حيث ،الخفيفة الجروح بعض
حيث الجروح على Al(OH)3
وترسب الماء في ذوبانه بسبب
االصباغ تثبيت في يستخدم كما فيتخثر الدم سيالن يوقف
.الشرب مياه تصفية وفي االقمشة على
∆
Al2
(SO4
)3
+ 6NaOH 2Al(OH)3
+ 3Na2
SO4
كبريتات هيدروكسيد هيدروكسيد كبريتات
االملنيوم الصوديوم االملنيوم الصوديوم
فـــي االلمنيـــــوم اوكسيـــــد
.الكريمة االحجار](https://image.slidesharecdn.com/random-161027114933/85/slide-62-320.jpg)



![66
مقدمة 1 - 4
اذ ،حد ابعد الى الكيمياء علم في مهمة المحاليل تعتبر
المألوف الوسط هي تكون خاصة بصفة السائلة المحاليل ان
تساعد انها حيث الكيميائية للتفاعالت بالنسبة ًاغالب
التفاعل لحدوث المتفاعلة المواد بين التداخل حدوث على
.الكيميائي
Solution املحلول 2 - 4
بينها يحدث ال اكثر او مادتين من مكون متجانس خليط
المحلول في بوفرة الموجودة المادة تسمى ،كيميائي تفاعل
المحلول في بقلة الموجودة المادة وتسمى )Solvent( مذيب
:االتية بالمعادلة ذلك تمثيل ويمكن .)Solute( بالمذاب
مذاب + مذيب محلول
Solute + Solvent Solution
املحاليل انواع 1 - 2 - 4
المحاليل هي ًاشيوع واكثرها اهمها انواع عدة المحاليل
هذه تحضير ويمكن سائل المذيب يكون عندما اي ،السائلة
الطعام ملح اذابة مثل ،سائل في صلبة مادة باذابة المحاليل
اذابة او الطعام ملح محلول على لنحصل الماء في )NaCl(
سائل او ،)قاعدي (محلول الماء في الصوديوم هيدروكسيد
سائل في غاز اذابة او الماء في الكحول كإذابة سائل في
ويسمى الماء في )HCl( الهيدروجين كلوريد غاز كاذابة
)حامضي (محلول الهيدروكلوريك بحامض االخير الناتج
.])1 - 4( الشكل[
H2
O
HCl HCl
كلوريد غاز حامض محلول
الهيدروجين الهيدروكلوريك
)1 - 4( الشكل
المحاليل من مختلفة انواع
حامضي محلول
قاعدي محلول
ملحي محلول
KOH
HCl
KCl
تعلم هل
في نستخدمه الذي الماء
يعتبر اليومية حياتنا
على يحتوي حيث محلول
والبكتريا الفلزية االمالح
االخرى المواد من وكثير
تراكيزها نسبة يحدد الذي
بتـواجـــدهـا المســـــموح
ًاطبق الشرب مياه في
.العالمية للمعايير](https://image.slidesharecdn.com/random-161027114933/85/slide-66-320.jpg)
![67
الهواء مثل غاز في غاز منها للمحاليل أخرى انواع وهناك
المختلفة السبائك مثل صلب في صلب ومحلول ،الجوي
في وسنتطرق الذهب وسبائك المعدنية النقود قطع واهمها
.فقط السائلة المحاليل الى الفصل هذا
املحاليل طبيعة 2 - 2 - 4
كمية حسب وذلك تسميتها في المحاليل تختلف
فالمحلول .الذوبان عملية طبيعة او والمذيب المذاب
المحلول هو )Saturated Solution( مشبع بأنه يوصف الذي
المذيب وان المذاب من ممكن قدر أكبر على يحتوي الذي
عند المذاب من اخرى زيادة اي يذيب ان يستطيع ال
كمية تفوق عندما أما .معين وضغط محددة حرارة درجة
في اذابته من للمذيب يمكن قد ما محلول في المذاب
المشبع بفوق المحلول هذا يسمى االعتيادية الظروف
ثابت غير المحاليل من النوع وهذا )Supersaturated Solution(
راسب شكل على المذاب من الزائدة الكمية تلفظ أنها حيث
مشبع غير بأنه المحلول ويعرف .مشبع محلول الى ليتحول
مناقلالمذابمنكميةعلىاحتوىاذا)Unsaturated Solution(
المحددين والضغط الحرارة درجة عند للتشبع الالزمة الكمية
.)2 - 4( الشكل
عند يسمى المحلول في المذاب جزيئات تتأين عندما
،)Electrolyte Solution( االلكتروليتي بالمحلول المحلول ذلك
جزيئاته تتأين عندما ًاقوي ًاالكتروليت يكون قد والمذاب
الهيدروكلوريك حامض مثل المحلول في تام بشكل
ان اي ًاضعيف ًاالكتروليت المذاب يكون وقد .])3 - 4 (الشكل[
HCl H+
+ Cl-
)2 - 4( الشكل
.مشبع محلول - أ
.المشبع فوق محلول - ب
.مشبع غير محلول - جـ
)3 - 4( الشكل
االلكتروليت جزيئات تتأين
في تـــام بشـــــكل القــــــــوي
.المذيب](https://image.slidesharecdn.com/random-161027114933/85/slide-67-320.jpg)
![68
ًاجد بسيطة بدرجة ًاوأحيان تامة غير ٍبدرجة تتأين جزيئاته
بدرجة )(يتأين يتفكك حيث الهيدروفلوريك حامض مثل
مع توازن حالة في ايوناته وتكون المذيب في ًاجد قليلة
ادناه المعادلة وفي ،])4 - 4( الشكل[ المتأينه غير الجزيئات
حالة في ًاجزئي المتأينة المادة ان المتعاكسة االسهم تعني
.الناتجة االيونات مع توازن
HF H+
+ F-
تسمى ًامطلق المذيب في تتأين ال جزيئاتها مركبات وهناك
والكحول السكر مثل الكتروليتية غير بمحاليل محاليلها
.االثيلي
Solubility الذوبان قابلية 3 - 4
تذوب ان يمكن المذابة المادة من كمية اكبر بانها تعرف
مشبع محلول على للحصول معين مذيب من ثابت حجم في
الذوبان قابلية وتختلف .)(محددة معلومة حرارة درجة عند
.والضغط الحرارة ودرجة والمذيب المذاب لطبيعة ًاتبع
.يأتي كما بايجاز سنشرحها والتي
واملذيب املذاب طبيعة 1 - 3 - 4
دورق في الطعام ملح بلورات من صغيرة كمية وضعت اذا
الدورق رج واذا ،ببطء فيه تذوب البلورات فان ،ماء به
عملية تؤدي حيث ،اكبر بسرعة البلورات تذوب بمحتوياته
الن ،اكبر بصورة بالماء البلورات سطح مالمسة الى الرج
وهذا ،للذوبان المعرض بالسطح تتعلق ظاهرة الذوبان عملية
فيه السكر وضع بعد بالملعقة الشاي قدح تحريك في السبب
حبيبات من اسرع يذوب السكر مسحوق ان كما .)5 - 4 (الشكل
الماء جزيئات لمالمسة المعرض المسحوق سطح الن ،السكر
كلما انه نستنتج ًااذ ،السكر لحبيبات السطح من اكبر يكون
سرعة ازدادت للمذيب المعرض المذابة المادة سطح ازداد
غير أو القطبية فالطبيعة للمذيب بالنسبة اما ،الذوبان
)4 - 4( الشكل
االلكتروليت جزيئات تتأين
المــــذيب فــــي الضـــعيف
وتكــــون جزئـــــي بشــــــكل
متواجدة الناتجة االيونات
غير الجزيئات مع بتوازن
.المتأينة
)5 - 4( الشكل
عند بســرعة الســــكر يذوب
.بالملعقة تحريكه](https://image.slidesharecdn.com/random-161027114933/85/slide-68-320.jpg)

![70
Concentration of Solution املحلول تركيز 4 - 4
هما رئيسيين جزئين من يتكون المحلول ان اسلفنا كما
المذاب كميات حيث من المحاليل وتختلف .والمذيب المذاب
هذه عن التعبير بواسطتها يمكن طرق وهناك .فيها والمذيب
عادة العالقة هذه عن ويعبر ببعض بعضها وعالقتها الكميات
المادة كمية بانه المحلول تركيز يعرف .المحلول بتركيز
التعبيرويمكن،المحلولاوالمذيبمنمعينةكميةفيالمذابة
مصطلحي ويستخدم ًاكمي او ًاوصفي المحلول تركيز عن
تركيز لوصف )Concentreated( ومركز )Dilute( مخفف
كمية على يحتوي الذي فالمحلول .])8 - 4( [الشكل المحلول
بينما .مخفف محلول بانه يوصف المذاب من ًانسبي قليلة
المذاب من كبيرة كمية على يحتوي الذي المحلول يوصف
المحلول تحويل يمكن كما ،])9 - 4( [الشكل مركز محلول بانه
.اليه المذيب من اكبر كمية باضافة مخفف الى المركز
طرائق بعدة المحلول تركيز عن نعبر ان فيمكن ًاكمي اما
:اهمها
الكتلية املئوية بالن�سبة الرتكيز 1 - 4 - 4
وحدة 100 في المذابة المادة من الكتلة وحدات عدد وهو
او )المذيب او للمذاب الكتلية (النسبة المحلول من كتلة
المحلول من غرام مئة في المذاب غرامات عدد هي ببساطة
كما والمذيب للمذاب الكتلية المئوية النسبة وتحسب
:يأتي
: ان او
:آخر بتعبير او
)8 - 4( الشكل
مركزومحلولمخففمحلول
.النحاس كبريتات من
)9 - 4( الشكل
المذاب جزيئات توزيع - أ
.المركز المحلول في
المذاب جزيئات توزيع - ب
.المخفف المحلول في
المذاب كتلة
%100 × ـــــــــــــــــــــــــــــــــــــ = للمذاب الكتلية النسبة
المحلول كتلة
)m1
( المذاب كتلة
%100 × ـــــــــــــــــــــــــــــــــــــــــــــــ = للمذاب الكتلية النسبة
)m1
+m2
( المحلول كتلة
)m1
( المذاب كتلة
%100 × ـــــــــــــــــــــــــــــــــــــــــــــــ = للمذاب الكتلية النسبة
)mT
( المحلول كتلة
) أ (
)(ب
مخففمركز](https://image.slidesharecdn.com/random-161027114933/85/slide-70-320.jpg)

![72
:2 - 4 مثال
من % 4 مقدارها كتلية نسبة على يحتوي الخل من نموذج
نحصل لكي نحتاجها التي الخل كمية ما .الخليك حامض
الخليك؟ حامض من 20 g على
:احلـــــــــــل
m1
%100 × ــــــــــــــ = للمذاب الكتلية النسبة
mT
20 g
%100 × ـــــــــــــــ = % 4
mT
2000
ــــــــــــــ = mT
4
mT
= 500 g نحتاجها التي الخل كمية
احلجمية املئوية بالن�سبة الرتكيز 2 - 4 - 4
الى المحلول مكونات من مكون كل حجم نسبة وهي
.مئة في ًامضروب للمحلول الكلي الحجم
المحلول ولحجم V2
المذيب ولحجم V1
المذاب لحجم يرمز
] )V1
+ V2
( والمذيب المذاب حجمي مجموع ويمثل [ VT
عن للتعبير الرياضية الصيغة نكتب ان يمكن عام وبشكل
)2 - 4( تمرين
لكل الكتلية النسب احسب
الهيدروكلوريك حامض من
20 g تخفيف عند والماء
الماء من 80 g في HCl من
.المقطر
)V1
( المذاب حجم
%100 × ـــــــــــــــــــــــــــــــــــــــــــــــــ = للمذاب الحجمية النسبة
)V1
+ V2
( المحلول حجم
)V1
( المذاب حجم
%100 × ـــــــــــــــــــــــــــــــــــــــــــــ = للمذاب الحجمية النسبة
)VT
( المحلول حجم
:للمذيب الحجمية المئوية النسبة ايجاد يمكن الطريقة وبنفس
)V2
( المذيب حجم
%100 × ـــــــــــــــــــــــــــــــــــــــــــ = للمذيب الحجمية النسبة
)VT
( المحلول حجم
تعلم هل
من يتكون الخل محلول ان
بتراكيز الخليك حامض
من كمية في مذاب مختلفة
.الماء](https://image.slidesharecdn.com/random-161027114933/85/slide-72-320.jpg)






![82
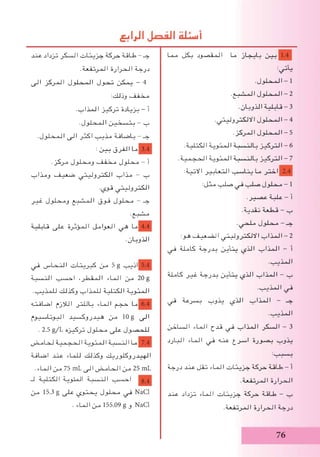
وجوده 1 - 3 - 5
االرض قشرة في انتشارا األكثر العنصر السليكون يعتبر
االرضية القشرة ربع من اكثر يشكل حيث ،األوكسجين بعد
االوكسجينمعًامتحديكونماًاغالبحيث،%28الىتصلبنسبة
يوجد وال .ورملية طينية ترسبات شكل على او التربة في
الصخور في يوجد ولكنه الطبيعة في حرة بصورة السليكون
تركيب في ويدخل )SiO2
( السليكون اوكسيد ثنائي هيئة على
وللسليكون .والرمل الكوارتز شكل وعلى السليكات مختلف
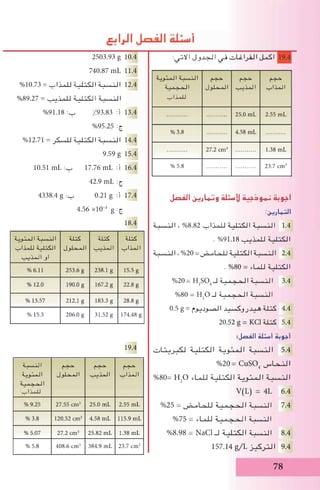
متبلورة احداهما صورتين )3 - 5( الشكل في مبين كما
متبلورة غير واالخرى غامق بني المسحوق لون يكون وفيها
اقل منه المتبلورة ،غامق رصاصي مسحوقه لون يكون وفيها
. نفسه التركيب لهما الصورتين وكلتا فعالية
حت�ضريه 2 - 3 - 5
ًامختبري تحضيره - أ
عنصر بتسخين المتبلور غير السليكون يحضر
وفق SiF4
السليكون فلوريد رباعي من جو في البوتاسيوم
:المعادلة
∆
SiF4
+ 4K Si + 4KF
في السليكون باذابة المتبلور السليكون يحضر بينما
بلورات تنفصل حيث المحلول تبريد ثم االلمنيوم منصهر
.المحلول عن السليكون
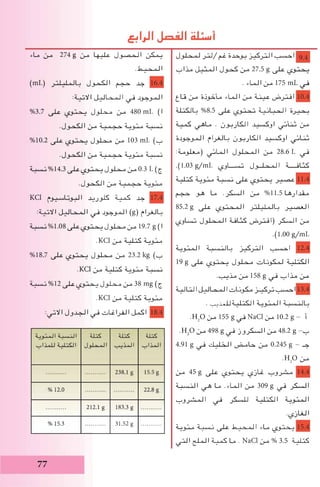
ًاصناعي تحضيره - ب
)SiO2
( السليكا باختزال صناعيا السليكون يحضر
المغنسيوم أو الكاربون وباستخدام عالية حرارة بدرجات
:آالتية المعادلة في كما .])4 - 5( الشكل[ مختزل كعامل
∆
SiO2
+ 2C 2CO ↑ + Si
تعلم هل
مرة الول السليكون حضر
برزلوس العالم قبل من
3281م عام )Berzelius(
فلوريد رباعي تفاعل من
البوتاسيوم مع السليكون
على حصل حيث
.البلوري غير السليكون
البلوري السليكون اما
قبل من مرة الول فحضر
)Deville( ديفايل العالم
التحلل من 4581م عام
لكلوريد الكهربائي
غير وااللمنيوم الصوديوم
نحو على الحاوي النقي
بداية وفي .سليكون %10
7091م العشرين القرن
بوتر العالم اكتشف
تحضير طريقة )Pottr(
تفاعل من السليكون
الكاربون مع السليكا
الطريقة اصبحت والتي
في المعتمدة التجارية
.الحاضر الوقت
)3 - 5( الشكل
.السليكون عنصر صور
متبلور - ب متبلور غير - أ
برزلوس العالم](https://image.slidesharecdn.com/random-161027114933/85/slide-82-320.jpg)
![83
بعض على يحتوي الطريقة بهذه الناتج السليكون ان
الى 90 من فيه السليكون نسبة تتراوح بحيث ،الشوائب
من النوع هذا يستخدم .الصناعي بالسليكون ويسمى % 95
وخاصة )Steel( والحديد البرونز سبائك صناعة في السليكون
. )Silicones( السليكونات تحضير وفي المطاوع الحديد
تكفي ال نقاوة ذو المنتج السليكون من النوع هذا إن
الرقائق أو الموصالت أشباه من كل صناعة في لالستخدام
ينقى فانه لذلك .الشمسية الخاليا أو )microchips( الدقيقة
ًالاو السليكون كلوريد رباعي الى أعاله السليكون بتحويل
المختزلة العوامل بأحد السليكون الى ثانية مرة يختزل ثم
: يأتي وكما المغنيسيوم مثل
Si + 2Cl2
SiCl4
SiCl4
+ 2Mg Si + 2MgCl2
بغسله وذلك السليكون من )MgCl2
( إزالة السهل من حيث
،السليكون يذوب وال )MgCl2
( يذوب حيث الحار بالماء
أخرى عملية تستخدم نقاوة أعلى سليكون على وللحصول
.])5 - 5( الشكل[ التكرير منطقة طريقة تسمى النقاوة لزيادة
ثم اسطواني قالب شكل على السليكون يعمل الطريقة هذه في
)5 - 5( الشكل
التكـــريرمنطقــــةطريقـــــة
عالي السليكون لتحضير
.النقاوة
)4 - 5( الشكل
.ًاصناعي السليكون تحضير
سليكا
)(كوارتز
كاربون
)(فحم
كهربائي مصدر
للتسخين
CO
شحن
منصهر
السليكون
تبريد
وقولبة
فرن
حراري
تركيز منطقة
الشوائب
منصهر
السليكون
قالب
السليكون
حراري مصدر
متحرك
خامل غاز](https://image.slidesharecdn.com/random-161027114933/85/slide-83-320.jpg)

![85
ال�سليكون ا�ستعمال 4 - 3 - 5
-: منها واسعة استخدامات للسليكون
المتكاملة الدوائر لصناعة االلكترونية الصناعة في - 1
.])6 - 5( الشكل [الحظ ،الشمسية الخاليا وفي
. مختلفة صناعات في تستخدم التي السبائك في - 2
. والسيراميك والسمنت الزجاج صناعة في - 3
األهمية ذات العضوية السليكونية المواد صناعة في - 4
.والبالستيكات الزيوت ومنها الكبيرة التجارية
ال�سليكونمركبات 5 - 3 - 5
،السليكون يكونها التي المركبات من كبير عدد هنالك
: منها نذكر
الهيدروجين مع السليكون مركبات - أ
)السليكون (هيدريدات
منها ،والهيدروجين السليكون من تتكون مركبات وهي
المغنيسيوم سليسيد تفاعل من المركب هذا ويحضر SiH4
وفق الهيدروكلوريك كحامض المعدنية الحوامض مع Mg2
Si
:االتية المعادلة
Mg2
Si + 4HCl SiH4
+ 2MgCl2
تلقائيا )SiH4
( يشتعل فمثال ،جدا فعالة مركبات والهدريدات
وفق والماء السليكون اوكسيد ثنائي لتكوين الهواء في
:االتية الكيميائية المعادلة
SiH4
+ 2O2
SiO2
+ 2H2
O
األوكسجين مع السليكون مركبات - ب
SiO2
:)السليكا ( السليكون اوكسيد ثنائي - 1
حجر مثل نقية سليكا شكل على الطبيعة في وتوجد
الصالدة شديدة مواد وهي ،])7 - 5( [الشكل والكوارتز الصوان
وسليكا .الصلب الحديد وتخديش الزجاج قطع في تستعمل
كميات على تحتوي التي ])8 - 5( الشكل[ الرمل مثل نقية غير
.مختلفة ألوانا تكسبها التي الشوائب من متفاوتة
)6 - 5( الشكل
في الســليكـون استخــــدام
.المتكاملة الدوائر صناعة
)7 - 5( الشكل
السليكا اشكال احد الكوارتز
.النقية
)8 - 5( الشكل
السليكا اشكال احد الرمل
.النقية غير](https://image.slidesharecdn.com/random-161027114933/85/slide-85-320.jpg)
![86
:أهمها خواص وللسليكا
أو البروم أو للكلور تعرضها عند تتفاعل ال ،فعالة غير - أ
.الحوامض ومعظم الهيدروجين
: والقواعد الهيدروفلوريك حامض مع تتفاعل - ب
SiO2
+ 6HF H2
SiF6
+ 2H2
O
السايالن فلوريد سداسي
SiO2
+ 2NaOH Na2
SiO3
+ H2
O
الكاربونات أو االكاسيد مع التفاعل على القابلية لها - جـ
تعرف مركبات تتكون حيث ،الشديد بالتسخين الفلزية
.بالسليكات
القلوية الفلزات سليكات محاليل الى الحوامض إضافة - د
الى تجفيفها يمكن التي ،المائيـــة الســـليكا يعطـــي
)Silica Gel( السليكا جل يسمى بلوري غير مسحوق
كعامل رئيسية بصورة يستعمل حيث ،])9 - 5( [الشكل
العالية وقابليته الكبيرة السطحية لمساحته وذلك مجفف
.الماء المتصاص
Silicates السليكات - 2
وتكون ،الطبيعة في واسعة بصورة السليكات تنتشر
ويظهران األرضية القشرة من %74 حوالي األوكسجين مع
األرضية الكرة سطح على الوفرة ذات للعناصر كسليكات
وسليكات )CaSiO3
( الكالسيوم سليكات مثل ،])10 - 5( الشكل[
أو اوكسيد تفاعل من تحضران اللتان .)Na2
SiO3
( الصوديوم
المعادلتينفيكما،الشديدبالتسخينالسليكامعالفلزكاربونات
شديد تسخين
: اآلتيتين
CaO + SiO2
CaSiO3
شديد تسخين
Na2
CO3
+ SiO2
Na2
SiO3
+ CO2
سليكات هي واستعماال شيوعا السليكات أنواع أكثر إن
المائي محلولها والتي الماء في للذوبان القابلة الصوديوم
)9 - 5( الشكل
.مجفف كعامل جل السليكا
)10 - 5( الشكل
السليكات اشكال احدالطين
.الطبيعية](https://image.slidesharecdn.com/random-161027114933/85/slide-86-320.jpg)
![87
صناعية مجاالت في يستخدم الذي )الزجاج (ماء يدعى المركز
،الحرائق من والورق األقمشة بعض حماية مثل مختلفة
البناء في استعماله وكذلك ،رخيصة الصقة كمادة واستعماله
. األخير لتقوية السمنت مع بخلطه
السليكون كاربيد - جـ
على تساهمية بأواصر السليكون مع الكاربون فيه ويرتبط
كاربون ذرة كل تحاط حيث ثالث باتجاهات شبكية بنية شكل
تحاط أيضا هي والتي سليكون ذرات بأربع معين بترتيب
الماس لبنيـــة مشــــابهـة كـاربـــون ذرات بأربــــع مـــنهـا كل
السليكون كاربيد تجعل البنية هذه إن .])11 - 5( [الشكل
وفي الجام ورق في كما جالية كمادة ويستخدم للغاية صلد
مسحوقه يخلط الغاية ولهذه .])12 - 5( [الشكل الكوسرة حجر
قالب في ويوضع الصوديوم سليكات أو الطين مع الناعم
السليكون تفاعل من السليكون كاربيد ويحضر .ويحرق
بدرجة الكهربائي القوس فرن في الكاربون مع اوكسيده أو
-:آالتية المعادالت وفق عالية حرارية
Si + C SiC
SiO2
+ 3C SiC + 2CO
Silicones السليكونات - د
ومستقرة سامة غير للسليكون عضوية مركبات وهي
السليكون زيوت وأهمها .الحرارة درجات من واسع مدى على
طبيعة السطوح على تضفي بأنها تتصف التي )Silicone oil(
األنسجة سطوح مثل للرطوبة مضادة او لاللتصاق مانعة
بأنه يتصف )Silicone Rubber( السليكون ومطاط .والبنايات
ويبقى الهيدروكاربوني المطاط من حراريا استقرارا أكثر
صناعة في ويستعمل ،الحرارة درجات من واسع مدى في مرنا
والراتنجات .أحكام كمواد والمطابخ الحمامات وفي القوالب
مواد صناعة في تستخدم التي )Silicone Resin( السليكونية
.أيضا للماء مضادة البناء مواد جعل وفي كهربائيا عازلة
تعلم هل
:)Aerogels(الهوائي الجل
المصنعة المواد من وهو
الكثافة ذات الجديدة
%10 من وتتكون القليلة
السليكون اوكسيد ثنائي
.غـــــاز او هــــواء %90 و
اخف المادة هذه وتصبح
تمأل عندما الهواء من
وهـــي ،الهــيليوم بغــــــاز
بصـــــرية صفــــات تمتلك
وكهــــــربائية وصوتيــــــة
اهم احد ،عادية غير
في دخولها استخداماتها
،الشبابيك زجاج صناعة
السليكا توضع حيث
من طبقتين بين الهوائية
صفات لتحسين الزجاج
.للزجاج العزل
)11 - 5( الشكل
.السليكون كاربيد بنية
)12 - 5( الشكل
.كوسرة حجر](https://image.slidesharecdn.com/random-161027114933/85/slide-87-320.jpg)












![104
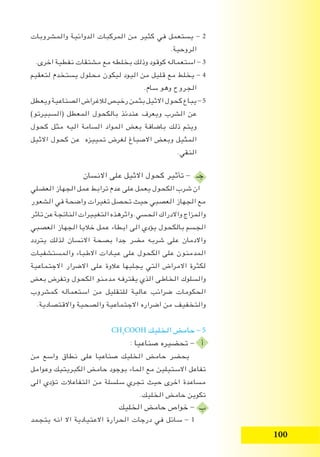
VA اخلام�سة الزمرة عنا�رص 1 - 7
)N( النتروجين عنصر من الزمرة هذه عناصر تتألف
والبزموث )Sb( واالنتيمون )As( والزرنيخ )P( والفسفور
للعناصـــر الــــدوري الجدول في موقعها مبين كما )Bi(
بامتالكها جميعها العناصر هذه تشترك .])1 - 7( الشكل[
.الخارجي الطاقة غالف في الكترونات لخمسة
VA اخلام�سة للزمرة العامة ال�صفات 2 - 7
معا تشكل الزمرة لهذه الخمسة العناصر أن من الرغم على
،األرضية القشرة في الوزن حيث من %0.2 عن تقل نسبة
في الزمرة هذه عناصر تتشابه .كبيرة أهمية تكتسب انها اإل
البعض في تختلف لكنها ،العام الكيميائي السلوك بعض
للترتيب المشتركة السمات تعكس هذه التشابه وأوجه .االخر
:الزمرة لهذه العامة الصفات واهم .لعناصرها االلكتروني
لعنصري الفلزية صفة من الزمرة هذه عناصر صفات تتدرج - 1
البزموث لعنصر فلزية صفة الى والفسفور النتروجين
اشباه واالنتيمون الزرنيخ عنصري من كل يكون بينما
.فلزات
15
P
7
N
33
As
51
Sb
83
Bi
12
Mg
11
Na
14
Si
13
Al
6
C
5
B
4
Be
3
Li
1
H
19
K
20
Ca
21
Sc
22
Ti
23
V
24
Cr
25
Mn
26
Fe
27
Co
28
Ni
29
Cu
30
Zn
31
Ga
32
Ge
37
Rb
38
Sr
39
Y
40
Zr
41
Nb
42
Mo
43
Tc
44
Ru
45
Rh
46
Pd
47
Ag
48
Cd
49
In
50
Sn
55
Cs
56
Ba
57
La
72
Hf
73
Ta
74
W
75
Re
76
Os
77
Ir
78
Pt
79
Au
80
Hg
81
Tl
82
Pb
87
Fr
88
Ra
89
Ac
104
Rf
105
Db
106
Sg
107
Bh
108
Hs
109
Mt
110
Uun
111
Uuu
112
Uub
9
VIIIB
7
VIIB
6
VIB
5
VB
4
IVB
3
IIIB
2
IIA
1
IA
11
IB
12
IIB
13
IIIA
14
IVA
8 10
15
VA
16
S
17
Cl
18
Ar
10
Ne
9
F
8
O
2
He
34
Se
35
Br
36
Kr
52
Te
53
I
54
Xe
84
Po
85
At
86
Rn
16
VIA
17
VIIA
18
VIIIA
)1 - 7( الشكل
للعناصر الدوري الجدول
الخامسة الزمرة وموقع
.فيه
.الزرنيخ
15
P
7
N
33
As
51
Sb
83
Bi](https://image.slidesharecdn.com/random-161027114933/85/slide-104-320.jpg)

![106
النرتوجني غاز حت�ضري 2 - 3 - 7
ًاوصناعي مختبريا النتروجين غاز تحضير يمكن
:وكاآلتي
ًامختبري تحضيره - 1
)NH4
Cl( االمونيوم كلوريد ملح من مزيج بتسخين وذلك
من قليلة كمية بوجود )NaNO2
( الصوديوم نتريت وملح
ويمكن ،])2 - 7( الشكل[ )انفجار حدوث (لمنع الماء
:االتيتين بالمعادلتين التفاعل عن التعبير
NH4
Cl + NaNO2
H2
O
NaCl + NH4
NO2
H2
O
∆
NH4
NO2
2 H2
O + N2
ًاصناعي تحضيره - 2
كبيرة تجارية وبكميات صناعيا النتروجين غاز يحضر
من الخالي المسال للهواء التجزيئي التقطير بعملية
ًاتارك أوال النتروجين يتقطر حيث ،الكاربون اوكسيد ثنائي
من أوطأ )-198i
o
C( غليانه درجة لكون وذلك ،االوكسجين
النتروجين غاز يحتوي ،)-183i
o
C(االوكسجين غليان درجة
من ضئيلة كميات على الطريقة بهذه عليه الحصول يتم الذي
برادة فوق الغاز بإمرار منها التخلص يمكن والتي االوكسجين
.CuO لتكون االوكسجين مع تتفاعل والتي الساخنة النحاس
)2 - 7( الشكل
مــن النتـــروجين تــحضيـر
.االمونيوم نتريت
N2
النتروجين غاز
ماء
ماء
االمونيوم كلوريد
مع
الصوديوم نتريت](https://image.slidesharecdn.com/random-161027114933/85/slide-106-320.jpg)

![108
النرتوجنيمركباتبع�ض 5-3-7
غالفها في الكترونات خمسة على النتروجين ذرة تحتوي
تساهمية أواصر تكوين في المشاركة يمكنها ولذلك الخارجي
كما ثالثية أو )NH3
( االمونيا جزيء في كما مفردة تكون قد
الكترونات ثالثة اكتساب او .)N2
( النتروجين جزيء حالة في
العناصر ذرات مع اتحادها وحسب ،واحد الكترون اكتساب أو
مركباتها في االخرى
:هي النتروجين مركبات أهم ومن
)NH3
( االمونيا غاز - 1
.والهيدروجين للنتروجين المهمة المركبات احد هو
النباتات و الحيوانات أجسام تحلل من الطبيعة في ينتج
امالح هيئة على التربة في االمونيا توجد و كما ,موتها بعد
.االمونيوم
ًامختبري االمونيا تحضير - أ
كلوريد ملح بتسخين مختبريا االمونيا غاز يحضر
المعادلة وحسب الكالسيوم هيدروكسيد مع بلطف االمونيوم
:االتية
باإلزاحة يجمع فانه الهواء من اخف االمونيا غاز أن وبما
اوكسيد يحوي عمود على يمرر أن بعد للهواء السفلية
في كما للغاز المصاحبة الرطوبة من للتخلص الكالسيوم
.])3 - 7( الشكل[
)3 - 7( الشكل
.ًامختبري االمونيا تحضير
∆
2 NH4
Cl + Ca(OH)2
CaCl2
+ 2 H2
O + 2 NH3
CaO
الرطوبة الزالة
هواء
CaO عمود
االمونيا غاز
غاز يجمع
باالزاحة االمونيا
للهواء السفلىNH4
Cl + Ca(OH)2
هواء](https://image.slidesharecdn.com/random-161027114933/85/slide-108-320.jpg)
![109
:صناعيا االمونيا إنتاج - ب
هابر بطريقة كبيرة وبكميات صناعيا االمونيا إنتاج يتم
للنتروجين المباشر االتحاد تتضمن والتي ])4 - 7( الشكل[
:اآلتية المعادلة وحسب الهيدروجين مع
N2
+ 3 H2
2 NH3
ًاسابق ذكره مر وكما
لالمونيا الفيزيائية الخواص
يؤدي والذعة نفاذة رائحة ذو اللون عديم غاز االمونيا - 1
.الهواء من اخف وهو ،العين تدمع إلى استنشاقه
االمونيابماءالمائيمحلولهويعرف ،الماءفيالذوبانكثير -2
ًامعرض تركه او المائي محلوله تسخين وعند ،)NH4
OH(
قابلية على البرهنة ويمكن ،االمونيا غاز يفقد فانه للجو
في المبينة النافورة بتجربة الماء في العالية ذوبانه
.)5 - 7( الشكل
.هابر فريتز العالم
)4 - 7( الشكل
ًاصناعيـــ االمونيـــا انتـــاج
.هابر بطريقة
حراري مبادل
التسخين قبل الغازات
عالي ضغط تحت
تسخين ملف
سائلة امونيا
NH3
الناتج NH3
N2
+ H2
المتجددة الغازات تبريد
N2
+ H2
المتفاعلة غير
)(راجعة
الغازات وضغط لتحريك مروحة
مساعد عامل
)460-550(˚C](https://image.slidesharecdn.com/random-161027114933/85/slide-109-320.jpg)

![111
لالمونيا الكيميائية الخواص
يتفكك ذلك ومع ،ًاكيميائي ًاثابت االمونيا جزيء يعتبر
على الغاز إمرار عند الهيدروجين و النتروجين لينتج
.الغاز خالل كهربائية شرارة إمرار عند أو ساخن فلزي سطح
في كما األوكسجين من جو في لالشتعال قابل االمونيا وغاز
:اآلتية المعادلة
4 NH3
+ 3 O2
2 N2
+ 6 H2
O
الحمراء الشمس زهرة ورقة لون يحول االمونيا محلول ان
.األزرق اللون إلى
االمونيا عن الكشف
اتحادها عند وجودها من والتأكد االمونيا عن الكشف يمكن
كثيفة بيضاء أبخرة ينتج حيث الهيدروجين كلوريد غاز مع
:االمونيوم كلوريد غاز لتكون نتيجة
NH3
+ HCl NH4
Cl
االمونيا غاز كلوريد غاز كلوريد غاز
الهيدروجين االمونيوم
Nitric Acid النتريك حامض - 2
االوكسجينية الحوامض أهم من النتريك حامض يعتبر
. HNO3
جزيئية صيغة ذو وهو للنتروجين
ًامختبري الحامض تحضير
ملح من مكون مزيج بتسخين عادة الحامض هذا يحضر
معوجة في المركز الكبريتيك حامض مع البوتاسيوم نترات
في التفاعل من الناتج النتريك حامض بخار ويكثف ,زجاجية
التعبير ويمكن ])6 - 7( الشكل[ بالماء مبرد استقبال وعاء
:يأتي بما التفاعل معادلة عن
∆
KNO3
+ H2
SO4
KHSO4
+HNO3
ورقة لون تغير القواعد
الى الحمراء الشمس زهرة
.الزرقاء](https://image.slidesharecdn.com/random-161027114933/85/slide-111-320.jpg)












![125
للكربيت العامة اخلوا�ص 3 - 3 - 8
الفيزيائية الخواص - 1
:اآلتية الفيزيائية الخواص الكبريت يمتلك
لون ذات االعتيادية الحرارة درجات في صلبة مادة .أ
.أصفر
.مميزة رائحة وذو الطعم عديم .ب
المذيبات بعض في يذوب ولكن الماء في يذوب ال .ج
CS2
الكاربون كبريتيد ثنائي مثل الالعضوية
الكبريت يترسب ًاتدريجي CS2
تبخير تم واذا
)S8
( الشكل ثماني تركيب ذات بلورات شكل على
.])3 - 8( الشكل[
.الكهربائي للتيار موصل غير .د
صفاتها في تتباين الطبيعة في متعددة صور له .هـ
األخرى العناصر وبعض الكبريت يمتلك.الفيزيائية
الخواص مختلفة إشكال وهي الصور من العديد
.نفسه للعنصر تعود واللون كالشكل الفيزيائية
إلى تقسيمها يمكن عديدة صور الكبريت ويمتلك
:هما رئيسيين نوعين
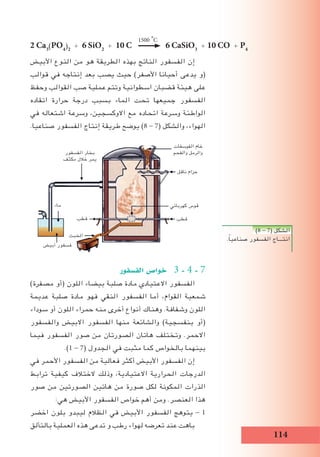
الكبريت هو ا ًشيوع وأكثرها البلورية الكبريت صور - 1
عند وثابتة ونّلال ةّليموني صفراء ريةِوّلب مادة وهو ني ِالمعي
على ويوجد ًااستقرار الصور أكثر وهو الغرفة حرارة درجة
وهنالك .البركانية المناطق في صفراء كبيرة بلورات شكل
بالكبريت تدعى البلوري الكبريت صور من آخر نوع
.الموشور تشبه بلوراته ألن وذلك الموشوري
المطاطي الكبريت أمثلتها ومن البلوري غير الكبريت - 2
تسخين من تحضيره ويمكن .)Plastic( اللدن الكبريت أو
البارد الماء في الكبريت سائل وصب )1500i
o
C( الى الكبريت
يحتوي الذي ])4 - 8( الشكل[ المطاطي الكبريت يتكون حيث
البلوري الكبريت من ًااستقرار أقل وهو حلزونية سالسل على
.البلورية الصورة إلى ببطء ويتحول
)3 - 8( الشكل
في الكبريت اذابة عند
كبريتيـــد ثنائــــي مـــذيب
المذيب وتبخير الكاربون
الكبريت يترسب ًاتدريجي
ذات بلورات شكل على
.)S8
( تركيب
)4 - 8( الشكل
.المعيني الكبريت )(أ
.الموشوري الكبريت )(ب
.المطاطي الكبريت )(ج
.
ب
أ
ج](https://image.slidesharecdn.com/random-161027114933/85/slide-125-320.jpg)

![127
الكربيت ا�ستعماالت 4 - 3 - 8
الصناعية المجاالت في عديدة استخدامات للكبريت
األسود والبارود الثقاب صناعة في يدخل فهو والزراعية
الزراعة في يستخدم كما .اشتعاله لسهولة النارية واأللعاب
مبيدات وفي األسمدة أنواع بعض و التربة قلوية لمعادلة
هو الكبريت استخدامات أهم أما .والحشرات الفطريات
،الكبريتيك حامض تحضير في كبيرة بكميات استخدامه
ويستخدم .العالم في تجارية كيميائية مادة أهم عدُي والذي
والمنسوجات والورق ،)(الطالء والدهانات األصباغ إنتاج في
ستخدمُي كما .الصناعية الكيميائية المنتجات من وعدد
المنتجات أما .النفط تصفية وفي الفلزات تعدين في ا ًأيض
والشامبو ،المطاط فتشمل ،الكبريت على المحتوية األخرى
الكيميائية المواد أمالح وفي )(المراكم السيارات وبطاريات
ومركباته الكبريت يدخل كما .التصوير أفالم في المستخدمة
لعالج يستخدم حيث ،المكونات من كواحد األدوية صناعة في
عالج في الكبريت زهر يستخدم كما الجلدية األمراض بعض
.الهضم اضطرابات
الكربيت مركبات بع�ض 5 - 3 - 8
الكبريت أوكسيد ثنائي غاز - أ
رئيسي بشكل SO2
الكبريت أوكسيد ثنائي غاز يتولد
الغاز هذا يتصاعد .األوكسجين بوجود الكبريت احتراق من
،البركانية النشاطات جراء من الطبيعة في كبيرة بكميات
تعدين أثناء الصناعية العمليات بعض من كذلك ويتولد
المشتقات لحرق نتيجة وكذلك واستخالصها العناصر بعض
.الحجري الفحم أو النفطية
اضافة من ًامختبري الكبريت اوكسيد ثنائي غاز يحضر
الصوديوم كبريتيت الى المخفف الكبريتيك حامض
ان يمكن الهواء من اثقل ولكونه ])6 - 8( الشكل[ ،Na2
SO3
المعادلة في كما ،االعلى الى الهواء ازاحة طريق عن يجمع
:االتية
اوكسيد ثنائي غاز تولد
احتــــراق مـــــن الكبريــت
.االوكسجين بوجود الكبريت](https://image.slidesharecdn.com/random-161027114933/85/slide-127-320.jpg)

![129
الغاز بهذا المقصورة المواد أغلب أن .])7 - 8( الشكل[
هذا استخدام ويمكن .الهواء إلى تعرضها عند ألوانها تسترجع
الكبريت من كميات حرق طريق عن التعقيم ألغراض الغاز
صناعة في كذلك ويستعمل ،تعقيمها المراد األماكن داخل
.األغذية حفظ
بوجود )400i
o
C( بدرجة ًاتلقائي الكبريت يشتعل أن ويمكن
الرائحة ذو الكبريت أوكسيد ثنائي غاز عنه وينتج األوكسجين
في انطالقه وكثرة ًاجد ضار غاز وهو ])8 - 8( الشكل[ النفاذة
الصناعية األنشطة أو الحجري الفحم حرق نتيجة الهواء
والحيوان اإلنسان على ًاجد سيئة صحية آثار له يكون األخرى
.الحامضية األمطار مسببات أكثر من أنه كما والنبات
H2
S الهيدروجين كبريتيد غاز - ب
ذو اللون عديم غاز هو H2
S الهيدروجين كبريتيد غاز
في يتكون و الفاسد البيض كرائحة نفاذة كريهة رائحة
من او العضوية المواد تحلل :هي طرائق بثالث الطبيعة
في كما الكبريتية المواد على المحتوية الجوفية المياه
من او نينوى محافظة في العليل حمام في الكبريتية العيون
والمنغنيز الحديد تستخدم التي للبكتريا الحيوي النشاط
.غذائها من كجزء
النفطية الغازات في الهيدروجين كبريتيد غاز يوجد
فقد لذا منه %28 على الطبيعي الغاز ويحتوي ،والطبيعية
إنتاج بها يوجد التي المناطق في الهواء تلوث في يتسبب
الممكن من النفط مصافي مناطق في وكذلك الطبيعي للغاز
مركبات على ترتكز التي الصناعات خالل من الغاز ينبعث أن
.الكبريت
بالجهاز المختبر في الهيدروجين كبريتيد غاز يحضر
])6 - 8( الشكل[ SO2
تحضير في استخدم الذي نفسه
مع الكبريتيك حامض مثل المخففة الحوامض تفاعل من
المعادلة وفق )II(الحديد كبريتيد مثل الفلزات كبريتيدات
:اآلتية
تعلم هل
الهيدروجينكبريتيدغازان
خطورة اكثر وهو ًاجد سام
اوكسيد احادي غاز من
.الكاربون
)2 - 8( تمرين
لتفاعل موزونة معادلة اكتب
مع الهيدروجين كبريتيد
ليكون الخارصين كبريتات
كبريتيد من ابيض راسب
.الخارصين
)8 - 8( الشكل
بسهولة الكبريت يحترق
في لالشعال مصدر بوجود
ًامتحد ازرق بلهب الهواء
.الجوي االوكسجين مع
بدرجة ًاتلقائي ويشتعل
الحالتينفيوينتج)400i
o
C(
الكبريت اوكسيد ثنائي غاز
.النفاذة الرائحة ذو](https://image.slidesharecdn.com/random-161027114933/85/slide-129-320.jpg)

![131
والرائحة اللون عديم القوام زيتي سائل الكبريتيك حامض
بجميع الماء في يذوب . 3غم/سم 1.84 تبلغ عالية كثافة وله
عند الحذر يستوجب مما عالية حرارة مولد التراكيز
.تخفيفه
ميال يمتلك حيث مجفف كعامل الكبريتيك حامض يسلك
ذلك ونالحظ العضوية المركبات من الماء النتزاع شديدا
بحامض وعاء في القصب سكر من ملعقة مقدار غمر عند
من سوداء كاربونية مادة بروز سنالحظ ،المركز الكبريتيك
المعادلة حسب السكر تفحم نتيجة ])9 - 8( الشكل[ ،الوعاء
:االتية
H2
SO4
مركز
C12
H22
O11
12C + 11H2
O
القصب سكر كاربون ماء
تحضير لمراحل مخطط
ًاصناعي الكبريتيك حامض
.التالمس بطريقة
لنقـــــل معدنيــــة حاويــــة
حامض من تجارية كميات
.المركز الكبريتيك
)9 - 8( الشكل
الكبريتيك حامض يمتلك
الماء النتزاع ًاشديد ًالمي
العضوية المركبات من
اضافة عند ذلك ونالحظ
المركز الكبريتيك حامض
من مقدار يحتوي بيكر الى
.القصب سكر](https://image.slidesharecdn.com/random-161027114933/85/slide-131-320.jpg)