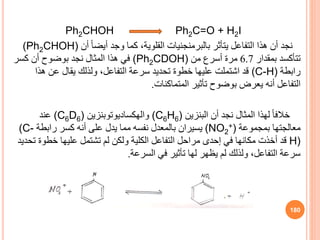
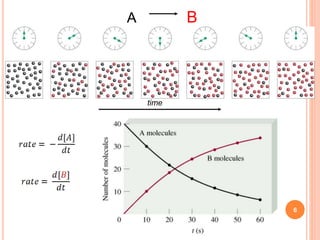
This document discusses the principles of kinetics in physical chemistry, focusing on the rates of chemical reactions and the factors affecting them. It elaborates on concepts such as reactant concentration, temperature, and activation energy, alongside their impact on reaction speeds. Additionally, the document includes examples and equations related to the measurement and comparison of reaction rates.





![(RATE R ) التفاعل سرعة
aA + bB cC + dD
dt
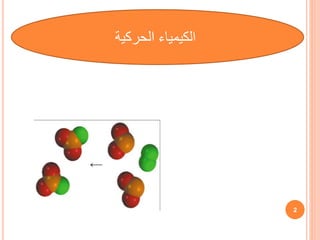
D
d
d
dt
C
d
c
dt
B
d
b
dt
A
d
a
R
]
[
1
]
[
1
]
[
1
]
[
1
9](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-9-320.jpg)
![CH4 (g) + 2O2 (g) CO2 (g) + 2H2O (g)
rate = -
d[CH4]
dt
= -
d[O2]
dt
1
2
=
d[H2O]
dt
1
2
=
d[CO2]
dt
2H2 + O2 2H2O
dt
O
H
d
dt
O
d
dt
H
d
v
]
[
2
1
]
[
]
[
2
1 2
2
2
10
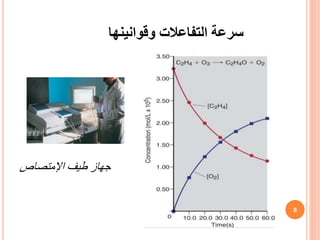
التفاعل سرعة وحدة
(Concentration) (time)-1
هي الشائعة والوحدة
:
mol l-1s-1](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-10-320.jpg)













![28
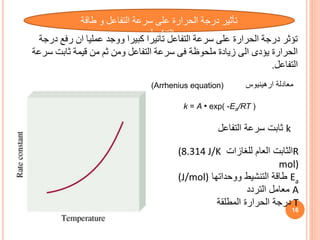
وتعتمد
على أدق أخرى بعبارة أو ،المتفاعلة المواد استهالك أو الناتجة المواد تكون معدل على التفاعل سرعة
ب تعيينه يمكن أس إلى ًامرفوع تركيز كل يكون بحيث التفاعل في المشتركة المواد من مادة لكل التركيز
التجربة
.
وهذا
مثل صحيحة ًاأعداد يكون قد األس
1
،
2
،
3
،
...
التفاعل درجة على األمثلة ومن ،الصحيح الواحد من ًاكسر يكون وقد
اآلتية التفاعالت تدرس
:
1
.
أكسيد خامس تفكك
النيتروجين
2N2O5 → 4NO2 + O2
معادلة
سرعة
التفاعل
-dC(N2O5)/dt = K[N2O5]1
هذا
األولى الدرجة من تفاعل
.
2
.
النيتروجين أكسيد ثاني تفكك
2NO2 → 2NO +O2
هي التفاعل سرعة معادلة
:
-dC(NO2)/dt = K[NO2]2
وهذا
الثانية الدرجة من تفاعل
.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-28-320.jpg)
![29
3
.
ثالثي تفاعل
إيثيل
بروميد مع أمين
االيثيل
البنزين محلول في
:
(C2H5)3N + C2H5 Br (C2H5)4NBr
رباعي بروميد
إيثيل
ثالثي أمين
إيثيل
أمين
التفاعل سرعة معادلة
:
-dC(C2H5Br)/dt = K[C2H5Br] [(C2H5)3N]
ا الدرجة من تفاعل ًاأيض ولكنه الثانية هي الكلية درجته السرعة معادلة من يظهر كما التفاعل هذا
ألولى
بروميد مادة إلى بالنسبة
االيثيل
ثالثي مادة إلى بالنسبة األولى الدرجة من ًاوأيض
إيثيل
أمي
ن
.
4
.
تفكك
االستيالدهيد
درجة عند ،الغازية الحالة في
450
ە
م
.
التفاعل سرعة معادلة
:
CH3CHO CH4 + CO
-dC(CH3CHO)/dt = K[CH3CHO]3/2
أي
هي التفاعل درجة أن
3/2
.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-29-320.jpg)





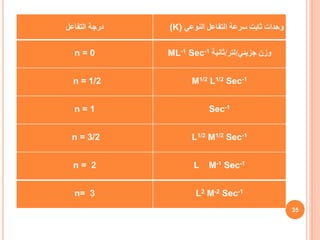



![rate = k [A]0 = k
t½ = t when [A] = [A]0/2
t½ =
[A]0
2k
[A] - [A]0 = -kt
الصفر الرتبة تفاعالت
ية
40
t زمن اى عند المادة [تركيزA]
t=0 الزمن بداية عند المادة [تركيزA]0](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-40-320.jpg)
![األ الرتبة تفاعالت
ولى
a 0 t = 0
a-x x t = t
[A] = (a – x) = a e-kt
األولى للرتبة التفاعل سرعة ثابت وحدة
sec-1
الرتبة احادى لتفاعل العمر نصف فترة
t1/2 = ln2/k 41](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-41-320.jpg)



![وبالتعويض
قيمة عن
K΄
على الحصول يتم
:
- ln (a-x) = Kt –ln a
ln (a/a-x) = Kt
2.303log (a/a-x) = Kt
log (a/a-x) = Kt / 2.303
K = 1/t 1n (a/a-x)
K = [ 2.303 log (a/a-x)] /t
ويمكن
كاآلتي األسية الصيغة في المعادلة وضع
:
X = a (1 – e-Kt)
45](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-45-320.jpg)
![ln[A] = ln[A]0 - kt
46
األ الرتبة تفاعالت
ولى](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-46-320.jpg)


![أ
-
المحلول في األولى الرتبة تفاعالت على أمثلة
:
تحويل
-N
كلورواستتانياليد
بارا إلى
–
كلورو
استتانياليد
:
كالتالي التفاعل معادلة كتابة ويمكن األولى الدرجة من التفاعل هذا يعد
:
ويتابع
ثم ،متفاوتة فترات في التفاعل من متساوي حجم بأخذ التفاعل سير
كل في يضاف
من قياسي بمحلول المتصاعد اليود ويعاير البوتاسيوم يوديد من زيادة مرة
الثي
وكبربتات
،
المركب أن ويالحظ
(
1
)
المركب بينما البوتاسيوم يوديد من اليود يطرد أن يستطيع
(
2
)
ال
ا المواد من الباقية الكميات لتركيز ًاقياس المعايرة تكون وبهذا ،ذلك يستطيع
بينما ،لمتفاعلة
االبتدائ للتركيز ًاقياسي تحويله قبل المحلول من نفسه الحجم معايرة تكون
يمكن ولذلك ،ي
المعادلة باستخدام مرة كل في النوعي التفاعل سرعة ثابت حساب
:
K = [2.303/t] log a/(a-x)
المعادلة أو
log (a/a-x)
= [Kt ]/ 2.303
49](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-49-320.jpg)






![A B
56
المادتان تكون عندما أي ،األول االحتمال حالة في
متساو تركيز ذواتي المتفاعلتان
rate = k [A]2
t زمن اى عند المادة (تركيزa-x)
t=0 الزمن بداية عند المادة (تركيزa)
t½ = t when x = a /2
t½ =
1
a
الرتبة ثنائى لتفاعل العمر نصف فترة](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-56-320.jpg)



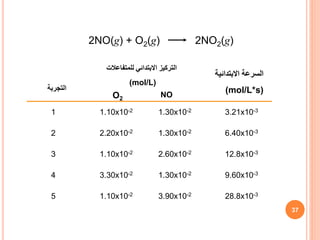
![61
(
2
)
الحمضي الوسط في الهيدروجين أكسيد فوق بواسطة الهيدروجين يوديد حمض أكسدة
:
التفاعل معادلة كتابة يمكن
:
2Hl + H2O2 → l2 + 2H2O
كالتالي خطوات عدة في ويتم الثانية الدرجة من التفاعل هذا
:
l- + H2O → H2O + lO-
H + + lO- → HIO
HlO + H+ + l- → H2O + l2
م كتابة يمكن وعليه ودرجته التفاعل سرعة تحدد التي وهي البطيئة الخطوة هي األولى والخطوة
عادلة
يلي كما التفاعل سرعة
:
[
H2O2
]
[
HI
]
= Rate of reaction = K
R
=
سرعة
التفاعل](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-61-320.jpg)
![62
الكاذبة الثنائية التفاعالت
:
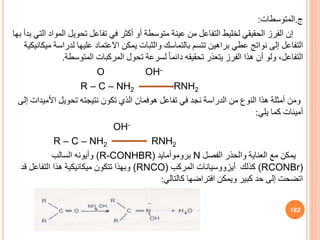
درجت وتتغير خاصة شروط تحت كذلك تكون ولكن ،حقيقة الثانية الدرجة من ليست التي التفاعالت
هذه بتغير ها
تأثير فمثال ،كاذبة ثنائية تفاعالت تسمى الشروط
الكحوالت
من زائدة بكميات العضوية األحماض على
، الكحول
التالية المعادلة في كما
:
R – COOH + R΄ OH → R - COOR΄ + H2O
العضوي الحامض التركيز على تعتمد التفاعل سرعة أن نجد التفاعل هذا في
(
RCOOH
)
هذا أن كما
التف سرعة عن يعبر ولذلك التفاعل أثناء في يتغير وتركيزه ،التفاعل لهذا الحافز بدور يقوم الحامض
كالتالي اعل
:
سرعة
التفاعل
=
ثابت
x
2
[
R - COOH
]
لحظة كل في التفاعل في جزيئين من أكثر مشاركة من بالرغم الثانية الدرجة من فالتفاعل
.
درج فإن التفاعل أثناء يتغير ال ًاثابت تركيزه ويظل الحافز بدور ليقوم معدني حامض بضاف وعندما
التفاعل هذا ة
األولى الدرجة من تصبح
.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-62-320.jpg)

![64
مع النيتروجين أكسيد أول تفاعالت الثالثة الدرجة من الغازية التفاعالت أهم من
األكسجين
أو
البرومين
أ
و
كالتالي التفاعل معادالت وضع ويمكن الكلورين
:
1) 2NO + O2 → 2NO2
2) 2NO + Br2 → 2NOBr
3) 2NO + Cl2 → 2NOCl
هي السابقة للتفاعالت التفاعل سرعة ومعادلة
:
-d(NO) / dt = K(NO)2(X2)
تركيز تمثل حيث
أو األكسجين
البرومين
الكلورين أو
.
عند الثالثة الدرجة للتفاعالت آ قيمة وتعطي
a = b = c
يلي كما
:
K=1/2τ [1/(a-a/2)2 – 1/a2] = 1/2τ.3/a2
τ =3/2 1/Ka2 Sec.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-64-320.jpg)
![65
خامسا
:
العامة الحالة
:
التفاعل درجة تكون عندما أي العامة الحالة في التفاعل درجة إليجاد
(
n
)
المواد أن االعتبار في األخذ مع
التالية الطريقة نتبع األولى تركيزها في متساوية المتفاعلة
:
R α Cn
R = K (a – x )n
dx/dt = K(a-x)n
المتغيرات بفصل
:
dx/(a-x)n= K dt
أن االعتبار في األخذ مع التكامل عملية بإجراء
n ≠ 1
على الحصول يتم
:
∫ dx/ (a- x)n = ∫K dt
1/ (n -1)(a-x)(n-1) = Kt + K΄ (29)
حيث
K΄
يلي كما قيمته استنتاج ويمكن التكامل ثابت
:
at t = o
x = o
K΄ = 1/ (n-1)(a-o)(n-1) = 1/ (n-1) a(n-1)
في قيمة عن وبالتعويض
المعادلة
(
29
)
على نحصل
:
1/ (n-1)(a-x)(n-1) = Kt + (n-1) a(n-1)
K= 1/ t(n-1) [1/ (a-x)(n-1) - 1/a(n-1)]
K΄](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-65-320.jpg)
![66
أن أي الثانية الدرجة من للتفاعل العامة الحالة معادلة وبتطبيق
(
n=2
)
إلى تؤول المعادلة أن نجد
:
K = [1/t ] x/a(a-x) LM-1 Sec-1
أن أي الثالثة الدرجة من التفاعل حالة وفي
(
n=3
)
إلى تؤول أنها نجد
:
K = 1/2t [1/(a-x)2 – 1/a2] L2 M-2 Sec-1
أن أي أنصاف ثالث الدرجة من التفاعل حالة وفي
(
n= 3/2
)
أنها نجد
تؤول
إلى
:
K = 2/t [1/ (a -x)1/2 - 1/a1/2] L1/2 M-1/2 Sec-1
أن أي أنصاف ثالث الدرجة من التفاعل حالة وفي
(
n= ½
)
أنها نجد
تؤول
إلى
:
K = 2/t [ a½ - (a –x) ½]M½. L-½ .Sec-1](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-66-320.jpg)


![69
[A]t
t / s
اإلبتدائية السرعة
التف وثابت رتبة تعيين
اعل
وتطب
التفاضلية الطريقة
مختلفين وجهين على
1
-
اإلبتدائية السرعة طريقة
.
(Initial rate method)
مخت ابتدائية تراكيز باستخدام مرات عدة التفاعل باجراء
وتعيين لفة
فى الزمن مع التركيز تغير بقياس اإلبتدائية السرعات
تجربة كل
المعادلة وتطب](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-69-320.jpg)

![Br2 (aq) + HCOOH (aq) 2Br- (aq) + 2H+ (aq) + CO2 (g)
السرعة متوسط= -
D[Br2]
Dt
= -
[Br2]2 – [Br2]1
t2 – t1
المماس ميل
المماس ميل
المماس ميل
اللحظية السرعة
=
معينة لحظة عند السرعة
71](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-71-320.jpg)
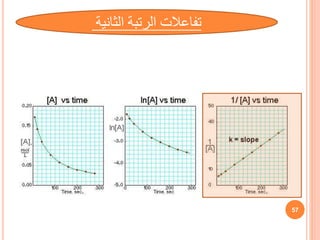
![ln[A]t = -kt + ln[A]0
1/[A]t = kt + 1/[A]0
[A]t = -kt + [A]0
الطريقة
التكاملية
إليجاد
رتبة
التفاعل
73](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-73-320.jpg)
![74
time
concentration
[A]0
[A]0/2
[A]0/4
[A]0/8
t1/2
t1/2
t1/2
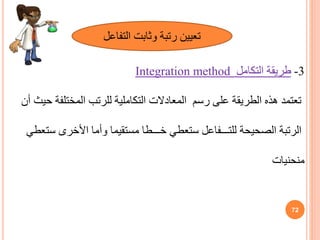
التف وثابت رتبة تعيين
اعل
4
-
النصف عمر طريقة
Half –life period)
)
تركيز نصف إلختفاء الالزم الزمن قياس على الطريقة هذه تعتمد
المواد
المتفاعلة](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-74-320.jpg)
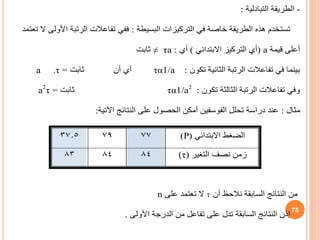











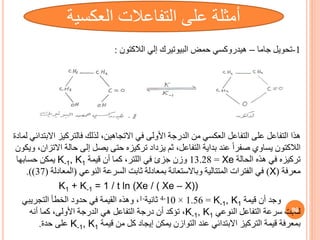
![dx/dt = K1 (a – Xe ) – K-1 Xe = 0 (34)
K-1 = K1 (a – Xe ) / Xe (35)
قيمة عن وبالتعويض
K-1
السرعة معادلة في
(
معادلة
33
)
أن ينتج
:
dx / dt = K1 (a – X ) – K-1(a – Xe) / Xe .X
dx / dt = [K1 a/Xe] (Xe – X )
بتكامل
في األخذ مع المعادلة
االعتبار
أن
X
=
عندما أي التفاعل بداية عند صفر
t = 0
على الحصول يتم
:
K1 = (Xe / a t) ln [Xe /( Xe – X)] (36)
قيمة عرفت فإذا
Xe
أمكن
قيمة حساب
K1
قياس من
(
X
)
متتالية فترات في
.
ًاوأحيان
المعادلة فان هذا وعلى آخر شكل في التفاعل سرعة ثابت معادلة توضع الموازنة لغرض
(
35
)
أن يمكن
التالية الصورة على توضع
:
K-1 .Xe = K1 ( a – Xe)
= K1a – K1. Xe
93](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-93-320.jpg)
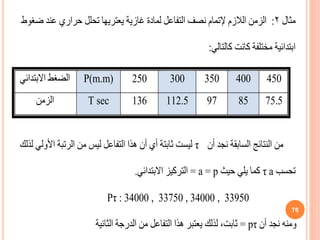
![( K-1 + K1) Xe = K1. A
Xe / a = K1 / (K-1 + K 1 )
بالتعويض
قيمة عن
Xe / a
المعادلة في
(
36
)
أن ينتج
:
]
K1 = (K1 / K1 + K-1 ) / t ln [ Xe / ( Xe – X)
Or
K1 + K-1 = 1/t ln [Xe / ( Xe – X ) ] (37)
بمقارنة
وصيغتها األولى الدرجة بمعادلة المعادلة هذه
:
K = 1/ t ln a / ( a-x )
التالي التشابه يتضح
:
التركيز
االتزان حالة في
Xe
االبتدائي التركيز محل حل
a
األولى الدرجة معادلة في
.
مجموع
االتجاهين في التفاعل سرعة ثابتي
(
K1 + K-1
)
النوعي التفاعل سرعة ثابت محل حلت
K
.
94](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-94-320.jpg)


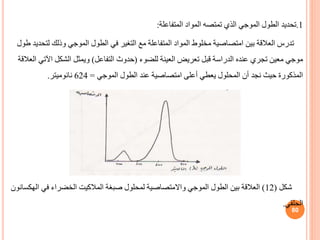
![المعادلة في وبالتعويض
(
41
)
أن ينتج
:
(1 / B ) ln (A + BX) = t + (1 / B ) ln A
(1 / B ) ln (A + BX) – (1 / B) ln A = t
بالتعويض
قيمة عن
(
1 / B
)
أن ينتج السابقة المعادلة في
:
( -1 / K1 + K-1 ) ln ( A + BX ) + (1 / K1 + K-1 ) ln A = t
(1 / t) ln A/ ( A + BX) = K1 + K-1
بقسمة
المقدار على األيسر الطرف في والمقام البسط
B
أن ينتج
:
( 1 / t) ln A/B /(A/B + B/B X) = K1 + K-1
قيمة عن بالتعويض
A/B
(
39
)
أن ينتج
:
1/t ln [ - Xe/ (-Xe +X) ] = K1 + K-1 (42)
1/t ln (+ Xe/ (Xe – X) ) = K1 + K-1
والمعادلة
(
42
)
لها
المعادلة شكل نفس
(
37
)
الحالة تمثل التي
(
أ
)
التركي قيمة في كان االختالف ولكن
ز
Xe
االتزان حالة في
.
97](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-97-320.jpg)


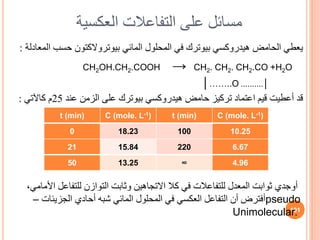
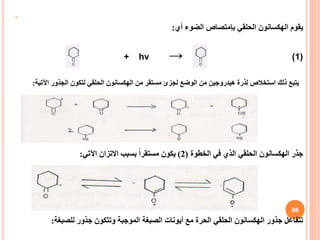
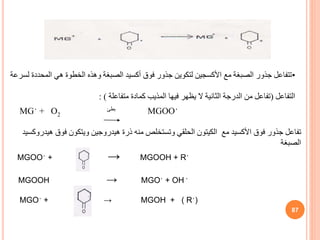
![هناك تكون وقد ، الح لتفاعل متفاعلة مادة نفسه هو ما ناتج يصبح أن يحدث ما ًاكثير
المتتابعة الخطوات من مجموعة
أى
ليعطي بعض مع بعضها يتفاعل التفاعل نواتج أن
وهكذا أخرى نواتج
..
الت التفاضلية للمعادالت حل إيجاد فقط الحاالت أبسط في أمكن وقد
ي
عمليات في والسيما ًاجد مهمة المتتابعة والتفاعالت ،التفاعل من النوف هذا تمثل
البلمر
ة
Polymerization.
ومن
على األمثلة ابسط
هذا
من المتعاقبة التفاعالت تكون أن التفاعالت من النوف
مع األولى الدرجة
وعليه عكسية تفاعالت وجود عدم
معادلة وضع يمكن
التفاعل
يلي كما
A K1 B K2 D
حيث
K1
،
K2
كانت فإذا ، النوعي التفاعل ثوابت هي
CD, CB, CA
للمواد التركيز تمثل
D, B, A
المتفاعلة للمادة بالنسبة التفاعل سرعة معادلة فإن التوالي على
A
هي
- d CA / dt = K1 CA = K1 [A]
.
التفاعالت
المتتابعة](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-103-320.jpg)
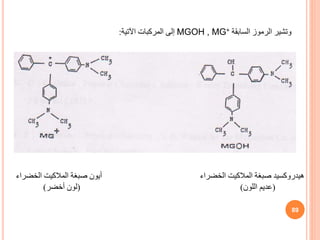
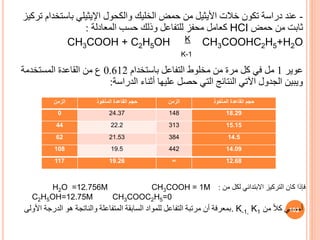
![وبتكامل
ينتج المعادلة
:
K1 = 1/t ln (a/ Ca
Or
K1. t = ln a – ln CA
الطرفين لن بأخذ
:
CA = a. ē K1t (46)
المادة لتكون التفاعل سرعة ومعادلة
D
هي
:
- dC / dt = K2 CB = K2 [B] (47)
محصلة
المادة لتكوين التفاعل سرعة
B
المادة من لتكوينها التفاعل سرعة عن عبارة
A
تفاعلها سرعة ًاناقص
المادة لتعطي
D
كالتالي وهي
:
d [B] / dt = K1 . CA – K2 CB (48)
قيمة عن بالتعويض
CA
المعادلة من
(
46
)
أن ينتج
:
d [B] / dt = K1ae –K1t – K2 CB
104](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-104-320.jpg)
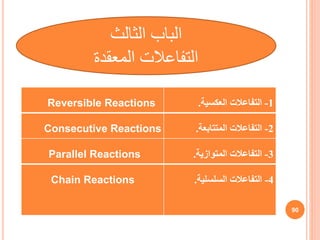
![القيمة في السابقة المعادلة طرفي بضرب
e k2t
أن ينتج
:
d [B] / dt .e K2t = K1ae (K2- K1)t – K2 CB. e K2t
:.d [B] / dt. e K2t + K2 CB. eK2 = K1 a e (K2 - K1)t
حاصل
وعليه ، دالتين ضرب
:
d / dt (e K2t . CB) = K1 a e (K2 - K1)t
بتكامل
أن ينتج السابقة المعادلة
:
∫d( e K2t. CB ) = ∫ K1ae (K2 – K1) t dt
:. e K2t. CB = K1 / K2 – K1 ae (K2 – K1) t + K΄
التكامل ثابت قيمة إليجاد
K΄
المعادلة طرفي نقسم
e K2t
على نحصل وبذلك
:
CB = K1a / ( K2 – K1) ē K1t + K΄ ē K2t (49)
105](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-105-320.jpg)
![التفاعل بداية عند
أى
عند
t
=
فإن ، صفر
CB = 0
.:
المعادلة في بالتعويض
(
49
)
أن ينتج
:
CB = K1a / ( K2 – K1 ) .e –K1xo + Kَ e-K2 xo = o
:. Kَ = - K1a / ( K2 – K-1 )
بالتعويض
K΄
المعادلة في
(
49
)
بقيمتها
نجد
أن
:
CB = K1a / ( K2 – K-1 ) e-K1t - K1a / ( K2 – K-1 ) e-K2t
CB = K1a / ( K2 – K-1 ) (e-K1t - e-K2t ) (50)
فإن
قيمة عرفت
K2 , K1
قيمة إيجاد السهل من أصبح
CA , CB , CD
زمن مرور بعد
=
t
على
قيمة تعيين يمكن حيث ،التفاعل
CA
المعادلة من
(
46
)
المادة وتركيز
CB
المعادلة من
(
50
)
أما ،
قيمة
CD
االبتدائي التركيز بمعرفة حسابها فيمكن
a
العالقة من
:
a = CA + CB + CD
عند
من كل تركيز بين العالقة دراسة
[
A
]
,
[
B
]
,
[
D
]
الزمن مع
الشكل على تحصل
المبين
: 106](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-106-320.jpg)
![107
والشكل
(
3
)
أن يوضح
[
B
]
التركيز بينما ينقص ثم القمة إلى يصل حتى يزداد
[
A
]
والتركيز ،التفاعل فترة طوال ينقص
[
D
]
يزداد
باستمرار
حتى
التفاعل نهاية
.
الــــزمــــن
تجزؤ التفاعل من النوف هذا على األمثلة ومن
األستيون
ا والمركب الميثان إلى الحرارة بتأثير
لمتوسط
عل التفاعل معادالت وضع ويمكن وااليثلين الكربون اكسيد إلى بدوره يتجزأ الذي الكيتين
التالي النحو ى
:
( CH3 )2 C = O → CH4 + CH2 = C = O → [ 1/2 C2 H4 + C = O]
كيتين
المتوسط المركب تركيز
(
الكيتين
)
الحقيقة وفي ،ينقص ثم القمة إلى يصل حتى يزداد
تجزأ إن
األستيون
المعادالت إليه تشير مما ًاتعقيد أكثر الحرارة بتأثير
.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-107-320.jpg)





![ولما
المادة تكوين معدل كان
B
هو
:
d [B] / dt = [B] = K1 ( a – x )
المادة تكوين ومعدل
D
هو
:
d [D] / dt = [D] = K2 ( a – x )
d [B] / d [D] = K1 / K2 = [B] / [D] ثابت
=
المادة تركيز (54)
أي
المادة التركيز بين النسبة أن
B
المادة تركيز إلى
D
مقدار يساوي لحظة أي في
الناتجة للمواد بالنسبة واحدة التفاعل درجة تكون أن بشرط ثابت
.
113](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-113-320.jpg)

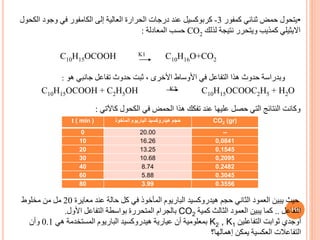



![وقد
تتص الهيدروجين ذرات و البروم ذرات من ًالك أن التفاعل هذا في افترض
رف
أ ذرات بواسطة الهيدروجين ذرات من كبير عدد توليد يتم أنه كما ،وسطية كحاالت
و
سرعة لحساب يزداد سوف التفاعل في الناقالت عدد فإن وبذلك البروم جزيئات
التفاعل
ت الثابتة الحالة بافتراض فإنه التفاعل خطوات سرعة ثوابت ضوء على الكلي
الحاالت كون
أن أي ثابت تركيز ذات التفاعل سير أثناء الوسيطة
:
d [Br] / dt = 0 d [H] / dt = 0
التفاع سرعة حساب يمكن المقترحة التفاعل خطوات ومن الفرض هذا ضوء وعلى
ل
يلي كما الكلية
:
d[Br] /dt = K1[Br2] - K2[Br][H2]+ K3[H][Br2]+K4 [H][HBr] – K5[Br]2 = 0
d[Br]/dt =K1[Br2]–{K2[Br][H2] - K3[H][Br2]-K4 [H][HBr]} – K5[Br]2 = 0 (6)
كذلك
:
d[H] /dt = K2[Br] [H2]- K3[H][Br2]-K4 [H][HBr] =0 (7)
المعادلة من وبالتعويض
(
7
)
المعادلة في
(
6
)
أن ينتج
:
d[Br] /dt = K1[Br2] – 0 – K5 [Br]2 = 0
119](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-119-320.jpg)
![ومنه
:
[Br˙]2 = K1 / K5 [Br2]
[Br] = ( K1 / K5 )½ [Br2]½ (8)
المعادلة في بالتعويض كذلك
(
7
)
بقيمة
(
Br
)
المعادلة من
(
8
)
على الحصول يتم
:
[H] = K2 ( K1 / K5 )½ [H2] [Br2]½ / K5 [Br1] + K4 [HBr]
الهيدروجين بروميد تكوين معدل على الحصول ويمكن
HBr
المعادالت من
(
2
)
،
(
3
)
،
(
4
)
كما
يلي
:
d[HBr] / dt = K2 [Br][H2] + K3[H][Br2] – K4[H][HBr] (9)
قيمة عن بالتعويض
(
Br
)
و
(
H
)
المعادلة في
(
9
)
على الحصول يتم
:
d[HBr] /dt = 2K2 (K1 / K5)½ [H2][Br2]½ / 1+K4 [HBr] / K3 [Br2] (10)
اآلتية الصورة على المعادلة هذه كتابة ويمكن
:
d[HBr] /dt = K [H2][Br2]½ / 1+ [HBr] / Ḱ[Br2] (11)
حيث
:
2K2 ( K1 / K5 )½ تساوي K
K3 / K4 تساوي
Ḱ 120](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-120-320.jpg)

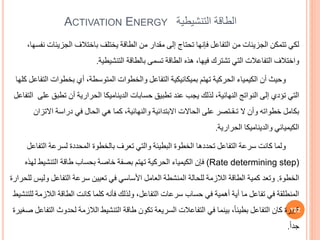
![إال لها ليس المنشطة الجزيئات ألن المسعر باســتخدام مباشرة التنشيط حرارة قياس يمكن وال
قصير وجود
برسم وذلك ،مباشرة غير بطريقة تعين ولكنها ،ًاجد
log K
مقابل
1/T
بمقدار الميل وضرب
(2.303 R)
برسم التفاعل حرارة بها تعين التي نفسها بالطريقة أي
log K
مقابل
1/T
حيث
K
االتزان ثابت هو هنا
ويساوي
Kf /Kr
(
والعكسي الطردي االتجاه في التفاعل ثابتي بين النسبة
)
فانت معادلة ومن
هو
ف
:
d (ln K)/dT = ΔHº/RT2
حيث
ΔHº
وبتك المتغيرات بفصل ،القياسية الحالة في المتفاعلة للمواد التنشيط طاقة هي
المعادلة هذه امل
على الحصول يتم التكامل ثابت وحساب
:
ln K= ΔHº/RT + ln Kα
حيث
α
ln K
وتساوي التكامل ثابت هي
(Kf)α/ (Kr)α
(
والعكسي الطردي التفاعل ثابتي بين النسبة
في
المطل الصفر عند القياسية الحالة
.)
ولكن
:
ΔHº = HºP -HºR
حيث
HºP
الناتجة للمواد الكلية الحرارة هي
.
HºR
المتفاعلة للمواد الكلية الحرارة هي
.
من كل عن بالتعويض
Kα ,K, ΔHº
المعادلة في
(
55
)
أن ينتج يساويهم بما
:
]
ln Kf/Kr = -(HºP-HºR/RT) + ln[(Kf) α/(Kr) α
Or
ln Kf/(Kf) α - HºR/RT = ln Kr/(Kr) α - HºP/RT (56)
123](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-123-320.jpg)







![التصادم نظرية تطبي
:
جزيئات ثالثة بين التفاعل
:
لدراسة
التفاعال في والسيما التصادم نظرية ضوء على جزيئات ثالثة بين التفاعل
المعروفة ت
النترو أكسيد ثاني لتكوين واألكسجين النتروجين أكسيد أول بين التفاعل يدرس
معادلة ،جين
هي التفاعل
:
2NO + O2 2NO2
هي التفاعل سرعة ومعادلة
:
-dC[O2 ]/dt = K[NO]2[O2]
حيث
K
التفاعل سرعة ثابت هو
[O2] [NO]
على واألكسجين النتروجين أكسيد تركيز هما
التوالي
.
أو من جزيئين تصادم يتطلب وأنه أولي تفاعل أنه معادلته من يبدو كما التفاعل هذا
أكسيد ل
س أن وهي النظر تلف بظاهرة يتمتع التفاعل هذا ولكن األكسجين من جزئ مع النتروجين
رعة
تش التي التفاعالت من قليل وهناك ،التفاعل حرارة درجة في بالزيادة تنقص تفاعله
هذه في ارك
الظاهرة
. 132](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-132-320.jpg)

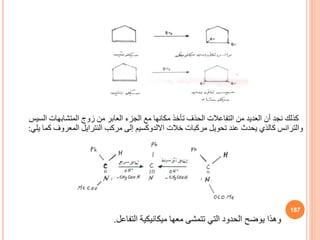
![يلي كما التفاعالت من النوف لهذا بديلة ميكانيكية افتراض تم وقد
:
يحدث
ًالأو التالي التوازن
:
NO + X2 NOX2
حيث
X2
هي الخطوة هذه سرعة معادلة ، آخر غاز أي أو األكسجين تمثل
:
d(NOX2)/dt = K1[NO] [X2]
حيث
K1
التفاعل ذلك يتبع الخطوة لهذه السرعة ثابت هي
البطئ
اآلتي
:
NOX2 + NO
2NOX
هي النهائية السرعة ومعادلة
:
R=K2[NO][NOX2]
=K2K1[NO]2[X2] = K[NO]2 [X2]
ال تتبعه الذي التوازن أن الواضح ومن التفاعل سرعة معادلة االعتبار ي تأخذ الميكانيكية وهذه
البطيئة خطوة
كالتالي يكون ان يمكن
:
2NO N2O2
N2O2 + X2 2NOX 134](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-134-320.jpg)




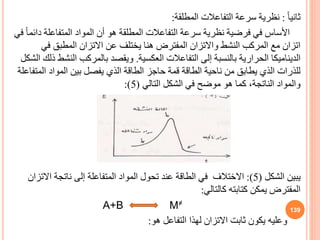

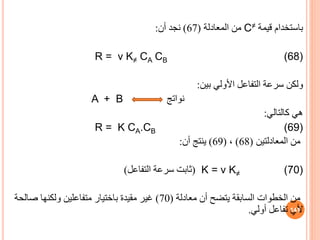




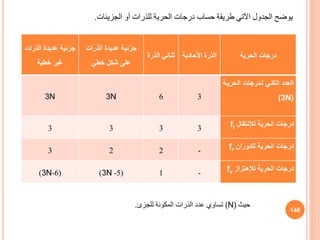









![المح هي التي المرجع حالة على يدل التنشيط معامل قوس في المذيل والصفر
لول
المعاد تصبح المخفضة المحاليل استخدام عند ولكن ، نهاية ماال إلى المخفف
لة
:
K = Ko(vA.vB/v≠) (89)
المعادلة
(
89
)
بواسطة ًالأو اشتقت
برونشتيد
نظرية تطبي قبل وبيرم
التفاعالت
المعاد لطرفي الطرفين لوغاريتمات بأخذ ،األيونية التفاعالت على المطل
أن نجد لة
:
log K = logK0 + logvA+ logvB - logv≠ (90)
معادلة من ولكن
ديبى
-
حيث التنشيط لمعامل هيكل
:
log vi = - 0.5Zi
2√I
حيث
Z
األيون شحنة هي
I , i
المعادلة من قيمتها وتعطي األيونية القوة هي
:
I = 1/2 ∑i Zi
2 Ci
المعادلة في الفعالية معامل قيمة عن بالتعويض
(
90
)
أن ينتج
:
log K = logK0 – 0.5√I [ZA
2 + ZB
2-(ZA+ZB)2]
حيث
:
ZAB = (ZA + ZB) 156](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-156-320.jpg)
![ومنه
:
logK = logK0 - 05√I [-2ZA.ZB]
= logK0 + ZA.ZB√I
logK/K0 = ZA.ZB√I (91)
العالقة برسم
بين
(
log(K/K0
األيونات لقوة التربيعي والجذر
(I)
الحصول يتم فإنه
في
يساوي ميله مستقيم خط على المخففة المحاليل
ZA ZB
.
وإش قيمة علــى تعتمد التفاعل سرعة ثابت قيمة أن الـعالقة هذه توضح كــما
ارة
تمي يمكن السلوك من أنواف ثالثة فهناك وعليه المحلول في الموجودة األيونات
يزها
:
1
-
عندما
تكون
ZA ZB
التفاعل سرعة ثابت قيمة فإن موجبة
K
زيادة مع تزداد سوف
بالمحلول الموجودة لأليونات األيونية القوة
.
2
-
عندما
تكون
ZA ZB
التفاعل سرعة ثابت قيمة فإن سالبة
K
القوة زيادة مع تقل سوف
األيونية
(I)
.
3
-
عندما
تكون
ZA ZB
=
قيمة فإن ًاالنهائي المخففة المحاليل في صفر
(K)
تتأثر ال
األيونات بتركيز
.
157](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-157-320.jpg)

![ZAZB=4
[C8(NH3)5Br]2+ + Hg2+
I
ZAZB=2
S2O8
2- + I-
II
ZAZB=1
NO2NCO2C2H5
-+I-
III
ZAZB=0
C12H22O11+OH-
IV
ZAZB=-1
H2O2+H+ +Br-
V
ZAZB=-2
[Co(NH3)5Br]2+ +OH-
VI
159
نتي أنه هو والمختلفة المتشابهة الشحنات حاالت في السلوك لهذا الفيزيائي التفسير
النسبية الشحنة جة
للرمز االسية القيمة مع تنخفض التنشيط معامل قيمة فإن ،النشط المركب على
Z2
كانت فإذا ،
جميع
األيونات
إذا عالية النسبية شحنته تكون النشط المركب فإن تشابهه شحنات لها
م
اوزنت
بأي
أن يعني وهذا ،األخرى الشحنات من واحدة
v≠
والنسبة ،ًاجد صغيرة
vA.vB/v≠
عالية تكون
.](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-159-320.jpg)

![.
للتفاعل األيونية القوة على األيوني التفاعل معدل اعتماد
:
[CoBr(NH3)5]+2 +OH- = [Co(NH3)5]+2 +Br- (1)
من كل أعطي
برونشتد
J.R.Bronsted
وليفنتون
R.Livingston
ثابت قيمة
عند المعدل
15
º
بالمقدار م
:
لتر
.
مول
-
1
.
دقيقة
K=91
يكون عندما التجربة خالل مقاسه
األصلي التركيز
لأليون
[CoBr(NH3)5]+2
(
بروميد بشكل الموجود
)
0.5x10-3M
،
ايون تركيز وكان
OH-
0.705x10-3M =
،
هذه من
النتائج
أحسبي
:
(
أ
.)
للتفاعل المعدل ثابت
(
1
)
نهاية ماال إلى التخفيف عند التفاعل تم إذا
(
ب
)
ا ثابت
لمعدل
وج وفي المتفاعلة األيونات من لكل المختلفة التراكيز عند المذكور للتفاعل
كميات ود
المع مع النتائج قارني التالي الجدول في هو كما الصوديوم كلوريد من مختلفة
لومات
السابقين الباحثين بواسطة ًاعملي عليها المحصل
(
الجدو في حقل آخر أنظري
ل
.)
I=2.2x10-3 , log ko=2.052 , k0=113L.M-1min-1
[Co Br(NH3)5]+2 + OH- = [Co(NH3)5]+2 +Br-
161
مســــائل](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-161-320.jpg)
![القياس CA.103 CB.103 CNaCl K I
1 0.596 1.004 - 89 2.2x10-3
2 0.600 0.696 0.005 76 75x10-3
3 0.600 0.696 0.020 56 22.5x10-3
4 0.600 0.691 0.00 49 32.5x10-3
162
A + B → C + D
I =1/2[C1x 12 +C1x12] +1/2[CAx22 +2CAX12] +1/2[CBX(1)2 +CBX12]
=1/2[2C1 ] + 1/2[4CA+2CA] +1/2[2CB] =1/2[2CI+6CA+2CB]=C1+3CA+CB)](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-162-320.jpg)










![4
.
التفاعل لسرعة المحددة والخطوة الحركية الطاقة
:
النات المواد ظهور معدل أو المتفاعلة المواد اختفاء معدل بفحص التفاعل معدالت قياس يمكن
عند جة
معينه حرارة درجة
(
ثابتة
)
ال في المشتركة المواد أحد تركيز إلى هذا ينسب أن وراء ًاسعي وذلك
أو تفاعل
جميعها
.
والقيا الطيفي والقياس الحجمي بالتحليل المعايرة مثل طرق بعدة التفاعل تتبع ويمكن
وغير اللوني س
ذلك
..
مختلف عند الخام الحركية الطاقة بيانات أو معلومات اختبار تتضمن القاطعة الخطوة ولكن
مراحل
فالت ومعقولة مقبولة نتيجة على الحصول إلى النهاية في األمر يصل حتى الممكنة التركيز
اآلتي فاعل
..
CH3Br + OH- CH3OH+Br
إل بالنسبة األولى الدرجة ومن الكلية التفاعل إلى بالنسبة الثانية الدرجة من التفاعل هذا
بروميد من كل ى
وأيون
الهيروكسيد
حيث ،
K
التفاعل سرعة ثابت هي
.
R= K [CH3 – Br] [OH-]
في
تحديد معادالت أن نجد األحيان أغلب
إتحاد
للتع ًامناسب ًامرشد ليست الكيميائية المواد
المواد على رف
ال في كما القلوي الوسط في األسيتون برومه تفاعل في ًالفمث التفاعل سرعة في المؤثرة
معادلة
:
OH-
CH3 – C – CH3 + Br2 CH3COCH2Br + HBr
O
تكون
الساب التفاعل سرعة معادلة
:
R =K[CH3COCH3][OH-]
الظاهر في البروم أن أي
يؤثر ال
ال البروم أن الواضح ومن ،المحلول قلوية هو التفاعل سرعة في
وأن بد
النهائي الناتج في مندمجة تكون المادة هذه أن حيث اإلجمالي التفاعل مراحل بعض في يدخل
CH3COCH2Br
التفاعل سرعة ًالفع تقاس التي المرحلة في داخلة غير ولكنها
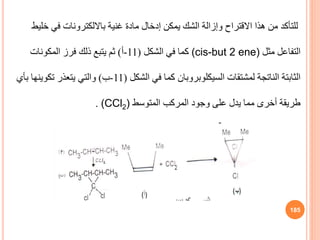
. 173](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-173-320.jpg)


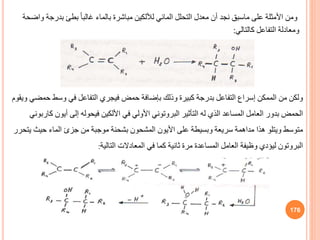

![للهاليدات المائي التحليل كذلك
األلكيل
Rx
اآلتية التفاعل سرعة معادلة تتبع أنها وجد
:
R = K[R-X]
اش تشمل ال التفاعل سرعة تحديد خطوة أن إلى الوصول الضروري من فليس وعليه
تراك
حال في ألنه ذلك التفاعل سرعة معادلة في يظهر لم الماء أن هو بسيط أساس على الماء
ة
لم أو اشترك سواء يذكر تغيير بدون ًالفع سيبقى تركيزه فإن كمذيب استخدام
في يشترك
للسرعة المحددة الخطوة
.
م باستخدام التفاعل إجراء فيمكن الماء دور توضيح ويمكن
آخر ذيب
حمض ًالمث
الفورميك
(H-COOH)
،
فيلية كنواة ًاجد قليل بتركيز الماء ويضاف
(Necleo Phile)
كالتالي تكون التفاعل سرعة معادلة أن نجد وعندها
:
R = K[R-X] [H2O]
غير
المذي بتغير تتغير أن الممكن من التحلل لتفاعل الواقعية الميكانيكية أن
من فليس ولهذا ب
المائي المحلول في حدث ما كيفية على التركيز الضروري
.
الت أن نجد ولذلك محاليل في إجراؤها يتم العضوية للتفاعالت العظمى الغالبية
غيرات
وميكانيكيت التفاعل سرعة في عمي تأثير لها يكون المذيب في ًاجد البسيطة
المركبات والسيما ه
من غمدها معها تحمل عادة المركبات هذه األيون أزواج مكونات مثل القطبية المتوسطة
التفاع أن نجد وبهذا استقرارها في ًاكثير يؤثر أن شأنه من والذي المذيب جزيئات
بقوة يتأثر ل
ال والقدرات قطبية ناحية من والسيما وطبيعته المستخدم المذيب بتركيب كبيرة
بالتذاوب متصلة
األيوني
.
178](https://image.slidesharecdn.com/8797456897874-210212145257/85/Kinetic-Chemistry-178-320.jpg)