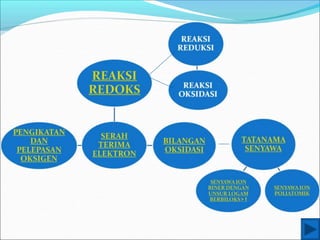
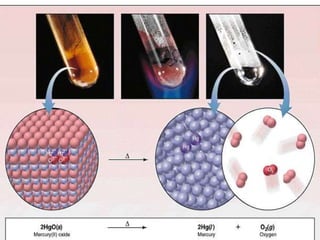
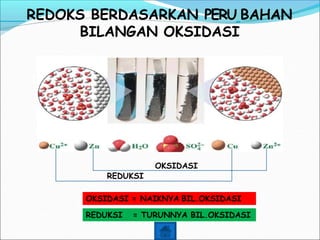
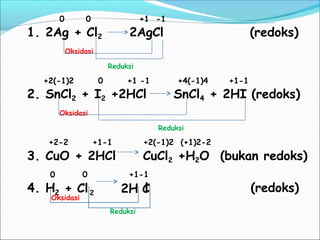
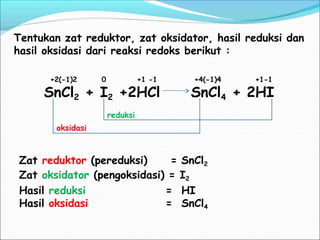
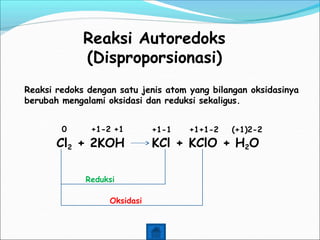
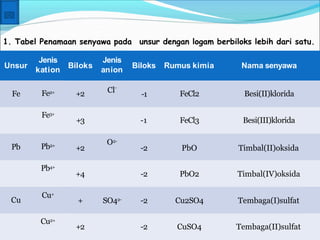
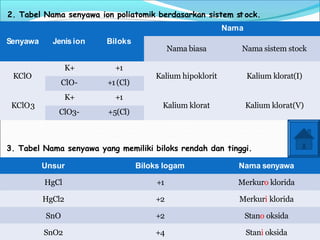
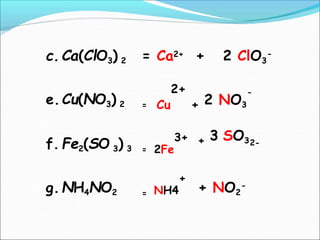
Reaksi redoks merupakan gabungan dari dua reaksi, yaitu reaksi oksidasi dan reduksi. Reaksi redoks berdasarkan perpindahan elektron di mana oksidasi melepaskan elektron dan reduksi mengikatkan elektron. Bilangan oksidasi dapat digunakan untuk menentukan apakah suatu zat mengalami oksidasi atau reduksi. Reaksi redoks terjadi dalam berbagai proses alam sekitar dan industri.