Ppt mbs
•Download as PPT, PDF•
0 likes•413 views
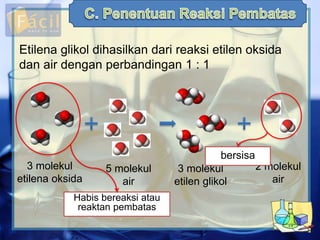
Etilena glikol dihasilkan dari reaksi etilen oksida dan air dengan perbandingan 1:1 yang menghasilkan 3 molekul etilena glikol dan 2 molekul air sisa. Logam besi 28 g bereaksi dengan oksigen 48 g menghasilkan besi oksida (Fe2O3) sebesar 40 g dan oksigen sisa 36 g.
Report
Share
Report
Share
Recommended
PPT Rumus Empiris dan Rumus Molekul

Dalam ppt ini membantu menjelskan materi rumus empiris dan rumus molekul. semoga bermanfaat
Reaksi Reaksi Kimia

ini adalah tugas mata kuliah Kimia dan Pengetahuan Lingkungan Industri semester 1 pada bab dasra-dasar ilmu kimia
Ar, Mr dan Persamaan Reaksi

media pembelajaran kimia (ppt + video) materi Ar, Mr dan Persamaan Reaksi
Kd meeting 3 (stoikiometri)

Materi kuliah kimdas tentang stoikiometri. Cari lebih bayak lagi materi kuliah semester 1 di:
http://muhammadhabibielecture.blogspot.com/2014/12/kuliah-semester-1-thp-ftp-ub.html.
More Related Content
What's hot
PPT Rumus Empiris dan Rumus Molekul

Dalam ppt ini membantu menjelskan materi rumus empiris dan rumus molekul. semoga bermanfaat
Reaksi Reaksi Kimia

ini adalah tugas mata kuliah Kimia dan Pengetahuan Lingkungan Industri semester 1 pada bab dasra-dasar ilmu kimia
Ar, Mr dan Persamaan Reaksi

media pembelajaran kimia (ppt + video) materi Ar, Mr dan Persamaan Reaksi
What's hot (18)
Penetapan kadar ca dalam ca co3 cara substitusi (11 1, alfa kelompok 4) asli

Penetapan kadar ca dalam ca co3 cara substitusi (11 1, alfa kelompok 4) asli
Similar to Ppt mbs
Kd meeting 3 (stoikiometri)

Materi kuliah kimdas tentang stoikiometri. Cari lebih bayak lagi materi kuliah semester 1 di:
http://muhammadhabibielecture.blogspot.com/2014/12/kuliah-semester-1-thp-ftp-ub.html.
Kumpulan materi un sma kimia versi 1 [edukasicampus.net]![Kumpulan materi un sma kimia versi 1 [edukasicampus.net]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Kumpulan materi un sma kimia versi 1 [edukasicampus.net]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Kumpulan materi un sma kimia versi 1 [edukasicampus.net]
Stoikiometri Larutan

Cara perhitungan stoikiometri dalam larutan untuk menetapkan kosentrasi dan massa senyawa dalam reaksi.
Similar to Ppt mbs (20)
Kumpulan materi un sma kimia versi 1 [edukasicampus.net]![Kumpulan materi un sma kimia versi 1 [edukasicampus.net]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Kumpulan materi un sma kimia versi 1 [edukasicampus.net]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Kumpulan materi un sma kimia versi 1 [edukasicampus.net]
2014 - SKL Kimia dan contoh soal serta pembahasannya

2014 - SKL Kimia dan contoh soal serta pembahasannya
More from olanascorepta
More from olanascorepta (20)
Recently uploaded
Modul Projek - Modul P5 Kearifan Lokal _Menampilkan Tarian Daerah Nusantara_...

Modul p5 yang bisa menjadi referensi
Laporan Kegiatan Pramuka Tugas Tambahan PMM.pdf

Laporan Kegiatan Pramuka Tugas Tambahan untuk pengisian di aplikasi PMM
ppt landasan pendidikan Alat alat pendidikan PAI 9_

halowww teman temann selamat membaca, semoga ilmunya bermanfaat. jika ada kekurangan kata atau kehilafan mohon di maaf kan sekian 🤩🥳
Seminar: Sekolah Alkitab Liburan (SAL) 2024

Apakah program Sekolah Alkitab Liburan ada di gereja Anda? Perlukah diprogramkan? Jika sudah ada, apa-apa saja yang perlu dipertimbangkan lagi? Pak Igrea Siswanto dari organisasi Life Kids Indonesia membagikannya untuk kita semua.
Informasi lebih lanjut: 0821-3313-3315 (MLC)
#SABDAYLSA #SABDAEvent #ylsa #yayasanlembagasabda #SABDAAlkitab #Alkitab #SABDAMLC #ministrylearningcenter #digital #sekolahAlkitabliburan #gereja #SAL
Modul Ajar PAI dan Budi Pekerti Kelas 2 Fase A Kurikulum Merdeka

Modul Ajar PAI Dan Budi Pekerti Kelas 2 Fase A Kurikulum Merdeka - abdiera.com
INSTRUMEN PENILAIAN PRAKTIK KINERJA KS Dok Rating Observasi (1).docx

INSTRUMEN PENILAIAN PRAKTIK KINERJA KS Dok Rating Observasi (1).docx
Patofisiologi Sistem Endokrin hormon pada sistem endokrin

membahas tentang patofisiologi sistem endokrin
Recently uploaded (20)
813 Modul Ajar KurMer Usaha, Energi, dan Pesawat Sederhana (2).docx

813 Modul Ajar KurMer Usaha, Energi, dan Pesawat Sederhana (2).docx
NUMERASI KOMPETENSI PENDIDIK TAHAP CAKAP DAN MAHIR.pdf

NUMERASI KOMPETENSI PENDIDIK TAHAP CAKAP DAN MAHIR.pdf
PRESENTASI OBSERVASI PENGELOLAAN KINERJA KEPALA SEKOLAH.pptx

PRESENTASI OBSERVASI PENGELOLAAN KINERJA KEPALA SEKOLAH.pptx
Modul Projek - Modul P5 Kearifan Lokal _Menampilkan Tarian Daerah Nusantara_...

Modul Projek - Modul P5 Kearifan Lokal _Menampilkan Tarian Daerah Nusantara_...
ppt landasan pendidikan Alat alat pendidikan PAI 9_

ppt landasan pendidikan Alat alat pendidikan PAI 9_
Modul Ajar PAI dan Budi Pekerti Kelas 2 Fase A Kurikulum Merdeka

Modul Ajar PAI dan Budi Pekerti Kelas 2 Fase A Kurikulum Merdeka
INSTRUMEN PENILAIAN PRAKTIK KINERJA KS Dok Rating Observasi (1).docx

INSTRUMEN PENILAIAN PRAKTIK KINERJA KS Dok Rating Observasi (1).docx
Patofisiologi Sistem Endokrin hormon pada sistem endokrin

Patofisiologi Sistem Endokrin hormon pada sistem endokrin
Ppt mbs
- 1. Etilena glikol dihasilkan dari reaksi etilen oksida dan air dengan perbandingan 1 : 1 3 molekul etilena oksida 5 molekul air 3 molekul etilen glikol 2 molekul air bersisa Habis bereaksi atau reaktan pembatas
- 2. Persamaan reaksi Jumlah mol tiap pereaksi Pembagian mol dengan koefisien Hasil bagi yang lebih kecil merupakan reaktan pembatas Hasil bagi yang lebih besar merupakan pereaksi yang bersisa Mol reaksi pembatas digunakan sebagai patokan
- 3. Sebanyak 28 g logam besi direaksikan dengan 48 g gas oksigen menghasilkan Fe2O3 (Diketahui Ar Fe = 50 dan O = 16). a. Tentukan massa Fe2O3. b. Tentukan massa zat pereaksi yang tersisa Penyelesaian Contoh Soal m Mr 28 g 56 g mol-1 Jumlah mol Fe = = = 0,5 mol m Mr 48 g 32 g mol-1 Jumlah mol O2 = = = 1,5 mol
- 4. Persamaa Reaksi 4Fe + 3O2 2Fe2O3 Jumlah mol zat Jumlah mol zat Koefisien 0,5 mol 1,5 mol 0,5 4 = 0,125 mol 1,5 3 = 0,5 mol Lebih kecil = reaksi pembatas 4Fe + 3O2 2Fe2O3 mol = Koefisien yang dicari Koefisien yang diketahui × Mol reaktan pembatas M : B : S : 0,5 1,5 0,5 3 4 × 0,5 = 0,375 2 4 × 0,5 = 0,25 1,125 0,25
- 5. a. Mr Fe2O3 = (2 × Ar Fe) + (3 × Ar O) = (2 × 56) + (3 × 16) = 112 + 48 = 160 Massa Fe2O3 = mol Fe2O3 × Mr Fe2O3 = 0,25 mol × 160 g mol–1 = 40 g Jadi, massa Fe2O3 = 40 g b. Massa O2 yang bereaksi= n O2 yang bereaksi × Mr O2 = 0,375 mol × 32 g mol–1 = 12 g Massa O2 sisa = massa O2 awal – massa O2 reaksi = 48 g – 12 g = 36 g. Jadi, massa O2 sisa = 36 g Kerjakan Quick Review Unit 5 halaman 158, buku Advanced Learning Chemistry 1A
- 6. 4. Serbuk besi sejumlah 28 gram (Ar Fe = 56) direaksikan dengan 20 gram belerang (Ar S = 32) sesuai dengan persamaan: Fe + S FeS, tentukan zat yang tersisa sesudah reaksi.
- 7. “Berusahalah untuk tidak menjadi manusia yang berhasil tapi berusahalah menjadi manusia yang berguna.’’ Einstein