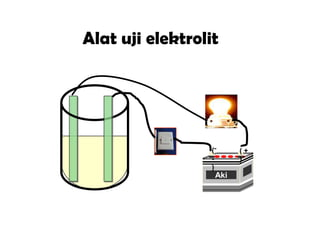
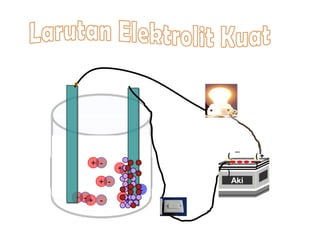
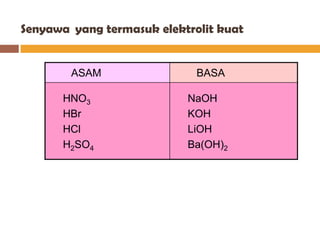
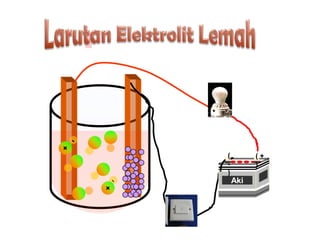
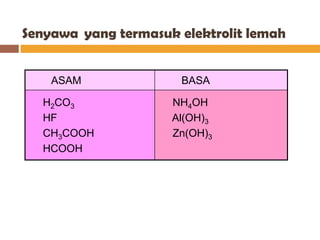
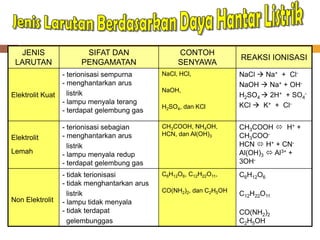
Dokumen tersebut memberikan penjelasan tentang larutan elektrolit dan non elektrolit. Larutan elektrolit mampu menghantarkan arus listrik karena terurai menjadi ion-ion yang dapat bergerak bebas, sedangkan larutan non elektrolit tidak dapat menghantarkan arus karena tidak terurai menjadi ion. Larutan elektrolit dibedakan menjadi kuat, yang terionisasi sempurna, dan lemah, yang terionisasi tidak se