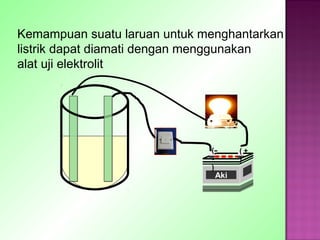
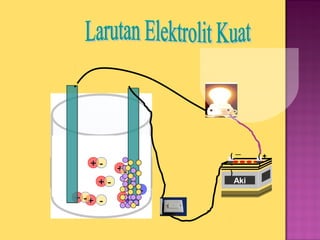
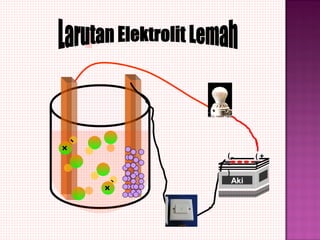
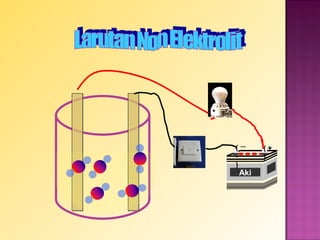
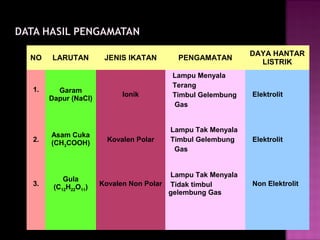
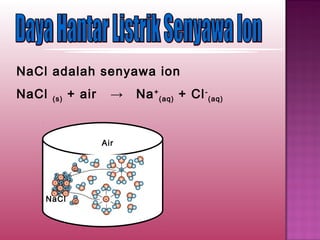
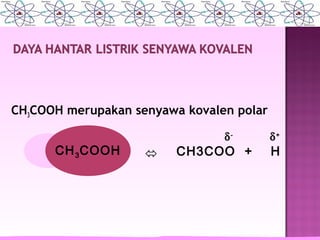
Dokumen tersebut membahas tentang elektrolit dan non elektrolit. Secara singkat, dokumen menjelaskan bahwa larutan dapat dikelompokkan menjadi elektrolit dan non elektrolit berdasarkan kemampuannya untuk menghantarkan listrik. Larutan elektrolit akan menghantarkan listrik karena terurai menjadi ion-ion, sedangkan larutan non elektrolit tidak akan menghantarkan listrik karena tidak terurai.