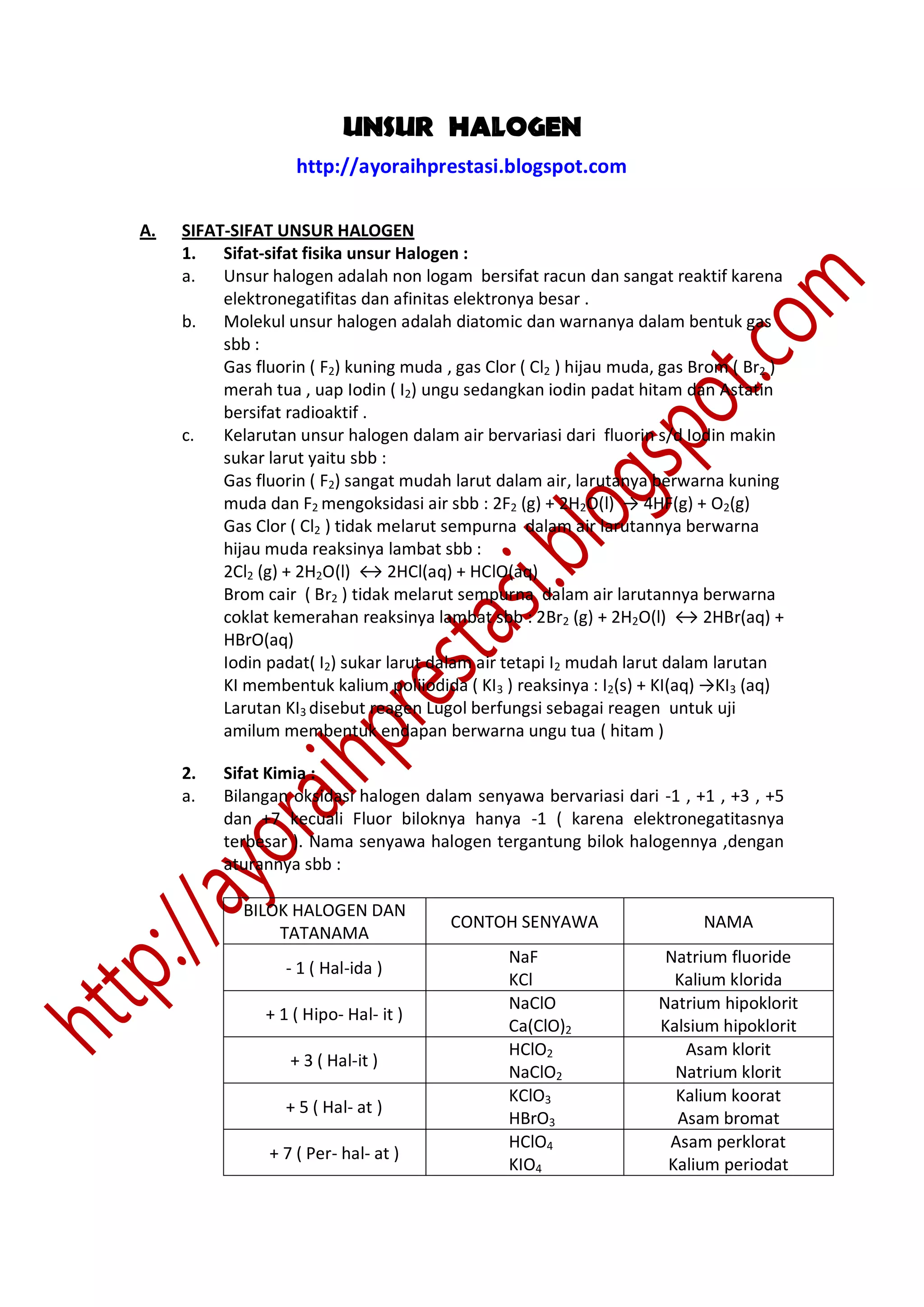
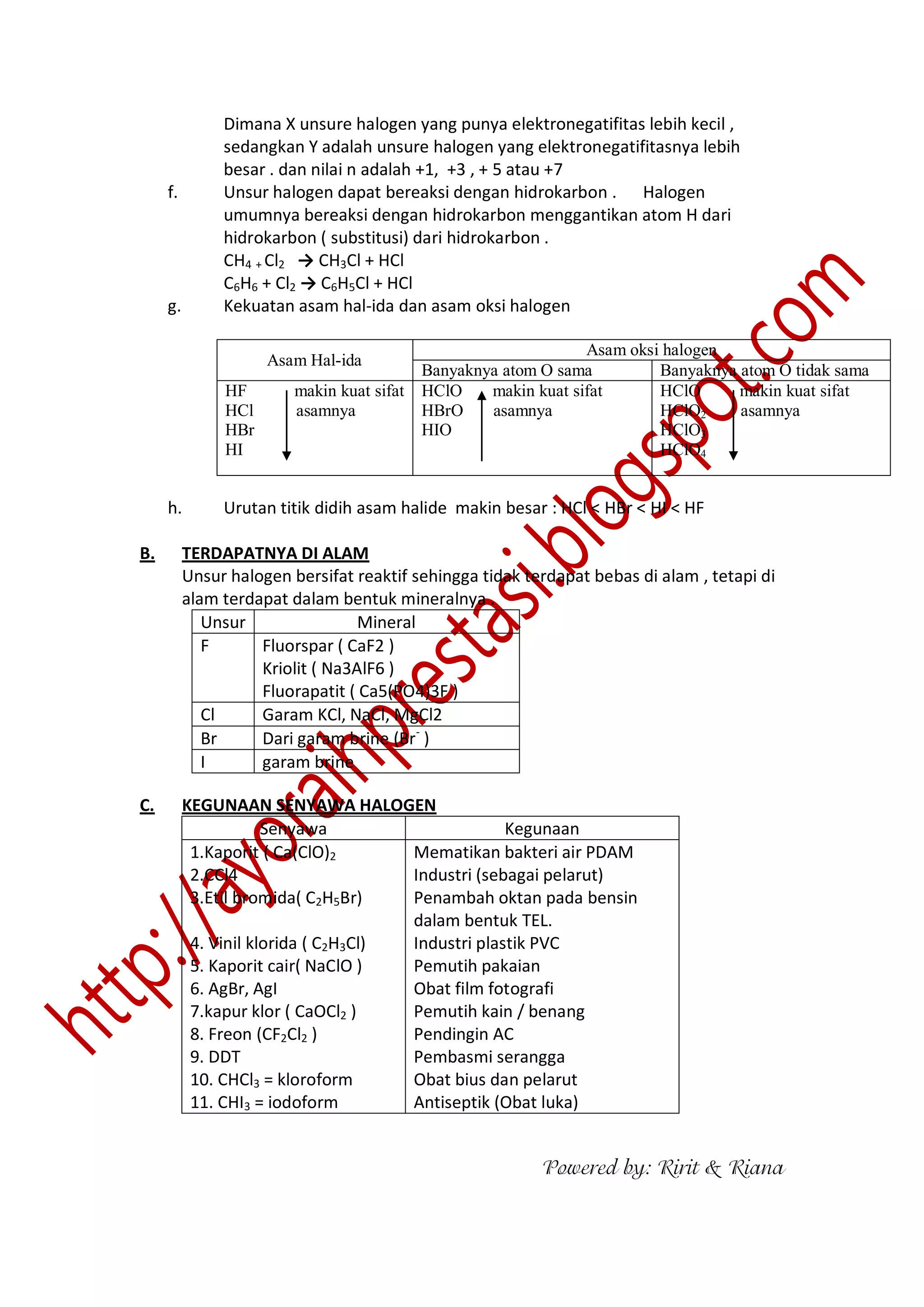
Unsur halogen adalah non logam yang sangat reaktif dan bersifat racun, memiliki variasi kelarutan dalam air serta bilangan oksidasi yang berbeda-beda. Reaksi unsur halogen dengan basa kuat dapat menghasilkan senyawa baru, dan mereka juga dapat bereaksi dengan unsur logam dan non-logam untuk membentuk senyawa halogen. Unsur halogen tidak ditemukan bebas di alam, melainkan dalam bentuk mineral dan memiliki berbagai kegunaan dalam industri dan kehidupan sehari-hari.