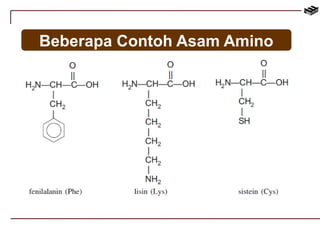
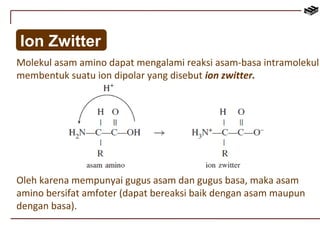
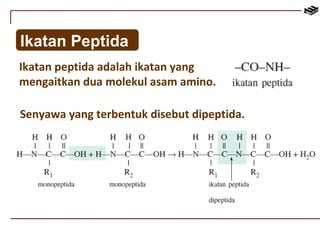
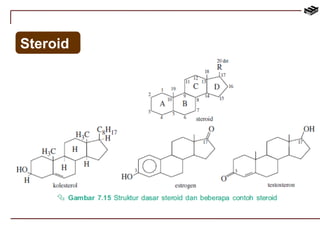
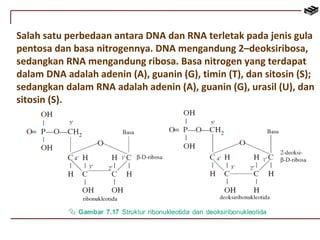
Dokumen ini menjelaskan tentang biomolekul, termasuk protein, karbohidrat, lipid, dan asam nukleat. Protein berfungsi dalam berbagai peran biologis dan terdiri dari asam amino, sedangkan karbohidrat digolongkan menjadi monosakarida, disakarida, dan polisakarida. Struktur dan fungsi lipid, termasuk lemak dan fosfolipid, serta struktur asam nukleat, seperti DNA dan RNA, juga diuraikan.