UNSUR, SENYAWA DAN CAMPURAN
- 1. UNSUR, SENYAWA DAN CAMPURAN
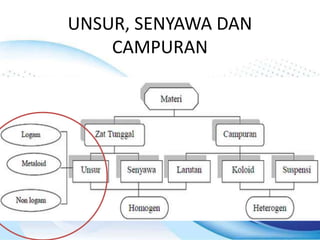
- 2. MATERI Materi : Segala sesuatu yang menempati ruang dan mempunyai massa hanya satu-satunya zat dan tidak ada zat lain selain dirinya Zat Tunggal : artinya semua bagian zat itu bersifat serba sama baik sifat fisis (wujud, warna, rasa, bau, dll.) dan sifat kimianya (rumus kimia, kereaktifan, dll.) Bersifat homogen
- 3. Unsur Zat tunggal yang tidak dapat di uraikan lagi menjadi wujud lain dengan reaksi kimia biasa Contoh : O (Oksigen), Fe (Besi), Al (Aluminium, Zn (Seng), H (hdrogen), Au (Emas), dsb.
- 5. Lambang Unsur Lambang Unsur :Gambar atau simbol untuk mempermudah penulisan unsur
- 6. Tata Penulisan Lambang Unsur 1. Setiap unsur dilambangkan dengan satu huruf dari huruf awal nama latinnya yang dituliskan dengan huruf kapital
- 7. 2. Jika Huruf awal dari nama latinnya sama, maka diberi huruf lain yang dituliskan dengan huruf kecil
- 8. Perbedaan Unsur Logam dan Non Logam
- 9. Perkembangan Pengelompokan Unsur 1. Bedasarkan sifat Logam dan Non logam 2. Menurut Antonie Lavoiser Pengelompokan unsur tersebut berdasarka sifat kimianya. Unsur-unsur kimia di bagi menjadi empat kelompok. Yaitu gas, tanah, logam dan non logam Kelebihan : sudah mengelompokan 33 unsur yang ada berdasarka sifat kimia sehingga bisa di jadikan referensi bagi ilmuan-ilmuan setelahnya Kelemahan : Penglompokan masih terlalu umum
- 10. 3. Menurut Dalton Pengelompokan berdasarkan sifat dan kenaikan nomor atom 4. Menurut John Jacob Berzelius Pengelompokan unsur tersebut berdasarka sifat dan kenaikan nomor atom sudah mengelompokan 50 unsur
- 11. 5. Menurut J Dobereiner mengelompokan unsur-unsur berdasarkan kemiripan sifat-sifatnya Setiap kelompok terdiri dari tiga unsur sehingga disebut Triade Dobereiner Pengelompokan berdasar massa atom unsur, dengan masa atom unsur yang ditengah merupakan rata – rata unsur – unsur dari massa yang mengapitnya
- 12. 5. Menurut J Dobereiner Kelebihannya : adanya keteraturan setiap unsure yang sifatnya mirip massaAtom (Ar) unsure yang kedua (tengah) merupakan massa atom rata-rata di massa atom unsure pertama dan ketiga. Kekurangannya: pengelompokan unsur ini kurang efisian dengan adanya beberapa unsur lain dan tidak termasuk dalam kelompok triad padahal sifatnya sama dengan unsur dalam kelompok triefd tersebut.
- 13. 6. Menurut Oktaf Newlands mengelompokan unsur-unsur berdasarkan kenaikan massa atom relatif. Newlands mengumumkan penemuanya yang di sebut hukum oktaf. Ia menyatakan bahwa sifat-sifat unsur berubah secara teratur.. Unsur pertama mirip dengan unsur kedelapan, unsur kedua mirip dengan unsur kesembilan, dan seterusnya Pada saat daftar Oktaf Newlands disusun, unsur-unsur gas mulia belum ditemukan. Ternyata pengelompokan ini hanya sesuai untuk unsur-unsur ringan (Ar rendah)
- 15. 5. Menurut Oktaf Newlands Kelemahannya : 1. hanya berlaku untuk unsur-unsur ringan. Jika diteruskan, teryata kemiripan sifat terlalu dipaksakan 2. masih ditemukan beberapa oktaf yang isinya lebih dari delapan unsur. 3. penggolonganya ini tidak cocok untuk unsur yang massa atomnya sangat besar.
- 16. 5. Sistem Periodik Mendeleev sifat-sifat unsur adalah fungsi periodik dari massa atom relatifnya. Artinya, jika unsur-unsur disusun menurut kenaikan massa atom relatifnya, maka sifat tertentu akan berulang secara periodik kelebihannya adalah peramalan unsur baru yakni meramalkan unsur beseerta sifat-sifatnya. Kelemahan : masih terdapat unsur-unsur yang massanya lebih besar letaknya di depan unsur yang massanya lebih kecil dan pemebetulanmassa atom. Sebelumnya massa atom In = 76 menjadi 113. selain itu Be, dari 13,5 menjadi 9. U dari 120 menjadi 240
- 17. Tabel Periodek Unsur Mendeleev
- 18. Sistem Periodik Modern dari Henry G. Moseley sifat dasar atom bukan didasari oleh massa atom relative, melainkan berdasarkan kenaikan jumlah proton. Kenaikan jumlah proton ini mencerminkan kenaikan nonor atom unsur tersebut. kebaikan nomor atom dan kemiripan sifat. Lajur-lajur horizontal, yang disebut periode disusun berdasarkan kenaikan nomor atom ; sedangkan lajur-lajur vertikal, yang disebut golongan, disusun berdasarkan kemiripan sifat.
- 19. Tabel Periodeik Unsur Modern
- 21. Perbedaan Asam dan Basa Asam Basa bersifat bersifat rasanya rasanya Mengubah warna indikator . . . . . menjadi . . . . . . korosif kausatik asam pahit Mengubah warna indikator . . . . . . menjadi . . . . . . biru merah merah biru H OH Menghasilkan ion . . . . dalam air Menghasilkan ion . . . . dalam air Tidak licin Licin
- 22. bersifat bersifat rasanya rasanya Mengubah warna indikator . . . . . menjadi . . . . . . korosif kausatik asam pahit Mengubah warna indikator . . . . . . menjadi . . . . . . biru merah biru Menghasilkan ion . . . . dalam air merah Menghasilkan ion . . . . dalam air H OH Tidak licin Licin Mempunyai pH Mempunyai pH < 7 >7