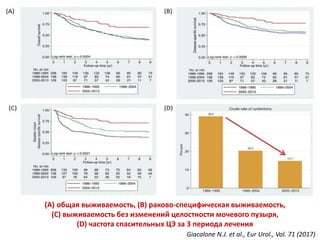
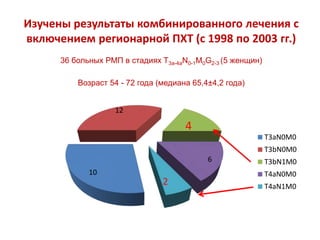
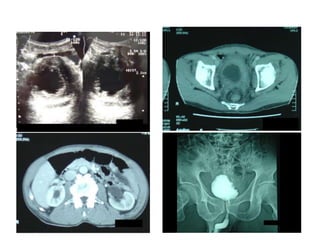
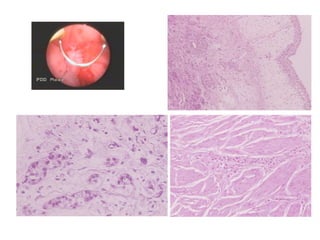
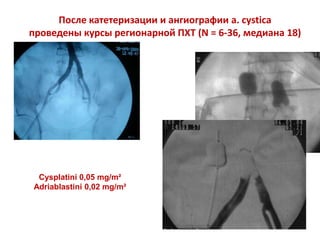
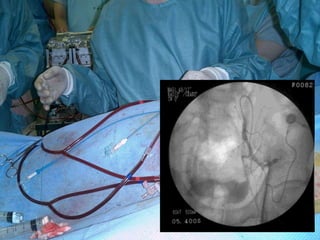
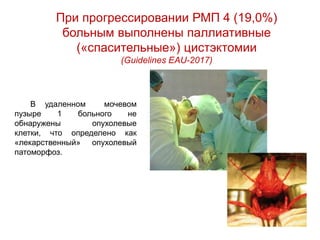
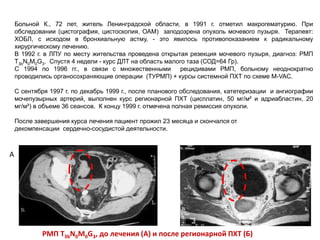
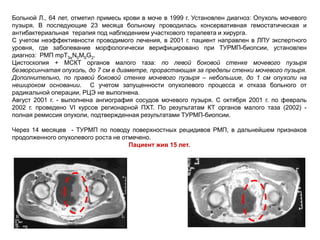
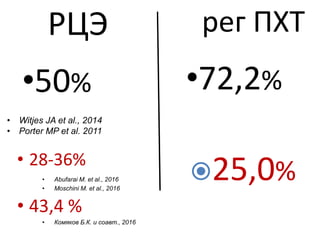
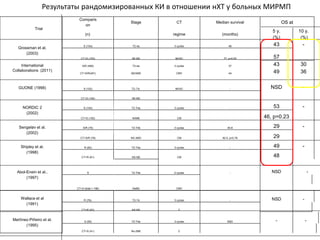
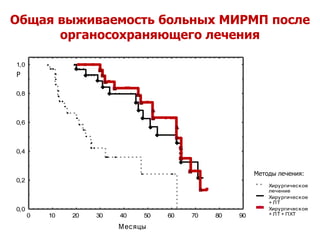
Документ исследует результаты лечения мышечно-инвазивного рака мочевого пузыря, акцентируя внимание на важности радикальной цистэктомии и комбинированной терапии. Подробно рассматриваются вопросы выживаемости, особенности проведения химиотерапии и радиотерапии, а также анализируются современные подходы к органосберегающему лечению. Приводятся данные о частоте осложнений и результатах метаанализов различных методов лечения.
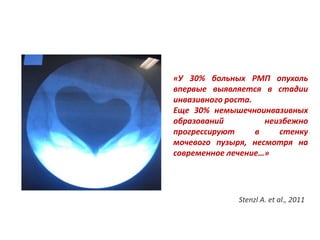

![Радикальная цистэктомия - стандартный
метод лечения локализованного МИРМП в
большинстве западных стран [Stein, J.P. et al., J
Clin Oncol, 2001; Hautmann R.E. et al., Urology, 2007]
В тщательно отобранной популяции
пациентов цель мультимодальной
терапии в сохранении мочевого пузыря
и QoL, без ущерба для результата
[Ploussard G. et al., Eur Urol, 2014]
МИРМП
ОВ
- ?
QoL
- ?](https://image.slidesharecdn.com/2017-171120075854/85/slide-5-320.jpg)


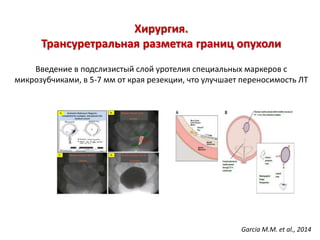
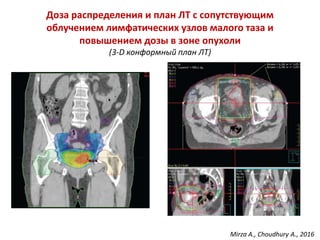
![Облучение. Адаптивная лучевая терапия
Конусная лучевая компьютерная томография (КЛКТ) позволяет
уменьшить дозу облучения здоровых тканей (кишечник и стенка
мочевого пузыря), позволяя подвести к опухоли СОД=70 Гр с
оптимальным уровнем воздействия на опухоль и минимальным
побочным эффектом [Nikapota A.D. et al., 2016; Hafeez S. et al., 2016]
Kibrom A.Z., Knight K.A., 2015](https://image.slidesharecdn.com/2017-171120075854/85/slide-10-320.jpg)
![Химиотерапия. Сроки начала проведения ХТ
до сих пор не определены окончательно
Сведения, подтверждающие преимущество использования НАХТ или АХТ, по-прежнему, обсуждаются
[Mathieu R. et al., 2015].
Полный лекарственный патоморфоз рака после НАХТ в 28% случаев, что определялось
морфологическим типом строения опухоли: при ТСС – max патоморфоз после 3 курсов НАХТ [Pokuri V.K. et al., 2016].
Использование HOXA9
(промотор метилирования)
в качестве потенциального
прогностического биомаркера
устойчивости клеток РМП к
цисплатину
Xylinas E. et al., 2016](https://image.slidesharecdn.com/2017-171120075854/85/slide-12-320.jpg)
![Новые тренды
• 2004- точечное геномное воздействие + ЛТ: созданы 2 рекомбинантных
аденовируса: Ad-hUPII-GFP с зеленым флуоресцентным белком (GFP), и Ad-
hUPII-ФНО, на основе фактора некроза опухоли альфа (TNF-альфа). Высокий
эффект in vitro у TNF-альфа при инфицировании клеток РМП [Zhu H.J. et al., 2004].
Вывод о пользе внутрипузырного введения Ad-hUPII-ФНО в связи с высокой
активностью ингибирования роста раковой опухоли в модели РМП человека
• 2012– изучен молекулярный профиль опухоли, в сочетании с методами
лучевой визуализации, что может играть важную роль в выборе
оптимального лечения для сохранения мочевого пузыря [Koga F., Kihara K., 2012].
• 2016- успешное использование синергетического эффекта ЛТ и ткане-
сецифического онколитического аденовируса (Ad-PSCAE-UPII-E1A) при
воздействии на клетки РМП. Построена и опробована in vitro модель
аденовируса Е1А, под контролем антигена простаты UPII и промотора
стволовых клеток (PSCAE). Обнаружен синергетический противоопухолевый
эффект аденовируса и ЛТ, что может быть потенциальной стратегией для
терапии больных РМП [Wang L. et al., 2014; Zhang H. et al., 2016].](https://image.slidesharecdn.com/2017-171120075854/85/slide-13-320.jpg)
![Стратегия наблюдения больных после завершения
курса комбинированного лечения
1. При полном опухолевом ответе мочевой пузырь остается
потенциальным источником рецидива, следовательно,
долгосрочный мониторинг имеет важное значение
[Lerner S.P., 2016; Witjes A.J. et al., 2016; Milowsky M.I. et al., 2016]
2. Эндоскопическая оценка эффекта ТМП, с систематической
повторной биопсией слизистой после полного завершения
курса. При выраженной резистентности и прогрессировании
опухоли - выполнение спасительной ЦЭ (Guidelines EAU-2017)
У пациентов после БМП показатели 5-летней
ОВ и РСВ составили 36-74% и 50-82%, соотв.
[Ploussard G. et al., 2014].
Лучший эффект ОСЛ отмечен у больных с
небольшим объемом опухоли в стадии Т2,
без сопутствующего гидронефроза или Cis
[Mathieu R. et al., 2015].
Gerardi M.A. et al., 2016](https://image.slidesharecdn.com/2017-171120075854/85/slide-14-320.jpg)