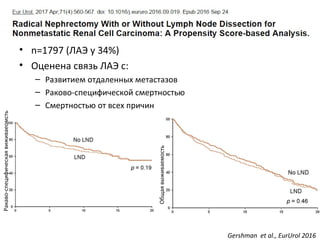
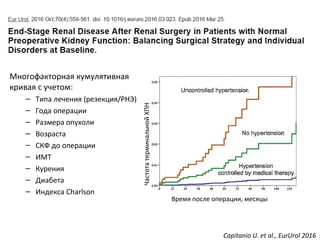
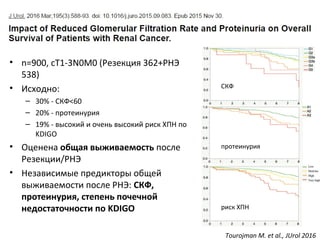
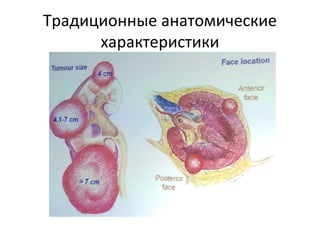
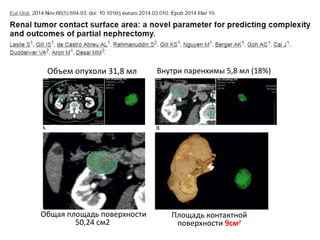
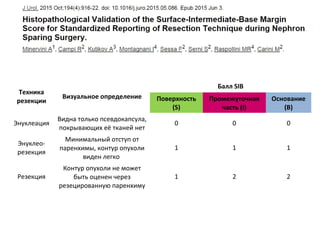
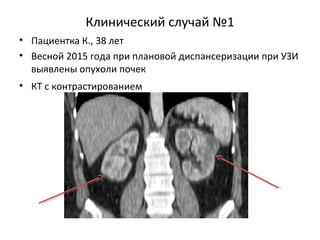
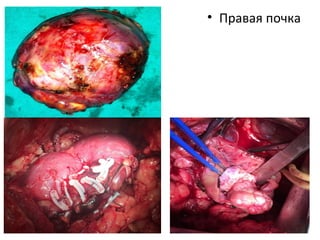
Документ рассматривает почечно-клеточный рак, его заболеваемость и связанные с ним современные методы диагностики и терапии. Обсуждаются хирургические и аблативные технологии, а также методы визуализации, такие как КТ и МРТ, их достоинства и ограничения. Кроме того, подчеркивается важность биопсии для определения гистологического типа опухоли и ее степени дифференцировки.