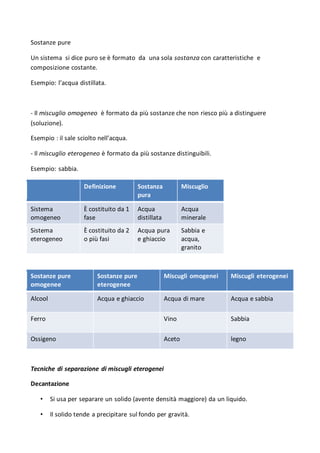
Il documento descrive le differenze tra sostanze pure, miscugli omogenei e miscugli eterogenei, fornendo esempi di ciascuno. Vengono inoltre illustrate diverse tecniche di separazione di miscugli, come decantazione, filtrazione e centrifugazione, con dettagli su un'esercitazione pratica. Infine, vengono presentate applicazioni delle tecniche di separazione attraverso esperimenti concreti.