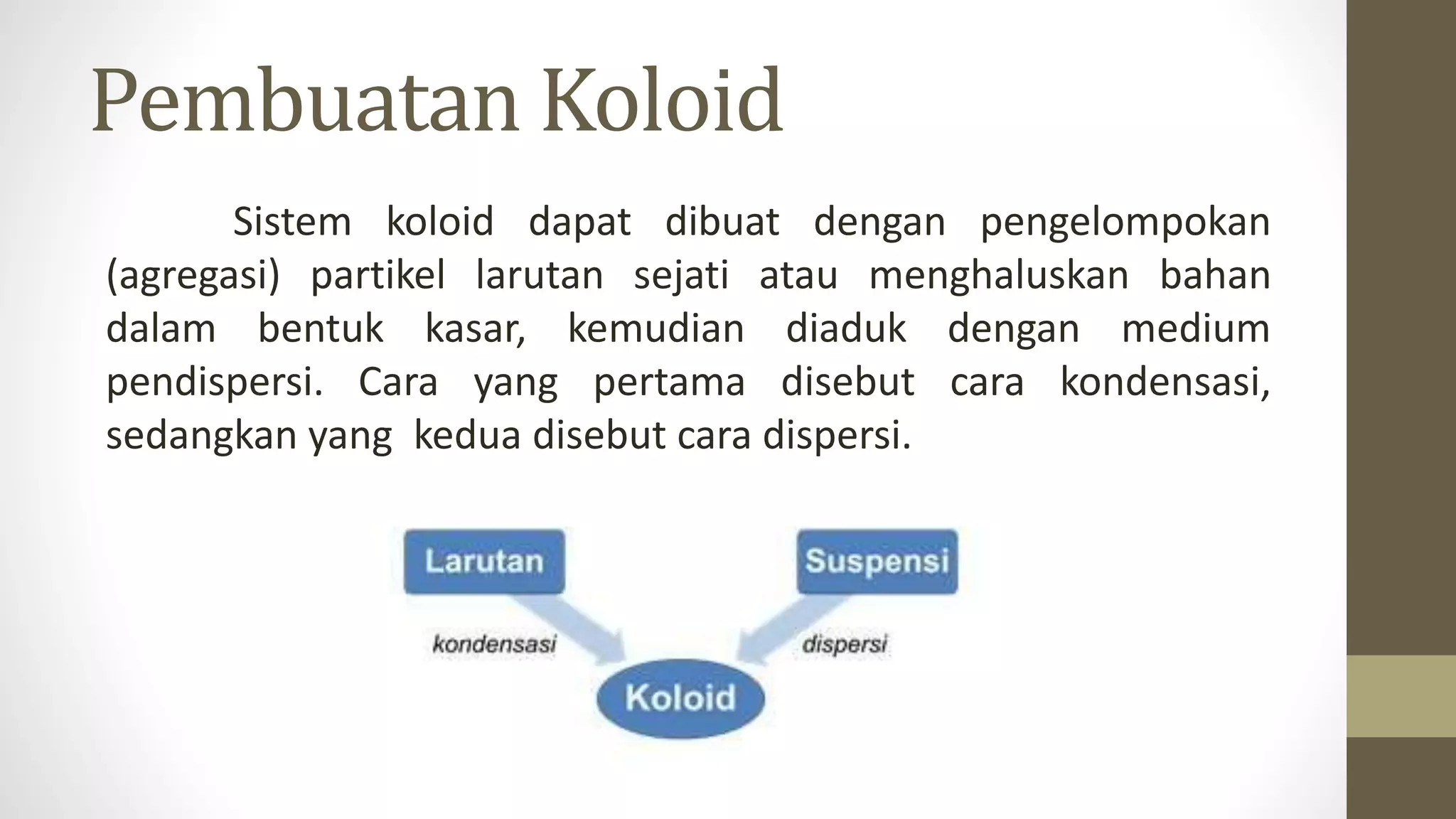
Dokumen ini menjelaskan tentang sistem koloid, yang merupakan campuran antara larutan dan suspensi, beserta jenis-jenis koloid seperti emulsi, sol, busa, aerosol, dan gel. Sifat koloid seperti efek Tyndall, gerak Brown, dan koagulasi dijelaskan, serta cara pembuatan koloid melalui kondensasi dan dispersi. Selain itu, juga dibahas aplikasi koloid dalam kehidupan sehari-hari, seperti pemutihan gula, penggumpalan darah, dan penjernihan air.