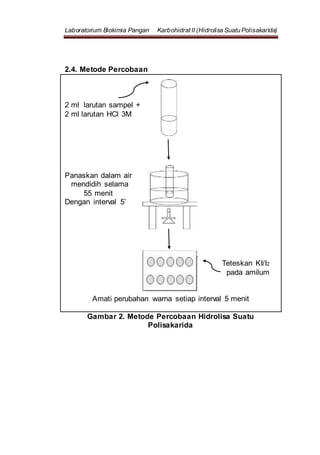
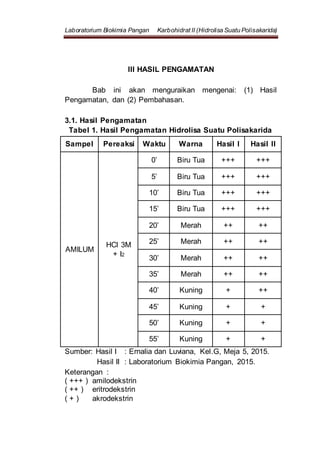
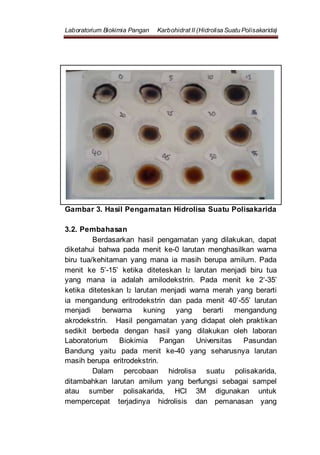
Laporan praktikum ini membahas tentang hidrolisis polisakarida untuk membuktikan bahwa polisakarida terdiri dari beberapa monosakarida. Dengan menggunakan HCl dan pemanasan, amilum dihidrolisis menjadi amilodekstrin, eritrodekstrin, dan akrodekstrin, yang ditandai dengan perubahan warna menggunakan indikator iodium. Kesimpulan menunjukkan bahwa pengamatan warna selama proses menunjukkan tahapan hidrolisis yang berhasil.