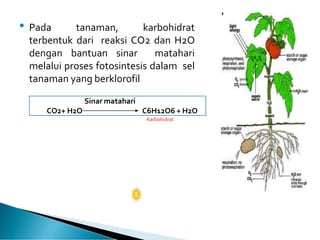
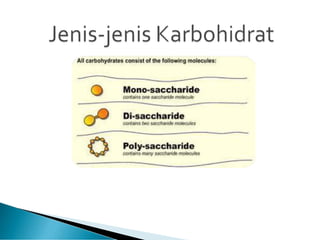
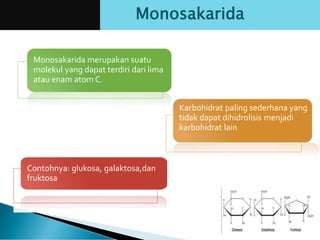
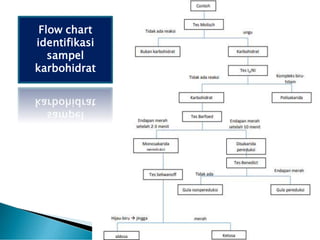
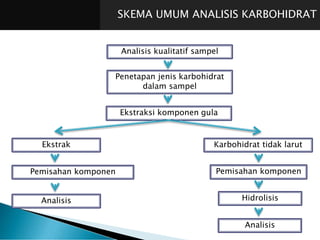
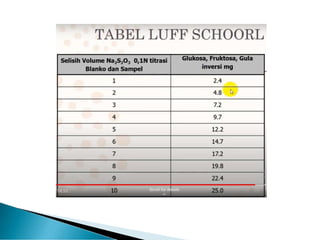
Teks tersebut merupakan ringkasan tentang analisis karbohidrat yang mencakup definisi, jenis-jenis, sifat umum, dan analisis kualitatif dan kuantitatif karbohidrat. Secara khusus membahas tentang monosakarida, oligosakarida, polisakarida, pati, glikogen, serat pangan, dan metode-metode analisis kualitatif dan penetapan kadar karbohidrat dapat dicerna.