More Related Content
ODP
DOC
PPTX
PPTX
PPTX
PDF
нүүрсний тухай товч мэдээлэл DOC
PPT
What's hot
PPT
DOCX
DOCX
ODP
дотоод шүүрлийн булчирхай DOCX
химийн тэнцвэр ба термодинамик үндэслэл PPT
PPT
PPTX
PPTX
PPTX
PPT
101 8-himiin urbaliin hurd PPTX
Химийн урвалын үгэн тэгшитгэл DOCX
ODP
PPTX
Газарзүй 10 дэлхийн усан мандал.pptx ODT
ODP
PPTX
шулуун замын жигд ба жигд биш хөдөлгөөн ODP
8 р анги нийлмэл бодис нэгж PPTX
Viewers also liked
PPTX
PDF
цайрын хүдрийн баяжуулалтын технологи PPTX
Марганцийн хүдрийг баяжуулах технологи PPTX
PPTX
Презентация Калгутинского месторождения DOCX
PPTX
PPTX
PPT
Цагаан хоол эрүүл мэнд шим тэжээл DOCX
PDF
ODP
PPT
PPTX
Similar to 101 16-erdes bayalag
PPTX
PPTX
Полиметаллын хүдрийн математик загварчлал PPTX
PDF
Эрдэм шинжилгээний хурлын эмхтгэл PDF
2013.09.05, Mонгол орны геологийн судалгаа төрөөс баримтлах бодлого, Б.Баатар... PPTX
гравитациар баяжуулах а рга PPTX
7 r angi dizain texnologi er PPTX
Уул уурхайн ирээдүйн чиг хандлага, технологи PPTX
уулын үйлдвэрийн технологийн үндэс лк-10 PPTX
PDF
уул уурхайн төслийн техник, эдийн засгийн үндэслэлд PDF
Уул уурхайн төслийн техник, эдийн засгийн үндэслэлд PPTX
Ашигт малтмалын ордод ашиглалт явуулах арга технологийн үндэс PDF
2016_IMPC_UB-Proceedings-pdf.pdf PPTX
уулын үйлдвэрийн технологийн үндэс лк-1 PDF
Ч.Отгонжаргал С.Мягмарсүрэн Б.Жаргалцэцэг Дэлхийн зах зээл дээрхи зэсийн үний... PPTX
ТЭЗҮ боловсруулагчдын уулзалт семинар DOCX
PPTX
"Экологи байгаль хамгаалал" Хичээл-10 PPTX
нүүрс ба түүний нунтаглал More from Xaz Bit
PPT
PPT
PDF
PPT
101 15-metalliin shinj chanar PPTX
PPT
101 11-elektrolit ba bish PPT
PPT
PPT
PPT
PPTX
PPT
101 3-organic bish angilal,nershil12 PPTX
101 16-erdes bayalag
- 1.
- 2.
Металлуудын байгальд орших
хэлбэр
Сульфид:FeS2 төмрийн колчедан,
PbS-хар тугалганы гялтгана, ZnS-
цайрын хуурмаг, CaSO4 ангидрит
Оксид: Fe3O4 соронзон гүр,
Al2O3 ∙2H2O- хөнгөнцагааны боксит,
Силикат:3MgO∙2SiO ∙2H2O-асбест,
SiO2 –элс, кварц,
Карбонат:CaCO3 –шохойн чулуу,
CuCO3 ∙Cu(OH)2-малахит буюу оюу
- 3.
Хлорид:NaCl-хоолны давс,
KCl∙MgCl2-карналлит
Сульфат:Na2 SO4∙10H2O-
мирабилит, CuSO4 ∙5H2O- зэсийн
байван, Na2B4O7 ∙10H2O- тунсаа
Фосфат:Ca3 (PO4)2 -фосфорит
Волластонит: -Ca3(Si3O9)
- 4.
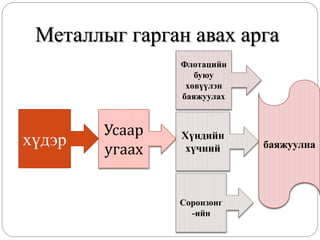
Металлыг гарган авахарга
хүдэр
Усаар
угаах
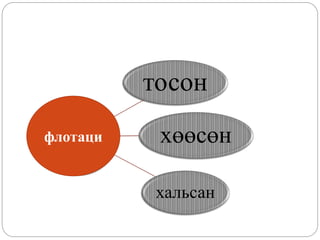
Флотацийн
буюу
хөвүүлэн
баяжуулах
Хүндийн
хүчний
Соронзонг
-ийн
баяжуулна
- 5.
- 6.
- 7.
Хүндийн хүчний арга
Үндсэнэрдэс хоосон чулуулаг
хоёрын нягтын ялгаанд
тулгуурлана.
Соронзонгийн арга:
Соронзон орны үйлчлэлд өртөг
ялгаанд тулгуурлана.
- 8.
- 9.
Гидрометаллурги
Ердийн температурынүед хүдэрт
байгаа металлыг янз бүрийн урвалж
ашиглан усан уусмалд шилжүүлээд
түүнээсээ электролизоор дан металл
гарган авах арга
CuO+H2SO4 =CuSO4 +H2O
CuSO4 +Fe=Cu+FeSO4
- 10.
Алтыг уусгах:
“Хаан дарс”HNO3 +4HCl
Au+HNO3 +4HCI=H[AuCl4]+NO↑+2H2O
Хүчилтөрөгчийн оролцоотойгоор
цианидын уусмалд уусгадаг.
4Au+8KCN+2H2O+O2=4K[Au(CN)2]+4KOH
2K[Au(CN)2]+Zn=K2 [Zn(CN)4]+2Au
- 11.
- 12.
Цэвэршүүлэлт хийх арга
Ваакуум нэрлэг: Металлуудын
дэгдэмхий чанар харилцан адилгүй
байдагт тулгуурлана.
Дулааны задаргааны арга:
Жнь: металл титаныг цэвэр иодтой
9000С –д халаахад
Ti+2I2 =TiI4
)(22 )(2
14001300
)(4
200100
)(2
00
цэвэрTiITiITiI хатуу
С
уур
C
хольц
- 13.
Металлын хайлшууд
Амальгам-хайлшМе ба Hg
Бронз- Cu (80-90%)+Sn (20-10%)
Дуральюмин-AI (95% хүртэл)+Cu(3-
5%)+Mn ба Mg нэмэлт
Алт үнэт, эдлэл-Au нь Ag болон бусад
металлуудтай нэгдэнэ. (үнэт эдлэлийн
сорьцыг алтны агуулгаас хамааруулан
тухайлбал 375 гэсэн сорьц- 37,5%-Au, 583
гэвэл 58,3% -Au)
- 14.
Латунь-Cu+Zn (4-50%)
Мельхиор-Cu+Ni (5-30%)
Ган-Fe(98%)+C (1,5%)+ Mn,
Cr, Ni, S, P, Si хольц
Ширэм- Fe (93%)+C (4,5%
хүртэл)+ Mn, Cr, Ni, S, P, Si
хольц
- 15.







![Алтыг уусгах:
“Хаан дарс” HNO3 +4HCl
Au+HNO3 +4HCI=H[AuCl4]+NO↑+2H2O
Хүчилтөрөгчийн оролцоотойгоор
цианидын уусмалд уусгадаг.
4Au+8KCN+2H2O+O2=4K[Au(CN)2]+4KOH
2K[Au(CN)2]+Zn=K2 [Zn(CN)4]+2Au](https://image.slidesharecdn.com/101-16-erdesbayalag-150130051450-conversion-gate02/85/101-16-erdes-bayalag-10-320.jpg)




