More Related Content
PPTX
ODT
PPT
PPTX
PPTX
ODT
ODT
PPTX
What's hot
PDF
Хүнийн хөгжлийн индексийг тооцох аргууд DOCX
үйлдвэрлэлийн дадлагын тайлан PPT
Архи , тамхины талаарх бодит мэдээлэл PPT
PDF
хөдөлмөр эрхлэлт ба ажилгүйдэл PPTX
гэр бүл түүний нийгмийн үүрэг DOCX
PPTX
DOCX
PPTX
эсийн бүтэц бүрхүүл бөөм сийвэн PPT
PPTX
ODP
ODP
PPTX
PPTX
ялгаруулах эрхтэн тогтолцоо PPTX
DOCX
катионуудыг таних чанарын чанарын урвалууд ODP
ODP
Viewers also liked
PPT
PPTX
PPTX
ODP
PPTX
PPT
101 15-metalliin shinj chanar PPTX
PDF
химийн жишиг даалгавар 2012 он 9 р анги ODP
PPTX
ODP
PPT
PPTX
PDF
химийн элементүүд үзүүлэн 2 ODP
PPT
PDF
PPTX
DOCX
Химийн элемент бүтээгээрэй PPTX
Similar to 101 4-yeleh huuli
PPT
PPTX
PPTX
DOCX
PDF
DOCX
Ximi 9 r angi angiin daalgavar PPT
ODP
PDF
PPT
PDF
800.mn 2014 chemistry a by byambaa avirmed PPTX
DOCX
хими ээлжит хичээлийн хөтөлбөр DOCX
DOCX
физик химийн үүсэл хөгжлийн үндсэн чиглэл PPTX
DOCX
физик химийн үүсэл хөгжлийн үндсэн чиглэл DOCX
PPTX
Tsewerlex arga 1 r bair amjilt PDF
More from Xaz Bit
PPT
101 11-elektrolit ba bish PPTX
PPT
101 8-himiin urbaliin hurd PPTX
PPT
101 3-organic bish angilal,nershil12 PPTX
PPTX
PPT
PPTX
PPT
PPT
101 4-yeleh huuli
- 1.
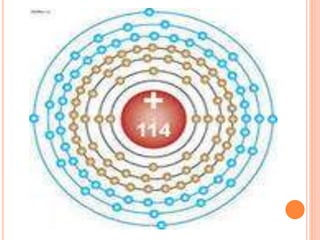
АТОМЫН БҮТЭЦ БАҮЕЛЭХ СИСТЕМИЙН
ХООРОНДЫН ХОЛБОО
ЗНАЧЕНИЕ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
Агуулга:
Үелэх системийн бүтэц, aтомын
иончлолын (I) ба төрөлсөх ажил (E),
СЦЧ (Δχ), өдөөгдсөн төлөв, орбитын
радиус, валент чанар, үе, давхраа,
бүлэг
- 2.
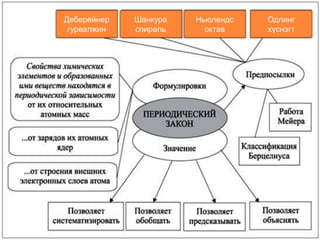
Химийн элементүүдийг ангилаханхны
оролдлогыг 1829 онд химич
И.Доберейнер хийжээ.
Түүнээс хойш 1862 онд Францын
химич А.Э. Шанкуртуа, 1863 онд
Английн химич Р.Ньюлендс, 1864 онд
Германы химич Л.Майэр нар атом
жингийн холбогдлуудаар
элементүүдийг ангилах санааг
дэвшүүлж оролдлого хийж байжээ.
- 3.
- 5.
- 7.
Химийн элементийн үелэххуулийг нээж,
үелэх системийг боловсруулах хамгийн
шийдвэрлэх алхмыг Оросын эрдэмтэн
Д.И.Менделеев 1869 оны 2-р сард
“Оросын химийн нийгэмлэгийн сэтгүүл”-д
нийтлүүлсэн нэгэн өгүүлэлдээ “Атом
жин болон химийн төсөөтэй чанар
дээр үндэслэсэн химийн
элементүүдийг эмхлэн цэгцэлсэн
туршлага” нэртэйгээр үелэх системийн
анхны хувилбарыг химич нарт илгээжээ.
- 9.
Энэ үеднээгдээгүй байсан 6 элементийг
тэдгээрийн шинж чанарын хамт урьдчилан хэлж,
үелэх системийг хэрэглэхийн гайхамшигт жишээг
биеэр үзүүлжээ.
Эдгээр элементүүдийг үелэх системийн хоосон
байсан нүднүүдэд байрлуулаад экабор,
экахөнгөнцагаан, экацахиур, экаманган,
экадиманган, экатантал гэж нэрлэсэн.
Удалгүй тэдгээрээс бор, хөнгөнцагаан, цахиураас
эхлэн тус тус анхдагч нүдний элементүүд нээгдэж
сканди, галли, германи гэсэн нэрийг авчээ.
Эдгээрийн шинж чанар, нэгдэл нь Менделеевийн
урьдчилан хэлсэнтэй гайхалтай тохирч байлаа.
- 10.
- 11.
- 12.
- 13.
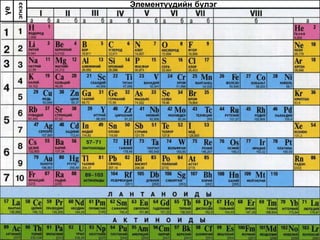
Бүлэг= валентын электронытоо
Үе = гадаад давхраа
Дэс дугаар=цөмийн цэнэгийн тоо
Жнь: IY- үед (давхраа) :
19K39.09 1s2 2s2 2p6 3s2 3p6 4s1
[Ne10 ] 3s2 3p6 4s1
) ) ) )
2 8 8 1
4- р үе учраас дөрвөн давхраатай
1-р бүлэг учраас гадаад давхраандаа 1
электронтой
- 14.
Электрон 1 түвшнээснөгөөд
шилжихдээ энергийг цацруулах ба
шингээнэ.
Э0+I =Э+ +е- , I-атомын иончлолын
энерги
Э0+е- =Э- +F , F-атомын электронд
төрөлсөх ажил (кЖ/ моль-атом)
Ө.х саармаг атомд электроныг
нэгдүүлж, түүнийг сөрөг цэнэгтэй ион
Э—-д шилжүүлэхэд ялгарах энерги.
- 15.
ﻼ =
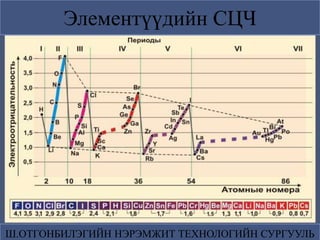
СЦЧ ньүелэх системийн үеийн дагуу
буурдаг. Иймд IA бүлгийн шүлтийн
металлууд, ялангуяа франци /Fz/
ХБСЦЧ-тай байхад, р-элемент
тухайлбал VllА бүлгийн элемент
түүний дотор S,P ХИСЦЧ-тай.
IF
2
1
- 17.
- 18.
- 19.
ДААЛГАВАР:
периодическая системахимических элементов
Periodic table
1. www.yandex.ru
2. www.google.com
3. www.wikipedia.org
Үелэх систем болон химийн элементүүдийн талаарх
15-20 даалгавар бүхий үгийн сүлжээ зохиох
Үелэх системд байрласан элементийн тодорхой дэс
дугаарт харгалзах тэр элементийг хэрхэн нээсэн
түүх, физик шинж чанар, хэрэглээ сэдвийг судалж 3-
5 слайд (Power point программ ашиглан) хийх
Хугацаа 09-23-ээс 10-07 хүртэл
tseelei@gmail.com электрон хаягаар ба электрон
хэлбэрээр өгөх










![Бүлэг= валентын электроны тоо
Үе = гадаад давхраа
Дэс дугаар=цөмийн цэнэгийн тоо
Жнь: IY- үед (давхраа) :
19K39.09 1s2 2s2 2p6 3s2 3p6 4s1
[Ne10 ] 3s2 3p6 4s1
) ) ) )
2 8 8 1
4- р үе учраас дөрвөн давхраатай
1-р бүлэг учраас гадаад давхраандаа 1
электронтой](https://image.slidesharecdn.com/101-4-yelehhuuli-150130051345-conversion-gate02/85/101-4-yeleh-huuli-13-320.jpg)