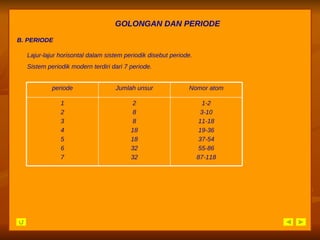
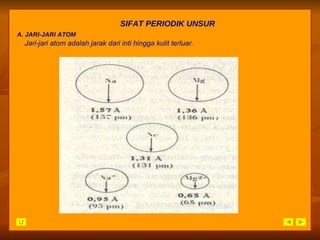
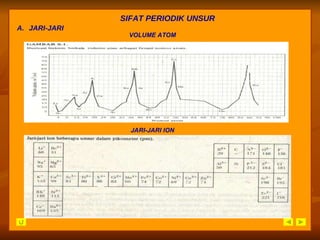
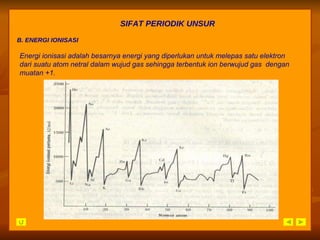
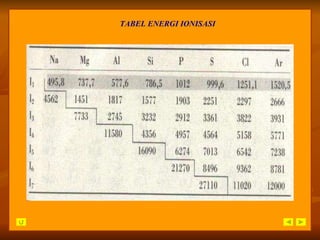
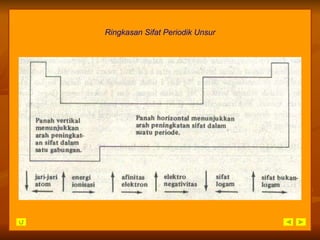
Dokumen ini membahas perkembangan tabel periodik unsur dari triade Dobereiner hingga sistem modern Moseley, dengan fokus pada pengelompokan unsur berdasarkan sifat dan nomor atom. Siswa diharapkan dapat memahami struktur dan sifat-sifat periodik unsur, serta menganalisis data keperiodikan dari tabel periodik. Evaluasi dan latihan soal disertakan untuk menguji pemahaman siswa tentang materi tersebut.