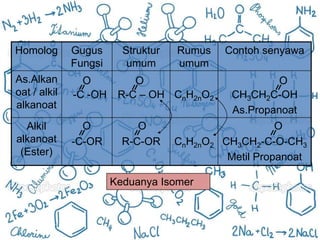
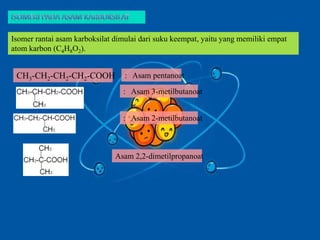
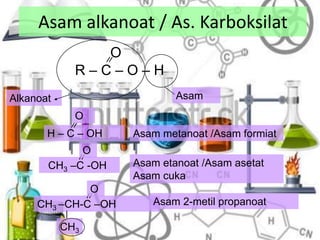
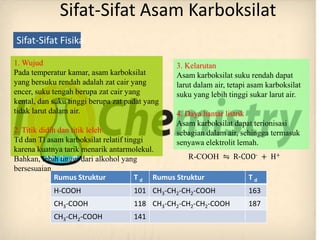
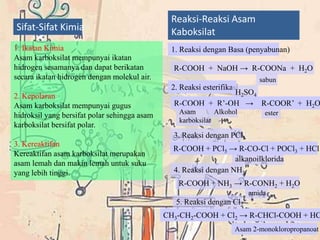
Asam karboksilat dan ester adalah senyawa organik yang memiliki rumus umum CnH2nO2 tetapi berbeda gugus fungsinya, yaitu asam karboksilat berfungsi sebagai asam dengan gugus -COOH, sedangkan ester berfungsi sebagai non-asam dengan gugus -COOR'. Keduanya memiliki sifat fisika dan kimia yang berbeda serta berbagai kegunaan penting.