ENERGI
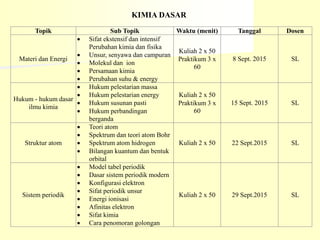
- 1. Topik Sub Topik Waktu (menit) Tanggal Dosen Materi dan Energi Sifat ekstensif dan intensif Perubahan kimia dan fisika Unsur, senyawa dan campuran Molekul dan ion Persamaan kimia Perubahan suhu & energy Kuliah 2 x 50 Praktikum 3 x 60 8 Sept. 2015 SL Hukum - hukum dasar ilmu kimia Hukum pelestarian massa Hukum pelestarian energy Hukum susunan pasti Hukum perbandingan berganda Kuliah 2 x 50 Praktikum 3 x 60 15 Sept. 2015 SL Struktur atom Teori atom Spektrum dan teori atom Bohr Spektrum atom hidrogen Bilangan kuantum dan bentuk orbital Kuliah 2 x 50 22 Sept.2015 SL Sistem periodik Model tabel periodik Dasar sistem periodik modern Konfigurasi elektron Sifat periodik unsur Energi ionisasi Afinitas elektron Sifat kimia Cara penomoran golongan Kuliah 2 x 50 29 Sept.2015 SL KIMIA DASAR
- 2. Stoikiometri Hukum dasar stoikiometri Penyetaraan persamaan kimia Pengaruh massa dalam reaksi kimia Reaksi pembatas Hasil secara teoritis, aktual dan persen (yield) Rumus empiris Rumus molekul Kuliah 4 x 50 Praktikum 3 x 60 6, 13 Okt. 2015 SL Ikatan kimia dan struktur molekul Ikatan kimia Jenis ikatan o Ikatan ion o Ikatan kovalen o Ikatan kovalen koordinasi o Ikatan kimia lainnya (ikatan van der waals, ikatan hidrogen, ikatan logam) Teori ikatan valensi Teori orbital molekul Kuliah 4 x 50 20, 27 okt. 2015 SL Ujian Tengah semester 3 Nov. 2015 (SL)
- 3. Kimia inti Proses peluruhan radioaktif Reaksi inti Kecepatan reaksi inti Faktor yang mempengaruhi kestabilan inti Deret peluruhan Perubahan energi dan reaksi inti Reaksi Fisi dan fusi Pengaruh biologis radioaktif Kuliah 2 x 50 10 Nov. 2015 MD Larutan Proses pelarutan Faktor yang berpengaruh terhadap pelarutan Perhitungan konsentrasi larutan dan pembuatan larutan Kuliah 4 x 50 Praktikum 3 x 60 17, 24 Nov. 2015 MD Sifat koligatif larutan dan keadaan koloidal Perhitungan sifat larutan elektrolit dan non elektrolit Osmosis. Sistem koloidal Kuliah 2 x 50 Praktikum 3 x 60 1 Des. 2015 MD Pengenalan senyawa organik Senyawa hidrokarbon Senyawa bergugus fungsi Kuliah 4 x 50 Praktikum 3 x 60 8 Des. 2015 MD Kuliah 26 x 50 Evaluasi Quiz, UTS dan UAS 4 x 50 Praktikum 18 x 60 Ujian Akhir Semester tanggal 15 Desember 2015 (MD)
- 4. REFERENSI: 1. Will, J.W., R. H. Petrucci, T. W. McCreary and A. C. Perry, 2005, General Chemistry, 4th Edition, Pearson Preintice Hall, New Jersey. 2. Syukri, S, 1999, Kimia Dasar, ITB, Bandung. 3. Keenan, C. W., D. C. Kleinfelter and J. H. Wood, 1989, Imu kimia untuk Universitas, alih bahasa A. H. Pudjaatmaka, Erlangga, Jakarta. 4. Zumdahl, S. S. and S. A. Zumdahl, 2007, Chemistry, 7th edition, Houghton Mifflin, New York. 5. Whitten, K.W., R.E. Davis, M. L. Peck and G. G. Stanley, 2003, General Chemistry, 7th edition, Brooks/Cole, USA.
- 5. KIMIA DASAR • Materi dan energi • Hukum-hukum dasar ilmu kimia • Struktur atom • Konfigurasi elektron • Ikatan kimia • Kimia inti • Unsur-unsur penting dalam bidang pertanian • Koloidal • Larutan • Pengenalan senyawa organik (sifat fisika dan kimia)
- 6. ILMU KIMIA
- 11. ENERGI: E = mc2 E = h c/
- 12. Materi & Perubahannya Zat tunggal campuran Unsur Senyawa Homogen Heterogen Sifat fisika Sifat kimia Sifat ektensif Sifat intensif MATERI
- 13. • Zat tunggal yg tidak dpt diuraikan lagi menjadi zat lain yg lbh sederhana dgn reaksi kimia biasa Au, Cu Unsur • Unsur alam : nomor 1 sampai 92 • Unsur buatan: nomor 93 sampai 108 Unsur Logam, non logam dan metaloid. Unsur metaloid: unsur peralihan dari logam ke non logam sehingga mempunyai beberapa sifat logam dan non logam • Alotrop: bentuk yg berbeda dr unsur yg sama Contoh: grafit dan intan bentuk alotrop dr karbon Sampai awal abad 19 memberikan lambang unsur berdasarkan bentuk gambar tertentu Menurut sistem Berzelius unsur mempunyai lambang yg terdiri dari 1 huruf atau 2 huruf H, C, O, N, Ca
- 14. Penulisan lambang unsur 1. Unsur yg tdr dr 1 huruf harus memakai huruf kapital 2. Unsur yg tdr dr 2 huruf harus memakai huruf besar pd yg pertama dan huruf kecil pd yg kedua Co : unsur cobalt tidak ditulis CO : karbon monoksida (senyawa)
- 16. Senyawa yi: zat yg dpt diuraikan secara kimia menjadi dua zat atau lebih dgn sifat berbeda dari asalnya Air : gas Hidrogen & gas oksigen Gula: arang & air Garam dapur: logam Natrium & gas chlor Batu kapur: kapur tohor & karbondioksida
- 17. Penulisan unsur dibedakan atas: • mono atom: besi (Fe) tembaga (Cu) karbon (C) emas (Au), dll • diatom : H2, O2, N2, F2, Cl2, Br2, I2 • tetraatom : P4 Penulisan Senyawa : air (H2O) gula pasir (sukrosa C12H22O11) alkohol (etanol C2H5OH) Rumus molekul hidrogen = H2 Lambang atom hidrogen = H Molekul = gabungan atom-atom Molekul Unsur atom-atomnya sejenis: H2, O2, N2 Molekul senyawa atom-atomnya berbeda jenis: NaCl, H2O, CH4 Atom = partikel terkecil penyusun unsur Molekul = partikel terkecil penyusun senyawa
- 18. Ion: Partikel bermuatan yang terbentuk dengan cara transfer elektron antara unsur atau padanan unsur Kation: ion bermuatan positif, Ca Ca2+ + 2e- Anion : ion bermuatan negatif , F2 + 2e- 2F- Senyawa Ionik • Beberapa ion sederhana: Kation (Na+, Mg2+, Al3+ Anion (Cl-, O2-, N3-) • Ion Poliatom Golongan khusus dari ion yang mana kelompok atom tersebut cenderung untuk bersama: NH4 +, NO3 -, SO4 2-, OH- Rumus untuk beberapa senyawa ionik
- 20. Campuran Campuran homogen atau larutan, tidak dapat dibedakan satu dgn lainnya Campuran heterogen, dapat dibedakan dgn mudah Ciri-cirinya: 1. Masing-masing komponen mempunyai rasa tersendiri gula rasanya manis msh dpt dirasakan dlm larutan gula 2. Komponen penyusun campuran dpt dipisahkan secara fisika penyaringan, penyulingan, penguapan, kristalisasi, kromatografi 3. Komponen penyusunnya tidak mempunyai perbandingan jumlah tertentu
- 21. Larutan: zar terlarut kadarnya kecil dan zat pelarut kadarnya besar Kelarutan: jumlah maksimum zat yg dpt larut dlm pelarut tertentu Cepat lambatnya suatu zat terlarut dalam pelarut ditentukan oleh: besar kecilnya partikel, suhu dan pengadukan.
- 25. Diskusi B Dapatkah larutan itu cairan, padatan atau gas ? Manakah diantara zat berikut larutan atau campuran heterogen? a. Cairan susu sapi b. Minyak goreng c. Amalgam perak ( digunakan untuk pengisi gigi terdiri atas perak dan merkuri yg tersebar secara merata) d. lumpur
- 26. Perubahan Materi Perubahan biologi Perubahan kimia Perubahan fisika Kayu abu Fotosintesis, fermentasi, perkaratan besi Pelapukan kayu oleh rayap Air es Kayu potongan kayu kecil
- 27. Perubahan apakah ini ?
- 28. Diskusi Pada urutan berikut manakah yang merupakan perubahan kimia dan manakah perubahan fisika? a. Gas Oksigen dicairkan, sebagian oksigen cair digunakan sebagai bahan bakar pesawat ruang angkasa, sebagian diuapkan dan dimasukan ke ruang penumpang, kemudian O2 digunakan untuk bernafas dan berubah menjadi CO2 dan H2O b. Lemak daging sapi dipanaskan di penggorengan sampai cair, dan dipanaskan terus sampai berubah kecoklat-coklatan dan menyebarkan bau menyengat,apabila terus dipanaskan lemak akan menyala dan terbakar. c. Nasi sudah menjadi bubur d. Susu menjadi basi
- 29. Menggambarkan reaksi kimia yang terdiri atas rumus kimia pereaksi dan hasil reaksi disertai koefisiennya masing-masing PENTING!!! Reaksi kimia mengubah zat-zat asal (pereaksi/ reaktan) menjadi zat baru (produk). Jenis dan jumlah atom yang terlibat dalam reaksi tidak berubah. Ikatan kimianya yang berubah, dimana ikatan kimia pereaksi diputus dan terbentuk ikatan kimia baru dalam produknya. PERSAMAAN REAKSI
- 30. PERSAMAAN REAKSI Reaksi setara antara H2 dan O2 membentuk air. 2 H2 + O2 2 H2O Perhatikan: 2 H2O koefisien angka indeks
- 31. PENYETARAAN PERSAMAAN REAKSI KIMIA Contoh ; Langkah 1: Al(s) + H2SO4(aq) Al2(SO4)3(aq) + H2(g) (belum setara) Langkah 2: 2Al(s) + 3 H2SO4(aq) Al2(SO4)3(aq) + 3H2(g) setara) LANGKAH-LANGKAH PENYETARAAN: - Tetapkan koefisien salah satu zat (biasanya yang paling kompleks), sama dengan 1, dan zat lain dengan abjad. - Setarakan lebih dahulu unsur yang berkaitan langsung dengan zat yang diberi koefisien 1. - Setarakan unsur lain. Biasanya unsur O disetarakan paling akhir.
- 32. PERUBAHAN ENERGI Energi : kemampuan melakukan kerja Bentuk energi : 1. kinetik 2. potensial 3. panas 4. cahaya 5. listrik 6. kimia 7. nuklir
- 33. 1. Energi kinetik : energi yang dimiliki suatu materi yang bergerak 2. Energi potensial: energi yang dikandung suatu materi berdasarkan tinggi rendah kedudukannya 3. Energi panas: energi yang ditimbulkan karena adanya gerakan partikel Ek = ½ m v Ep = m g h q = w c (t2-t1) = w c ∆t 4. Energi cahaya: energi yang dimilki oleh gerakan foton dalam bentuk gelombang elektromagnetik v = c/λ → Ec = h ν
- 34. 5. Energi listrik : energi yang diakibatkan oleh gerakan partikel bermuatan dalam suatu media (konduktor) 6. Energi kimia: energi yang dikandung suatu senyawa dalam bentuk energi ikatan antara atom-atomnya/ reaksi kimia 7. Energi nuklir: energi yang terkandung dalam inti atom karena adanya ikatan yang kuat antara partikel di dalamnya. W = q E