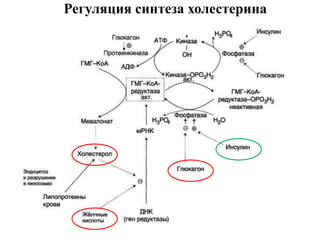
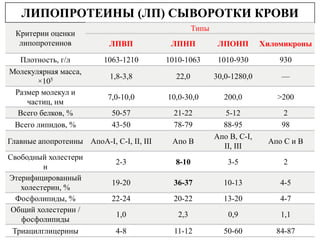
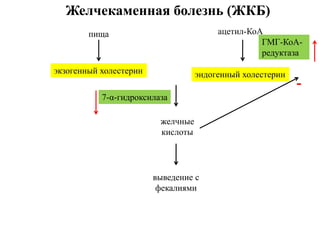
Документ содержит информацию о метаболизме и транспорте холестерина, атеросклерозе и гиперхолестеринемии. Основное внимание уделяется синтезу холестерина в печени, регуляции его уровня и механизму действия липопротеинов. Также рассматриваются причины развития желчекаменной болезни и показатели дислипидемий.