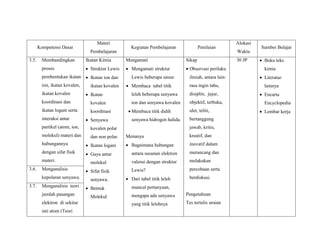
Silabus mata pelajaran kimia kelas X membahas ikatan kimia. Pokok bahasannya meliputi struktur Lewis, ikatan ion dan kovalen, ikatan koordinasi, senyawa polar dan nonpolar, ikatan logam, serta hubungan antara ikatan kimia dengan sifat fisik senyawa. Pembelajaran akan meliputi observasi, diskusi, dan percobaan tentang konsep-konsep tersebut. Penilaian mencakup sikap ilmiah, pengetahuan, dan keterampilan prakt