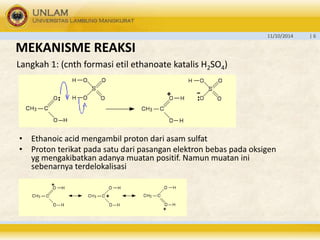
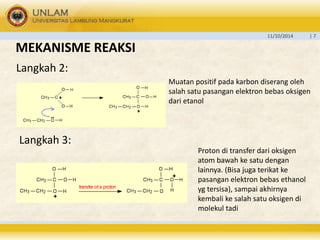
Dokumen tersebut membahas tentang esterifikasi, yaitu proses pembentukan ester dari reaksi asam karboksilat dengan alkohol menggunakan katalis asam. Ester merupakan senyawa organik yang dihasilkan dari penggantian gugus hidrogen pada asam karboksilat oleh gugus alkil atau aril dari alkohol. Contoh ester yang dijelaskan adalah etil asetat.








![11/10/2014 | 12
KINETIKA REAKSI
Usaha mempercepat reaksi
r k alkohol asam
[ ][ ]
k
Ae Ea /
RT
• Konsentrasi pereaksi harus tinggi (kemurnian tinggi; asam pekat;
alkohol ≈100%)
• Memperbesar A
Fase cair pengadukan atau pengocokan
Fase gas aliran di set turbulen
• Katalisator: asam untuk memperkecil E](https://image.slidesharecdn.com/pik2bab6esterifikasi-141110023114-conversion-gate02/85/Pik-2-bab-6_esterifikasi-12-320.jpg)



