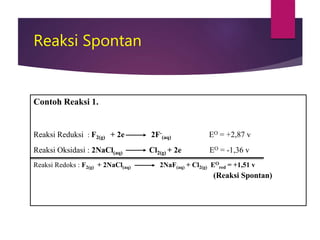
Dokumen tersebut membahas tentang sifat kimia unsur-unsur golongan halogen (VIIA) seperti fluor, klor, brom, dan iodin. Unsur-unsur ini memiliki konfigurasi elektron stabil, bentuk molekul monoatomik, dan kurang reaktif. Unsur-unsur ini digunakan dalam berbagai senyawa seperti pasta gigi, pemutih pakaian, dan obat gondok. Dokumen ini juga membahas tentang energi ionisasi, afinitas elektron,






![Konfigurasi Elektron Unsur Halogen
Berdasarkan Kulit
Unsur
Halogen
Konfigurasi
Elektron
Berdasarkan Kulit
Kulit (n) Elektron
Valensi
9F [He] 2s2 2p5 2 7
17Cl [Ne] 3s2 3p5 3 7
35Br [Ar] 3d10 4s2 4p5 4 7
53I [Kr] 4d10 5s2 5p5 5 7
86At [Ar] 4f14 5d10 6s2 6p5 6 7](https://image.slidesharecdn.com/6kimiaunsur-220227195605/85/6-kimia-unsur-8-320.jpg)