Analisis Obat
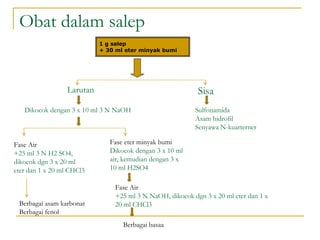
- 1. Obat dalam salep 1 g salep + 30 ml eter minyak bumi Larutan Sisa Dikocok dengan 3 x 10 ml 3 N NaOH Sulfonamida Asam hidrofil Senyawa N-kuarterner Fase Air +25 ml 3 N H2 SO4, dikocok dgn 3 x 20 ml eter dan 1 x 20 ml CHCl3 Fase eter minyak bumi Dikocok dengan 3 x 10 ml air, kemudian dengan 3 x 10 ml H2SO4 Fase Air +25 ml 3 N NaOH, dikocok dgn 3 x 20 ml eter dan 1 x 20 ml CHCl3 Berbagai asam karbonat Berbagai fenol Berbagai basaa
- 2. Tujuan analisis kualitatif senyawa obat Untuk mengidentifikasi zat-zat terutama obat yang berupa sediaan kimiawi, atau sediaan galenis dalam bentuk : 1. bubuk 2. tablet 3. Larutan, emulsi, salep, suppositora atau bentuk sediaan lain yang berupa campuran atau zat tunggal.
- 3. Penentuan Gugus Fungsionil No Gugus identifikasi Hasil 1 Alkohol Zat+As.sulfanilat+NaNO2+NaOH---merah frambos+eter---- warna masuk (aromatis); Tak masuk (alifatis) - Primer Zat + KMnO4 + H2SO4 warna hilang merah violet - Sekunder Zat + aqua brom + Nitroprusid + NH4Cl+ NH4OH merah coklat/ungu Merah coklat/ungu - Tertier Zat + HgO +H2SO4 Abu-abu Abu-abu 2. Fenol Zat + FeCL3 larutan ungu Larutan ungu 3. Aldehida Zat + Fehling A&B …..dipanaskan Merah bata 4. Keton Zat + Na-Nitroprusid + NH4Cl + NH4OH Violet 5. Karboksil Zat + alkohol+ H 2SO4 pekat…..panaskan Bau asetat 6. Inti benzen Zat + HNO3 pekat dingin + alkohol + Zn + HCl NaNO2 + Naftol dalam NH4OH Cincin merah
- 4. Asam askorbat (vit. C) Vitamin C adalah nutrien dan vitamin yang larut dalam air dan penting untuk kehidupan serta untuk menjaga kesehatan. Vitamin ini juga dikenal dengan nama kimia dari bentuk utamanya yaitu asam askorbat. Vitamin c termasuk golongan antioksidan karena sangat mudah teroksidasi oleh panas, cahaya, dan logam, oleh karena itu penggunaaan vitamin C sebagai antioksidan semakin sering dijumpai. C6H8O6 Titik leleh 190 C Pemerian : Bubuk kristal tak berwarna, rasa asam Kelarutan : air (1:4), etanol (1:25), aseton tak larut, eter tak larut, kloroform tak larut
- 5. Pemeriksaan kualitatif : Reaksi besi (III) klorida terbentuk warna ungu pada pH 6-8, bila perlu ditambahkan 1 ml larutan metanol-piridin 10%. Larutan 5 mg zat dalam 5,0 ml air menghilangkan warna 10 ml Tillmans (50 mg 2,6-diklorfenol-indofenolnatrium dalam 100 ml air). Demikian juga halnya dengan reduksi dalam keadaan dingin dari larutan garam perak amoniak, perekasi fehling, dan larutan kalium permanganat.
- 6. Sifat umum Rumus molekul sulfonamid umumnya adalah sebagai berikut : R1NH SO2NR2R3 Pada umumnya gugus amin dan gugus sulfonamid terletak pada kedudukan para satu sama lain dan R1 maupun R2 merupakan atom hidrogen sedangkan R3 merupakan gugus yang berbeda. Sulfonamid biasanya digunakan dalam sediaan berbentuk tablet, suspensi, injeksi, tetes mata dan salep mata. Sulfonamid mempunyai spektrum anti bakteri yang luas meskipun kurang kuat dibanding dengan antibiotika. Golongan Sulfonamid umumnya hanya bersifat bakteriostatik (menghambat pertumbuhan bakteri) namun pada kadar yang tinggi dalam urin Sulfonamid dapat bersifat bakterisid (membunuh kuman).
- 7. Reaksi Reaksi Umum obat gol. sulfonamida 1. Reaksi elementer terhadap C, H, S : positif 2. Reasi terhadap gugus gugus amin : reaksi diazotasi, reaksi dengan p-DAB- HCl , reaksi korek api, dan reaksi indohenol 3. Reaksi terhadap gugus sulfon : Zat + H2SO4 30% + 1 tts FeCl3 + HNO3 dan FeCl3 atau Barium Nitrat : endapan BaSO3 putih 4. Reaksi Purfurol : terhadap gugus amin bebas: 1 tts reagen (2 % purfurel dalam asam asetat ) + zat memberi warna merah tua, ungu positif kecuali sulfasuksidin, thalazol, Septazin 5. Reaksi Vanilin : Huckhal dan Turftiti Terhadap derivat metil pyridin , diatas kaca arloji atau objek : 1 tts + H2SO4 + beberapa kristal vanilin, campurkan + zat panaskan diatas nyala api kecil : kuning atau hijau muda Kecuali : sulfamerazin Na : merah tua, sulfamezathin Na : merah tua Irgamid : hijau tua – hitam dengan tepi merah
- 8. Analisis unk membedakan turunan barbiturat Reaksi zwikker positif dan kromatogramnya berwarna dg difenilkarbazon/HgCl2 positif negatif Reaksi dg pereaksi deniges Reaksi dg pereaksi deniges Positif 170-176 oC Siklobarbital Negatif 145-148 oC Heksobarbital Menghilangkan warna larutan KMnO4 basa dingin Warna merah-coklat setelah dipanaskan dengan formaldehida/asam sulfat (1:4) di penangas air Positif 170-176 oC Fenobarbital 130-135 oC Pentobarbital 188-192 oC Barbital negatif 177-180 oC metilfenobarbital