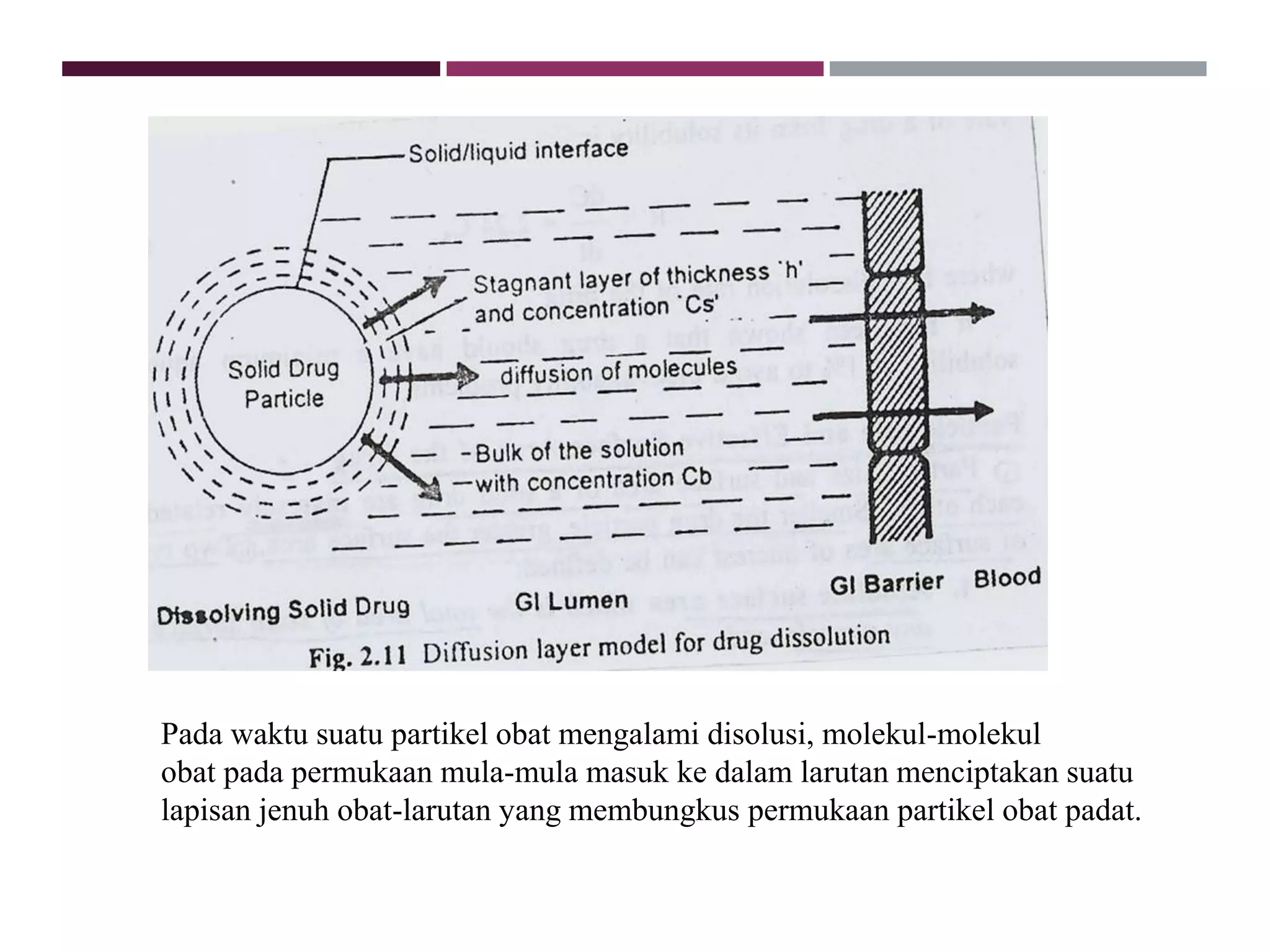
Dokumen ini membahas pengujian disolusi tablet, yang mencakup proses pelepasan zat aktif dari sediaan padat ke dalam media cair dan faktor-faktor yang mempengaruhi kecepatan disolusi. Uji disolusi digunakan untuk kontrol kualitas produk akhir dan memastikan ketersediaan hayati zat aktif. Metode, rumus, dan faktor fisikokimia serta formulasi berperan penting dalam menentukan hasil uji disolusi.