More Related Content
PDF
Αριθμός οξείδωσης, Γραφή Μ.Τ., Ονοματολογία PPTX
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΕΝΟΤΗΤΑ 1 (ΟΞΕΑ-ΒΑΣΕΙΣ-ΑΛΑΤΑ).pptx DOC
ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Α΄ ΛΥΚΕΙΟΥ DOC
Ν. Γλώσσα Β΄ Γυμνασίου, Εργασία-επάγγελμα-ανεργία PDF
10 Ασκήσεις στο Νόμο του Coulomb PDF
ερωτησεισ γεωγραφιασ β κεφαλαιου PDF
PDF
Χημικές αντιδράσεις Α΄ Λυκείου What's hot
PDF
Διαγώνισμα Χημείας Γ' Γυμνασίου (Ενότητα 1 - Οξέα / Βάσεις / Άλατα / Εξουδετέ... PDF
[Φυσική Γ' Γυμνασίου] Σύνοψη θεωρίας για όλη την ύλη PDF
ΠΛΑΓΙΕΣ ΕΡΩΤΗΜΑΤΙΚΕΣ ΠΡΟΤΑΣΕΙΣ PDF
Θεματα Βιολογιας α΄ Γυμνασίου PDF
Λεξιλογικός πίνακας "άγω", ενότητα 5 Αρχαίων Β΄ Γυμνασίου PPTX
DOC
ΒΙΟΛΟΓΙΑ Α ΓΥΜΝ- Διαγώνισμα Α τρίμηνο_Α ΟΜΑΔΑ DOCX
DOC
διαγωνισμα βιολογια α γυμνασιου β τριμηνου 2013 PDF
Διαγώνισμα Χημείας Γ γυμνασίου PDF
τυπολογιο φυσικησ β΄λυκειου ηλεκτρικο πεδιο DOC
ΧΗΜΕΙΑ Β ΓΥΜΝ- ΔΙΑΓΩΝΙΣΜΑ Α ΤΡΙΜ_Α ΟΜΑΔΑ PDF
Iστορία του Mεσαιωνικού & Nεότερου Kόσμου - Tράπεζα Θεμάτων : 2ο κεφάλαιο PDF
Δομικά σωματίδια της ύλης - Δομή του ατόμου PPTX
Σύμβολα χημικών στοιχείων και χημικών ενώσεων PDF
Χημεία Α' Λυκείου - Βασικές έννοιες (Inter learning) PDF
PDF
2ο κεφάλαιο χημεία β λυκείου γενικής παιδείας ασκήσεις 2014_2015 PPTX
Εξουδετέρωση οξέων βάσεων PPTX
Viewers also liked
PPTX
Το κυτταρο Κεφαλαιο 1 Βιολογια Γυμνασιου PPTX
PDF
Περιοδικός Πίνακας Γ' Γυμνασίου DOCX
φύλλο εργασίας το ερειστικό σύστημα του ανθρώπου PDF
Τα μέταλλα (Γ' Γυμνασίου) PDF
Θέματα χημείας γ΄ Γυμνασιου PPTX
PPTX
PPTX
Φωτοσύνθεση: Ιστορική Αναδρομή PPTX
ΒΙΟΜΗΧΑΝΙΚΟ ΜΟΥΣΕΙΟ ΦΩΤΑΕΡΙΟΥ - Γκάζι, Τεχνόπολη DOC
Aσκήσεις χριστουγέννων για τη γ γυμνασίου Similar to άλατα
PDF
Ερωτήσεις-Ασκήσεις στις χημικές αντιδράσεις Α΄Λυκείου PDF
οξέα βάσεις-κλίμακα pH-εξουδετέρωση PDF
αντιδράσεις οξείδωσης αναγωγής οργανικών ενώσεων PDF
Eρωτήσεις, ασκήσεις, αντιδράσεις,, διακρίσεις, ... (β λυκείου, χημεία, γενικό... PPSX
αντιδράσεις υποκατάστασης PPTX
Xhmikes antidraseis stoixeiometria mole PPTX
PDF
γενικο διαγωνισμα στη χημεια γ λυκ (θετ. κατ) PPT
Θεωρία Ηλεκτρολυτικής Διάστασης PPTX
PDF
τρίωρη γραπτή εξέταση στο 1ο κεφ. της χημείας β΄ λυκ (γπ) PDF
erotiseis_chem_c_gym .pdf PPTX
Oxea baseis alata_v_11.02 PDF
βιντεο θαυμαστου κοσμου της χημειας PDF
γραπτη εξεταση στη χημεια γ PPTX
91 - Ανίχνευση ιόντων - 2. PPTX
DOC
PDF
PPT
Διεθνές Έτος Χημείας, 2011 More from Petros Karapetros
PPTX
PPTX
PPTX
PPTX
PPTX
Παράγοντες που επηρεάζουν την ταχύτητα αντίδρασης PPTX
Tεχνολογία Aνασυνδυασμένου DNA PPTX
Κεφάλαι 5: Μενδελική κληρονομικότητα PPTX
Kεφάλαιο 1: Το γενετικό υλικό PPTX
2o Κεφάλαιο: Αντιγραφή και έκφραση της γενετικής πληροφορίας PPTX
PPTX
DOCX
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΒΙΟΛΟΓΙΑΣ Β ΛΥΚΕΙΟΥ PPTX
Iσοστάθμιση χημικής εξίσωσης PPT
PPS
PDF
Δράσεις 1ου ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ 2017-2018 PDF
Let's do it Greece: Δράσεις 1ου ΓΕΛ ΧΛΑΝΔΡΙΟΥ άλατα
- 1.
- 2.
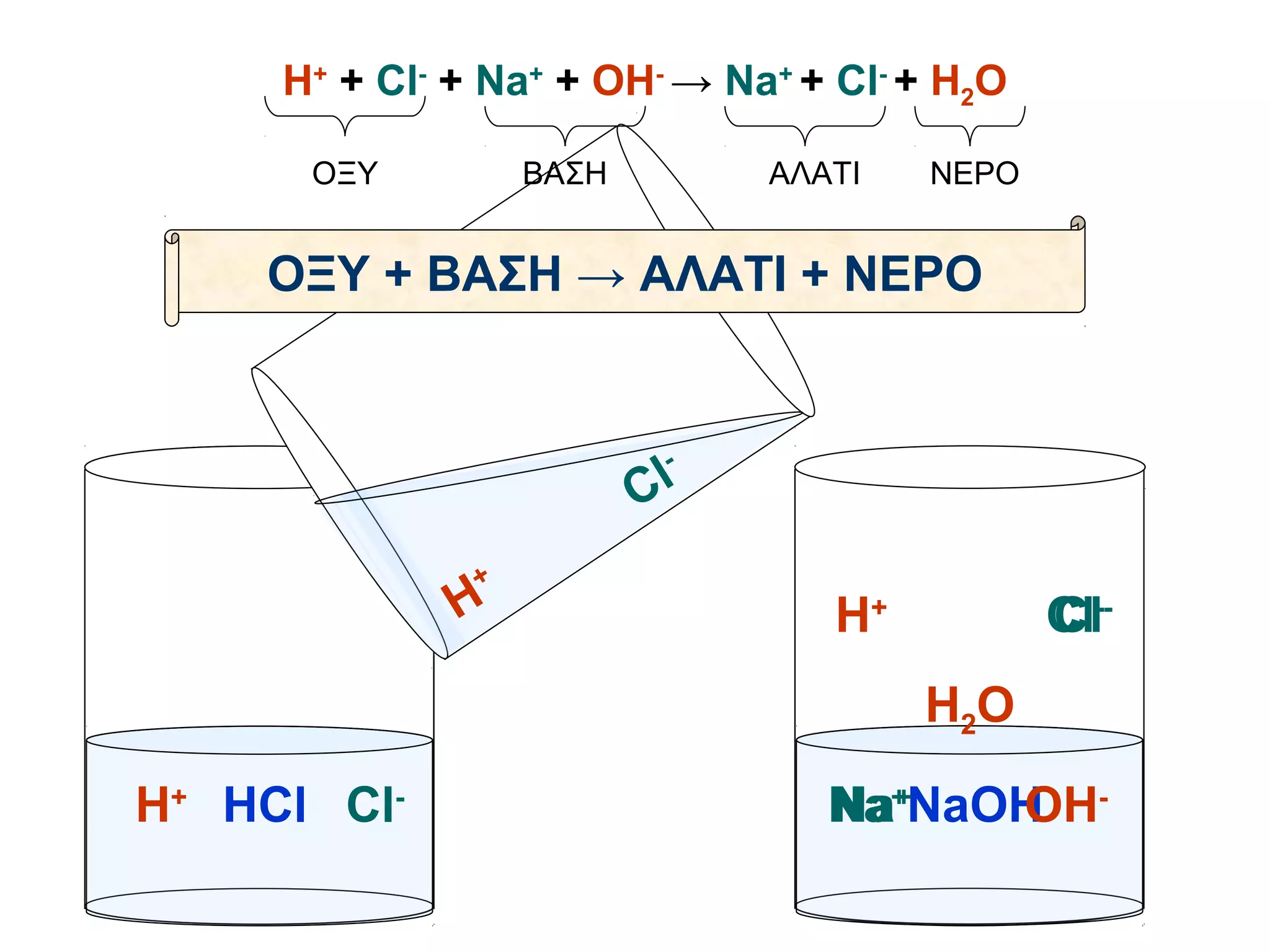
Η+ + Cl-+ Na+ + OH- → Na+ + Cl- + H2O
ΟΞΥ ΒΑΣΗ ΑΛΑΤΙ ΝΕΡΟ
ΟΞΥ + ΒΑΣΗ → ΑΛΑΤΙ + ΝΕΡΟ
Cl-
+
H H+ Cl--
Cl
Η2Ο
H+ HCl Cl- Na+NaOH -
+
OH
- 3.
Η+ + Cl-+ Na+ + OH- → Na+ + Cl- + H2O
ΟΞΥ ΒΑΣΗ ΑΛΑΤΙ ΝΕΡΟ
ΟΞΥ + ΒΑΣΗ → ΑΛΑΤΙ + ΝΕΡΟ
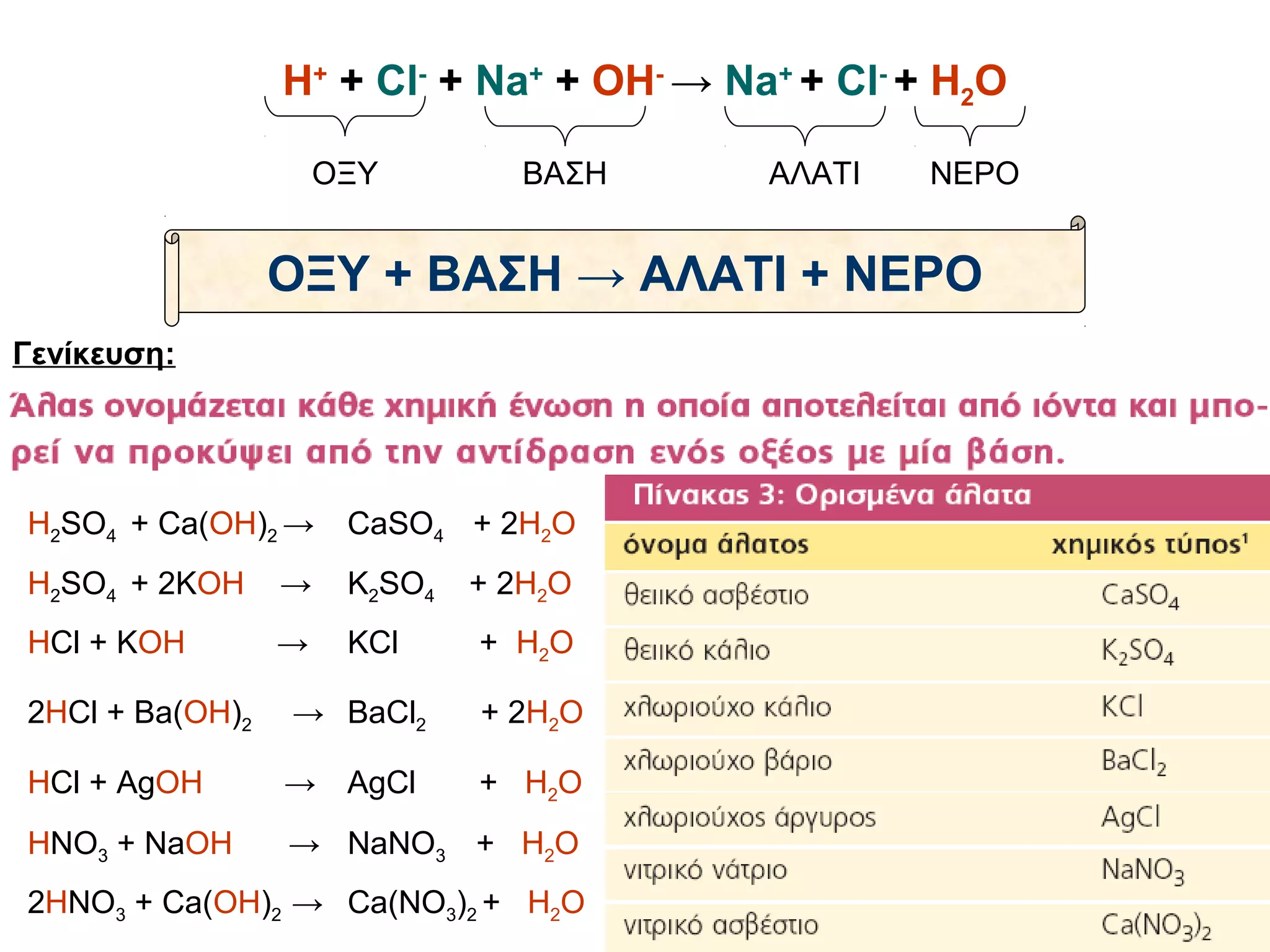
Γενίκευση:
H2SO4 + Ca(OH)2 → CaSO4 + 2H2O Θειικό οξύ + υδροξείδιο του ασβεστίου → Θειικό ασβέστιο
H2SO4 + 2KOH → K2SO4 + 2H2O Θειικό οξύ + υδροξείδιο του καλίου → Θειικό κάλιο
HCl + KOH → KCl + H2O υδροχλώριο + υδροξείδιο του καλίου → χλωριούχο κάλιο
2HCl + Ba(OH)2 → BaCl2 + 2H2O υδροχλώριο + υδροξείδιο του βαρίου → χλωριούχο βάριο
HCl + AgOH → AgCl + H2O υδροχλώριο + υδροξείδιο του αργύρου → χλωριούχος άργυρος
HNO3 + NaOH → NaNO3 + H2O νιτρικό οξύ + υδροξείδιο του νατρίου → νιτρικό νάτριο
2HNO3 + Ca(OH)2 → Ca(NO3)2 + H2O νιτρικό οξύ + υδροξείδιο του ασβεστίου → νιτρικό ασβέστιο
- 4.
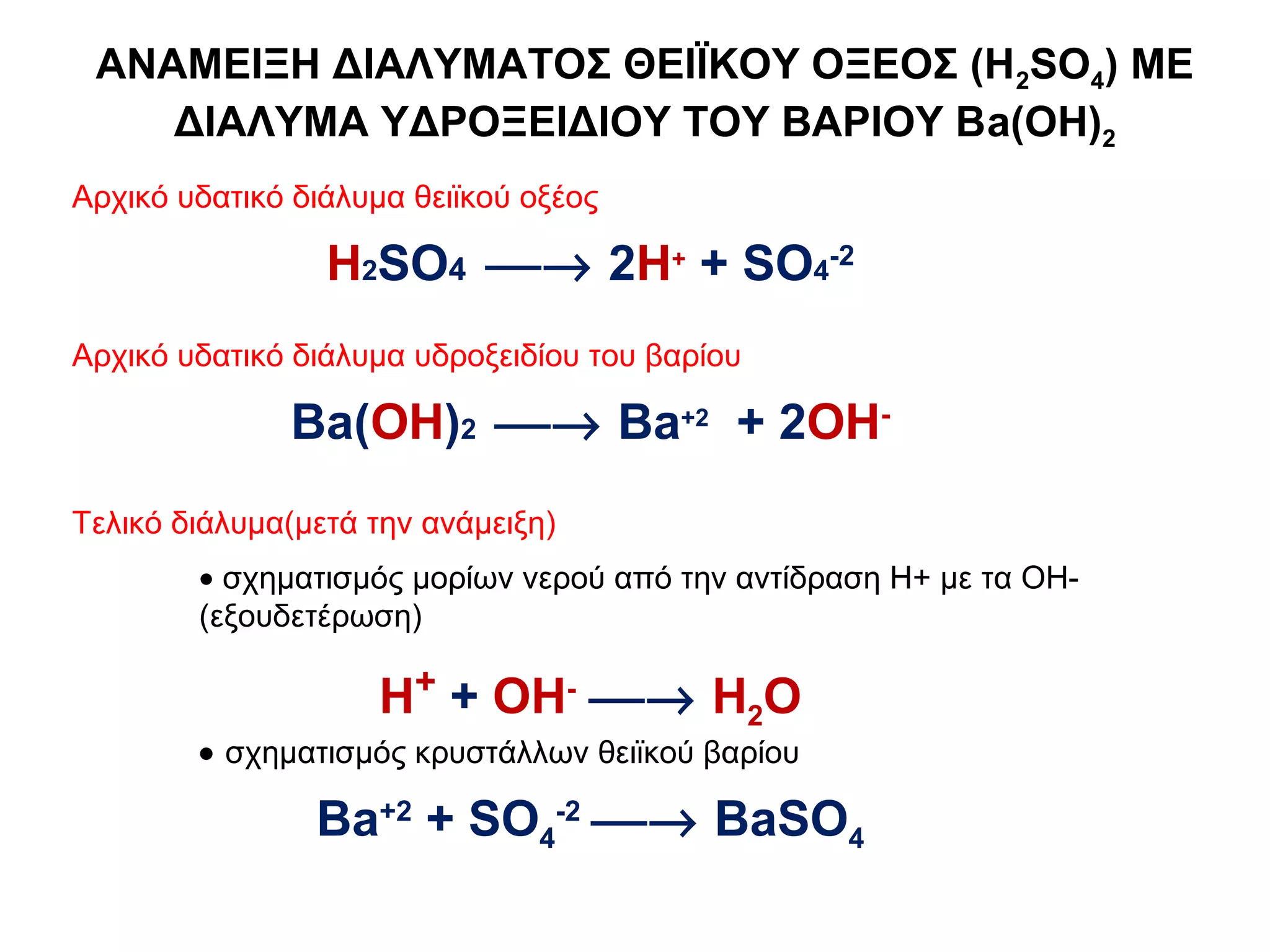
ΑΝΑΜΕΙΞΗ ΔΙΑΛΥΜΑΤΟΣ ΘΕΙΪΚΟΥΟΞΕΟΣ (Η2SO4) ME
ΔΙΑΛΥΜΑ ΥΔΡΟΞΕΙΔΙΟΥ ΤΟΥ ΒΑΡΙΟΥ Βa(ΟΗ)2
Αρχικό υδατικό διάλυμα θειϊκού οξέος
Η2SO4 → 2H+ + SO4-2
Αρχικό υδατικό διάλυμα υδροξειδίου του βαρίου
Βa(OH)2 → Ba+2 + 2OH-
Τελικό διάλυμα(μετά την ανάμειξη)
• σχηματισμός μορίων νερού από την αντίδραση Η+ με τα ΟΗ-
(εξουδετέρωση)
Η+ + ΟΗ- → H2Ο
• σχηματισμός κρυστάλλων θειϊκού βαρίου
Βa+2 + SO4-2 → BaSO4
- 5.
2Η+ + SO4-2+ Ba+ + 2OH- → Ba+ + SO4-2 + 2H2O
ΟΞΥ ΒΑΣΗ ΑΛΑΤΙ ΝΕΡΟ
ΟΞΥ + ΒΑΣΗ → ΑΛΑΤΙ + ΝΕΡΟ