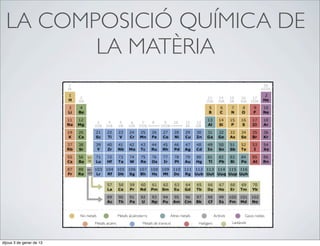
03. La composició química de la matèria viva
- 1. LA COMPOSICIÓ QUÍMICA DE LA MATÈRIA No metalls Metalls alcalinoterris Altres metalls Actínids Gasos nobles Metalls alcalins Metalls de transició Halògens Lantànids dijous 3 de gener de 13
- 2. La composició química de la matèria viva Els conceptes químics fonamentals per entendre la composició de la matèria són: element químic, àtom, molècula, substància composta i enllaç químic dijous 3 de gener de 13
- 3. La composició química de la matèria viva Els elements químics, els àtoms i les molècules Element químic o substància simple: És una substància que no es pot descompondre en d’altres mitjançant reaccions químiques. Està constituïda per un sol tipus d’àtoms Hidrogen H Carboni C Oxigen O Nitrogen N 104 elements químics, 15 dels quals no es troben en la naturalesa, s’obtenen artificialment dijous 3 de gener de 13
- 4. La composició química de la matèria viva Els elements químics, els àtoms i les molècules És la part més petita Àtom: d’un element químic Electró Protons: Partícula de càrrega elèctrica positiva, que juntament amb Protó els neutrons, constitueixen el nucli dels àtoms Neutrons: Partícula sense càrrega elèctrica, que juntament amb els neutrons, constitueixen el nucli dels Neutró àtoms Electrons: Partícula sense càrrega elèctrica negativa que forma part dels àtoms. Es troba en l’escorça i té una massa molt petita comparada amb la massa total d’un àtom dijous 3 de gener de 13
- 5. La composició química de la matèria viva Els elements químics, els àtoms i les molècules Hidrogen H · 1e-, 1p, 0n Nombre atòmic = 1 ·· Oxigen · O · · · Pes atòmic = 1 8e-, 8p, 8n Nombre atòmic = 8 Pes atòmic = 16 · · · Carboni · C · Nitrogen · N · · · · 6e-, 6p, 6n 7e-, 7p, 7n Nombre atòmic = 6 Nombre atòmic = 7 Pes atòmic = 12 Pes atòmic = 14 dijous 3 de gener de 13
- 6. La composició química de la matèria viva Els elements químics, els àtoms i les molècules Molècula: És la unió de dos o més àtoms. Electró Molècules homogènies: Els àtoms de Protó la molècula són del mateix tipus O2 N2 H2 Molècules heterogènies: Els àroms Neutró de la molècula són diferents H2O NaCl CH4 dijous 3 de gener de 13
- 7. La composició química de la matèria viva Els elements químics, els àtoms i les molècules Substància composta: Electró Protó És la formada per dos o més elements químics La seva part més petita és una Neutró molècula heterogènia, formada per àtoms de diferents tipus dijous 3 de gener de 13
- 8. La composició química de la matèria viva Els enllaços quimics És la unió entre àtoms, molèules o ions En la matèria viva els principals tipus d’enllaços són: Enllaç iònic: Entre ions Enllaç covalent: Entre àtoms Enllaços intermoleculars: Entre molècules dijous 3 de gener de 13
- 9. La composició química de la matèria viva Els enllaços quimics Ió negatiu o anió: Àtom Enllaç iònic Un dels àtoms capta que capta electrons electrons de l’altre Llei de l’octet: Els àtoms tendeixen a Ió positiu o catió: Àtom tenir 8 electrons en el seu últim que perd electrons orbital, excepte l’hidrogen, que en té 2 L’anió i el catió queden units per forces electrostàtiques Element químic electropositiu o metàlic: Els àtom que tenen menys de 4 electrons en el seu últim orbital, que tendeixen a donar-los i quedar-se en càrrega positiva L’enllaç iònic es dóna entre àtoms Element químic electronegatiu o no metàlic: d’electronegativitat molt diferent Els àtom que tenen més de 4 electrons en el seu últim orbital, que tendeixen a captar-los i quedar-se en càrrega negativa dijous 3 de gener de 13
- 10. La composició química de la matèria viva Els enllaços quimics Enllaç iònic NaCl Na+ (catió) Clorur sòdic Cl- (anió) Xarxa cúbica del NaCl dijous 3 de gener de 13
- 11. La composició química de la matèria viva Els enllaços quimics Enllaç covalent Enllaç covalent: Cada parell d’electrons compartits, que Es forma quan dos àtoms giren al voltant dels dos nuclis comparteixen electrons atòmics Molècules apolars: Entre molècules d’electronegativitat alta i similar Compostos formats per àtoms iguals Hidrocarburs Hidrogen molecular (H2) Metà (CH2) Nitrogen molecular (N2) Oxigen molecular (O2) dijous 3 de gener de 13
- 12. La composició química de la matèria viva Els enllaços quimics Enllaç covalent Enllaç covalent: Cada parell d’electrons compartits, que Es forma quan dos àtoms giren al voltant dels dos nuclis comparteixen electrons atòmics Molècules polars: Entre molècules d’electronegativitat alta i diferent, on uns àtoms atrauen més cap a si els electrons Molècules dipolars: Pol positiu i pol negatiu Aigua (H2O) Aigua: H2O dijous 3 de gener de 13
- 13. La composició química de la matèria viva Els enllaços quimics Enllaç covalent Hidrogen molecular (H2) Nitrogen molecular (N2) Oxigen molecular (O2) Metà (CH2) Aigua (H2O) dijous 3 de gener de 13
- 14. La composició química de la matèria viva Els enllaços quimics Enllaç covalent apolar Oxigen molecular (O2) Comparació de la distribució de càrregues en els diferents tipus d’enllaços Enllaç iònic Enllaç covalent apolar Enllaç covalent polar dijous 3 de gener de 13
- 15. La composició química de la matèria viva Els enllaços quimics Enllaços intermoleculars Són els enllaços entre molècules Enllaç d’hidrogen Forces de Van der Waals Es dóna entre molècules apolars, la Entre molècules dipolars dels hidrurs, degut distribució electrònica, per atzar es a la mida petita de l’àtom d’hidrogen torna assimètrica Espontàniament Molècula no Molècula polaritzada polaritzada (dipol instantani) Inducció de la polarització a la molècula veïna dijous 3 de gener de 13
