Quimica
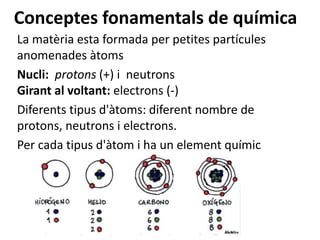
- 1. Conceptes fonamentals de química La matèria esta formada per petites partícules anomenades àtoms Nucli: protons (+) i neutrons Girant al voltant: electrons (-) Diferents tipus d'àtoms: diferent nombre de protons, neutrons i electrons. Per cada tipus d'àtom i ha un element químic
- 2. Element químic: Substància pura que no es pot separar més en altres més simples per mètodes químics. Compost químic: Substància pura que encara es pot separar en altres més simples por mètodes químics. Elements i compostos Hi ha 118 Els àtoms s’uneixen formant molècules
- 3. Nombre atòmic (Z): Nº de protons d’ un àtom. Cada element té un Z diferent. • Àtom neutre: mateix nº de protons que d’electrons • Ió: Àtom amb diferent nº d'electrons que de protons Catió (+): Àtom que ha perdut electrons Anió (-): Àtom que ha guanyat electrons - Els protons no es poden perdre ni guanyar Catió: Na+ Anió: Cl-
- 4. • Es la suma de protons i neutrons del nucli • En el nucli resideix quasi tota la massa de l'àtom. Els electrons quasi no tenen massa • Isòtops: Àtoms amb mateix nº de protons però diferent nº de neutrons Nombre màssic (A):
- 5. Exercici 1: Estructura atòmica 4- Completa la següent taula: Símbol Mn Ca Nom Carboni Brom Nombre atòmic 25 35 Nombre màssic 55 80 Nombre de protons 6 Nombre de neutrons 6 20 Nombre d’electrons 20
- 6. Exercici 2: Estructura atòmica Diu si són veritables o falses les següents afirmacions, explicant la resposta en cada cas a) Un isòtop és un àtom que no té neutrons b) El nucli està format per protons i electrons. c) Tots els components de l'àtom tenen càrrega elèctrica. d) Els àtoms amb càrrega positiva s’anomenen ions. i) Els àtoms amb càrrega negativa s’anomenen cations. f) El nombre atòmic indica el nombre de protons i de neutrons d'un àtom. g) Dos àtoms de clor han de tenir el mateix nombre de neutrons. h) El neutró no té massa. i) La massa dels protons i la dels electrons és d'igual valor. j) La càrrega elèctrica dels protons i els neutrons és la mateixa.
- 7. • A la massa de l’àtom la denominem massa atòmica. Es pren com a referència l'àtom de C • Es calcula fent la mitjana aritmètica ponderada dels isòtops d’un element Per això la massa atòmica d’un element no es un número sencer. Es poden trobar a la taula periòdica Massa atòmica:
- 8. Exercici: Càlcul de massa atòmica El Mg té 3 isòtops. Dada la seva abundància calcula la seva massa atòmica
- 9. Exercici 3: Massa atòmica El neó té 2 isòtops: un amb 10 protons, 10 neutrons i abundància del 91% i un altre amb 10 protons i 12 neutrons i abundància del 9%. ¿Quina és la massa atòmica mitjana ponderada del neó?
- 10. Massa molecular • La massa molecular es la massa que té una molècula • Per determinar la massa molecular sumarem les masses atòmiques de tots els àtoms que constitueixen la molècula.
- 11. Exercici 4: Massa molecular Calcula la massa molecular de les següents substàncies: a) Na2CO3 b) CdSO4 c) K2CrO7
- 12. El mol • Per relacionar la mesura de massa utilitzada en el laboratori (grams) amb les masses atòmiques i moleculars utilitzem el mol. Mol : quantitat de substància que conté 6,023 x 1023 unitats d’eixa substància.
- 13. Exercici resolt Un químic vol saber quants gram ha de pesar per tenir 1,5 mols de clorur de calci (CaCl2) ¿Pots ajudar-lo? Massa atòmica del Ca = 40,07 u.m.a. Massa atòmica del Cl = 35,453 u.m.a. Massa molecular CaCl2 = (40,07) + 2 (35,45) = 110,97 massa (g) = mols x massa molecular (g/mol) (1,5 mol) x (110,984 grams / mol) = 166,45 grams de CaCl2
- 14. Exercici resolt • Si tingués 2,8 grams d'or, quants àtoms d'or tindria? Au = 196,97 u.m.a. (2,8 grams) / (196,97 grams/mol) = 0,0142 mols Segons el nombre d'Avogadro en un mol d’or hi ha aproximadament 6,023 x 1023 àtoms. Per la qual cosa, en 0,0142 mols tindrem: (0,0142 mols) (6,023 x 1023 àtoms / mols) = 8,55 x1021 àtoms
- 15. Exercici 5: Mols i àtoms • Tenim 36 g de Fe2O3 ¿quants àtoms de ferro i quants d’oxigen tenim?
- 16. Composició centesimal La composició centesimal d'un compost és el tant per cent (%) en massa de cada un dels elements que el componen. Indice: nº àtoms del element
- 17. Exercici 6: Composició centesimal • Calcula el percentatge d'oxigen present en el àcid nítric (HNO3) ¿ Quin serà el percentatge del nitrogen? • ¿ I d’oxigen en el NaOH?
- 18. Fórmula empírica • Pot ser que coneguem la composició centesimal d’un compost però no la seva fórmula. • Fórmula empírica: proporció més simple entre els àtoms que formen un compost químic • Sempre serà entre números sencers EXEMPLES: H20 2 H: 1 O KClO3 : 1 K : 1 Cl : 3 O N2O4: 2 N : 4 O 1 N : 2 O (Es pot dividir entre 2)
- 19. Càlcul de la fórmula empírica • Es farà sempre per a 100 g de compost Exercici: S'analitza un compost de C i H obtenint-se un 80,0% de C i un 20,0% d'hidrogen. Calcula la seva fórmula empírica - Calcularem el número de mols de cada element per a 100 g 8O g de C 20 g de H Mol= 80g/12 uma = 6,67 mols de C Mol= 20 g/1 uma = 20 mols de H - Dividirem els mols dels elements entre el de menor número de mols i aproximaren al valors sencers La proporció mes simple serà = 1C : 3H La fórmula empírica serà = CH3
- 20. Exercici 7: Fórmula empírica Un compost conté 63,1% C, 11,92% d'H i 24,97 de F .Calcula la fórmula empírica del compost
- 21. Fórmula molecular • Formula molecular: Es la fórmula real del compost a la natura. • Sorgeix de multiplicar la fórmula empírica per un número sencer X 2 X 1 X 2
- 22. Càlcul fórmula molecular • Necessitem que ens diguin la massa molecular del compost Exercici: S'analitza un compost de C i H obtenint-se un 80,0% de C i un 20,0% d'hidrogen. Calcula la seva fórmula molecular sabent que te una massa molecular de 45 uma. Calcularem la fórmula empírica com abans: CH3 Calcularem la massa molecular dels seus múltiples: CH3 = 12 (C) + 3 (H) = 15 uma C2H6 = 24 (C) + 6(H) = 30 uma C3 H9 = 36 (C) + 9 (H) = 45 uma C4 H12 = 48 (C) + 12 (H) = 60 uma El compost que estem analitzant serà C3H9
- 23. Un compost té la següent composició en tant per cent: 19,3% de Na, 26,9% S i 53,8% d'O. El seu pes molecular és 238. Calcula la fórmula molecular. Exercici 8: Fórmula molecular
- 24. Completa: 1) Quan en la descripció d’un compost únicament s'indica la proporció d'àtoms dels diferents elements que el constitueixen, la fórmula es diu fórmula ............. 2) La fórmula que indica el tipus i nombre d'àtoms que constitueixen una molècula es diu fórmula …………… Exercici 9: Fórmules
