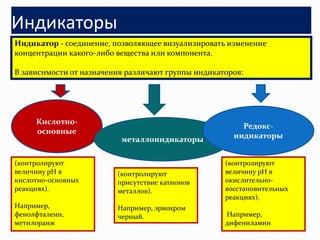
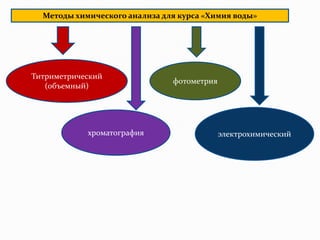
Документ представляет лекцию о показателях качества природной воды, включая анализ питьевой и сточной воды. В нем рассматриваются физико-химические параметры, такие как мутность, цветность, запах и вкусовые качества, а также методы их определения. Особое внимание уделяется санитарным требованиям и методологиям химического анализа для контроля качества воды.





















![Закон эквивалентов Дальтона
Вещества реагируют между собой в эквивалентных количествах
(или согласно своим химическим эквивалентам): n1 = n2 .
Используя данный закон можно определять концентрации растворов.
Выразим эквиваленты веществ через их нормальные концентрации:
n = CН∙V .
Тогда для двух реагирующих соединений, в соответствии с законом Дальтона
имеем: Cн1∙V1 = Cн2∙V2 .
По данной формуле можно рассчитать неизвестную концентрацию определяемого
вещества Cн2 если известна концентрация другого вещества, а так же определены
объёмы реагирующих веществ:
Cн2 = Cн1∙V1/V2 .
Сущность метода основана на точном измерении количества
реактива, израсходованного на реакцию с определяемым
веществом.
Название метода произошло от слова «титр».
Титр – один из видов массовой концентрации, в переводе с французского означает - титул,
качество.
Титр показывает число граммов растворенного вещества в 1 мл раствора (титр по исходному веществу) ;
[г/мл]](https://image.slidesharecdn.com/2-120218233151-phpapp02/85/slide-24-320.jpg)





















