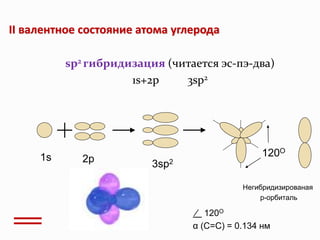
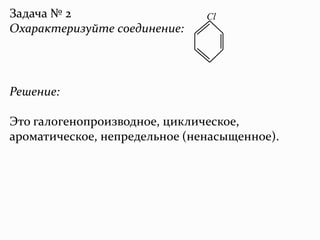
Документ представляет собой лекцию о теории химического строения органических соединений, разработанной А.М. Бутлеровым, рассматривая важность углерода и его валентности в органике. Рассматриваются классификация органических веществ и типы химических реакций, включая механизмы разрыва ковалентных связей. Лекция также охватывает связь между структурой молекул и их свойствами.