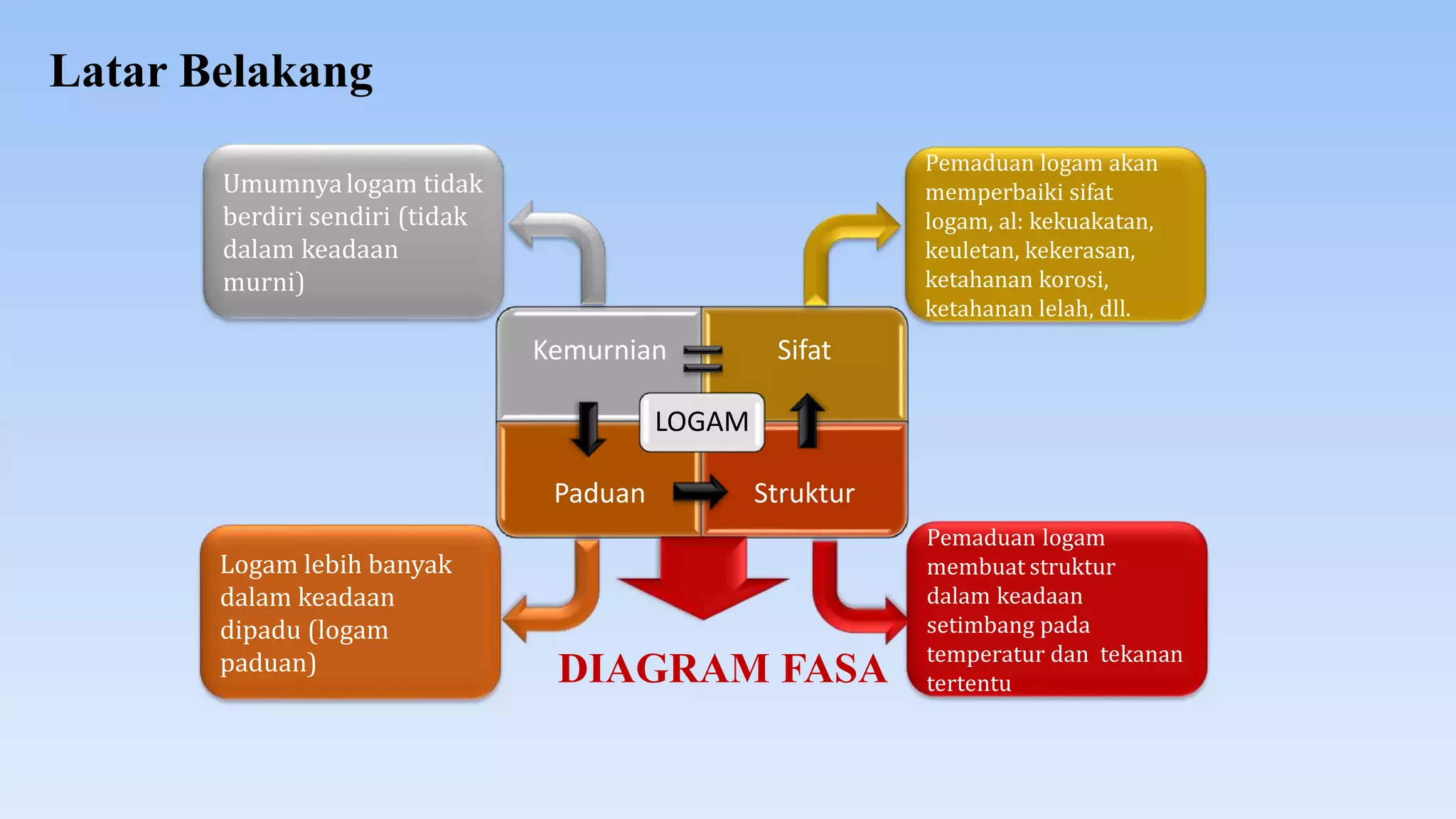
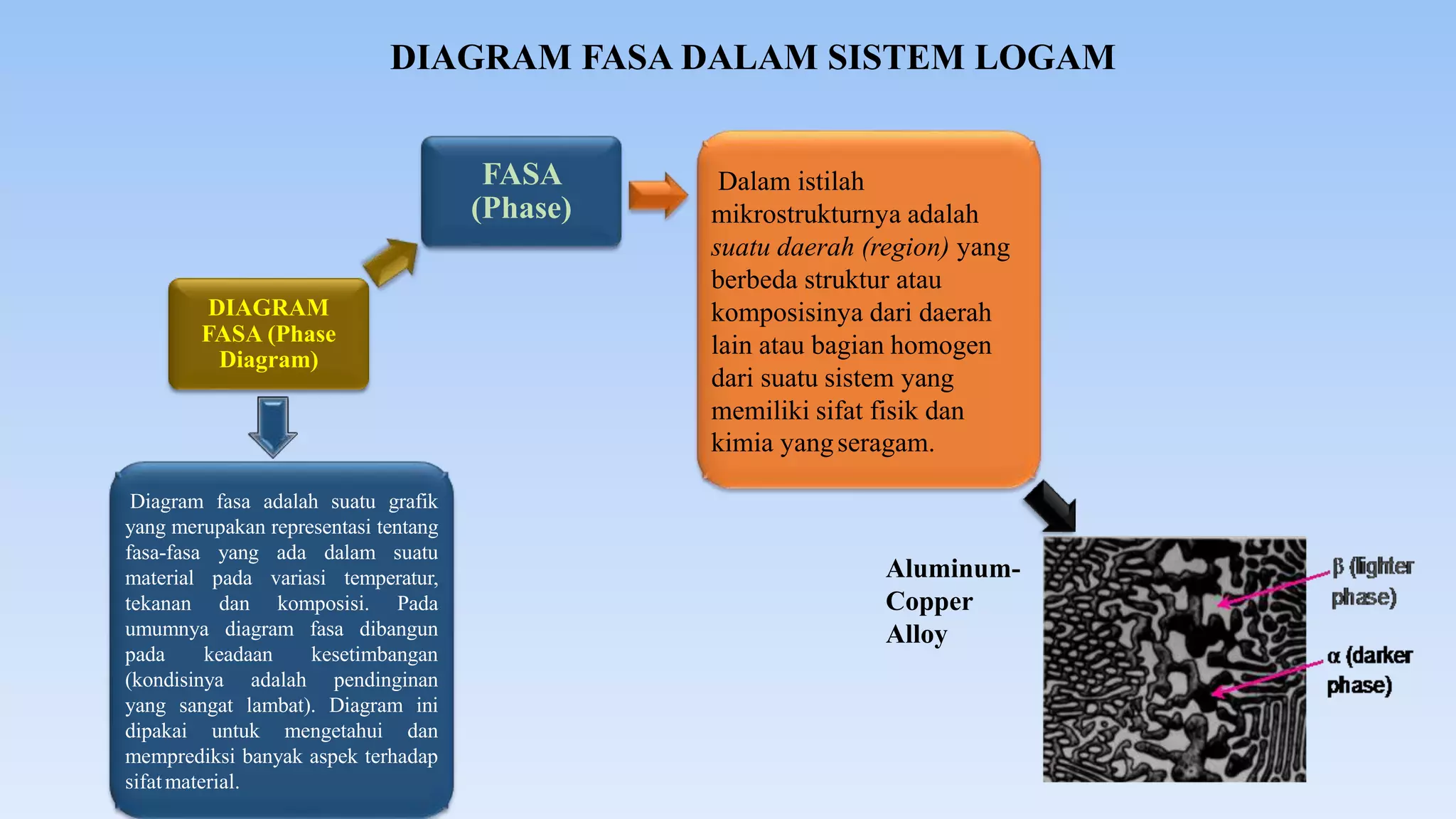
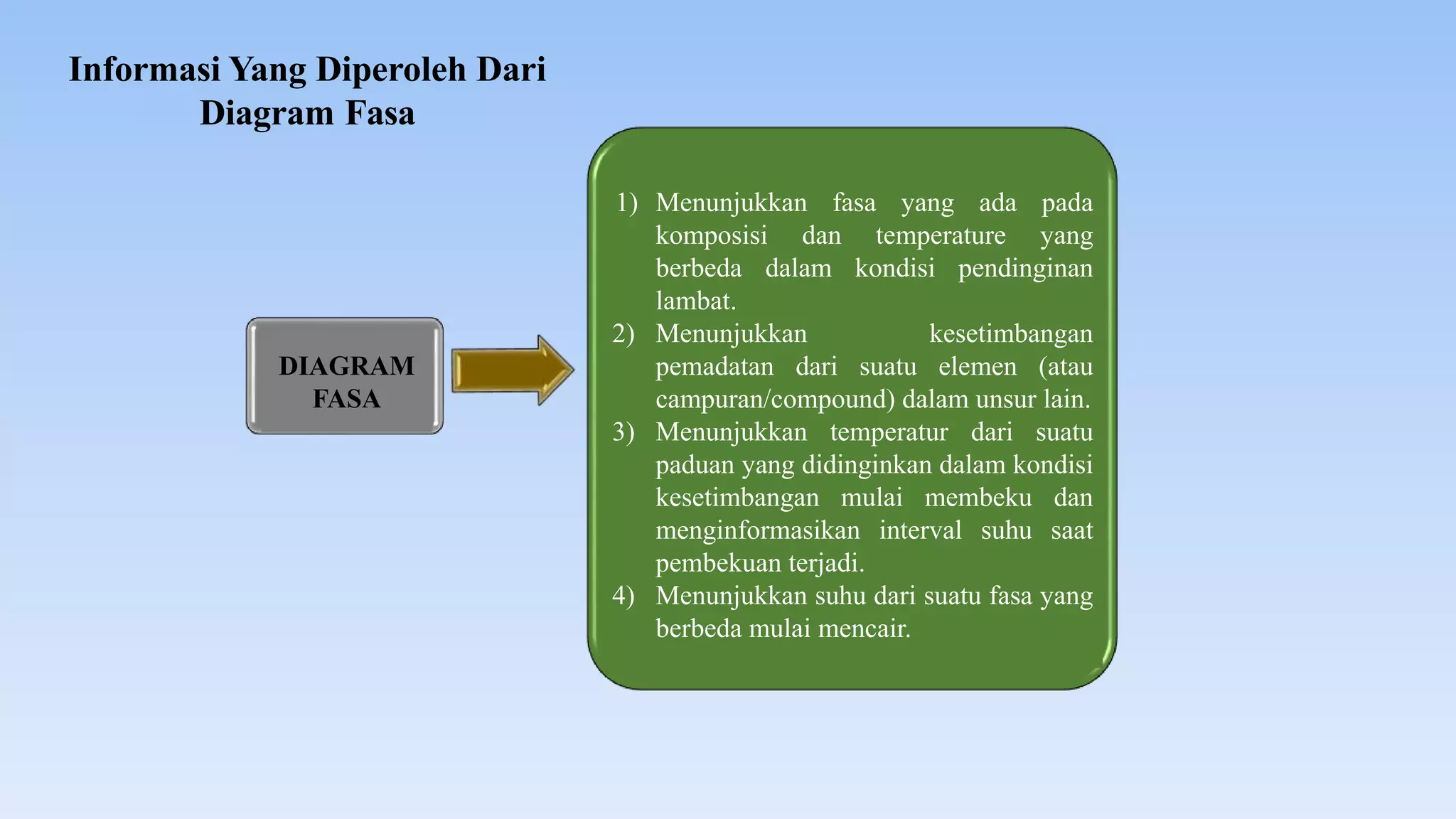
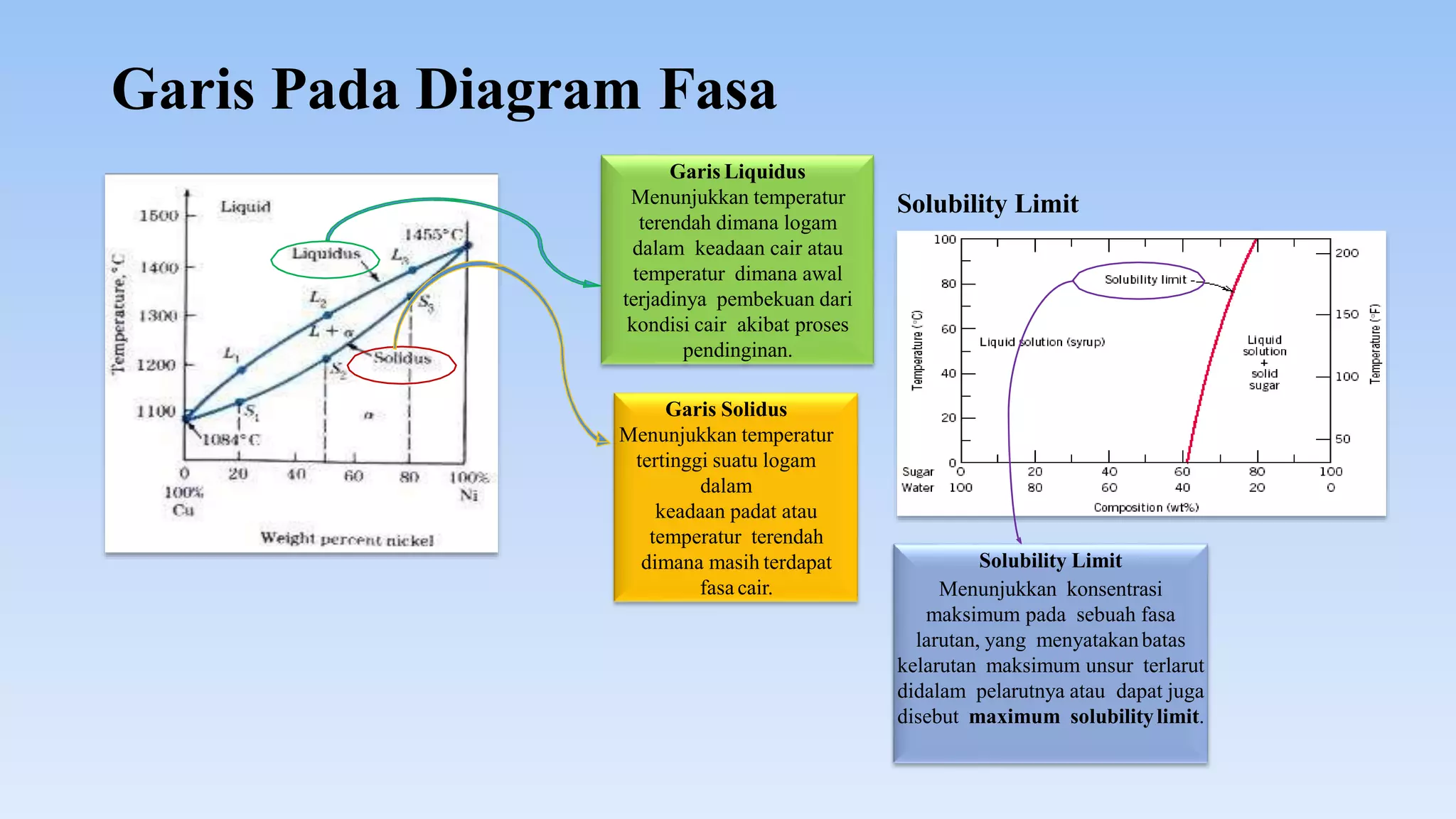
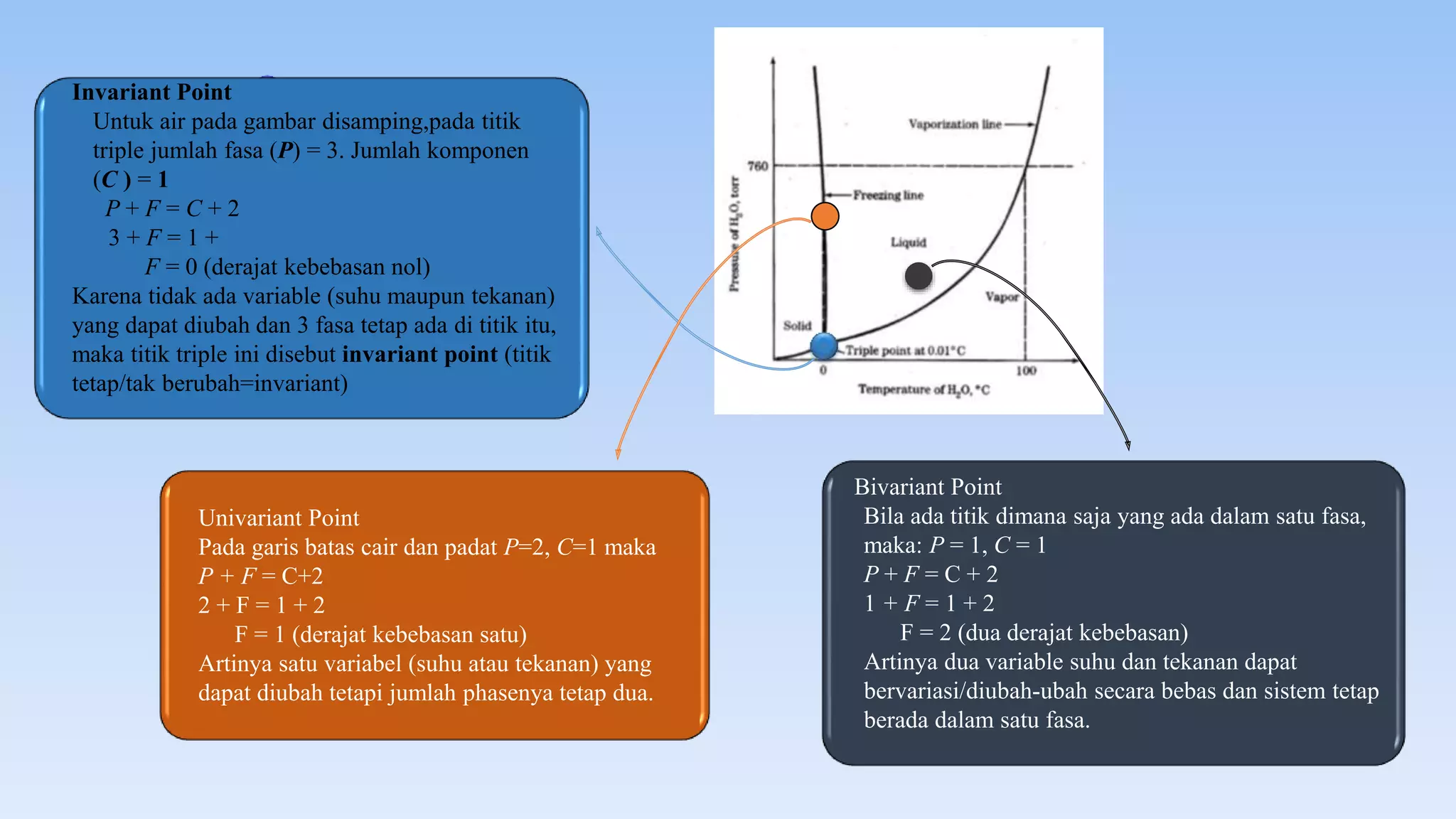
Dokumen ini membahas diagram fasa dalam metalurgi fisik yang menggambarkan interaksi antara temperatur, tekanan, dan komposisi logam paduan. Diagram fasa digunakan untuk menentukan sifat-sifat material dan kesetimbangan fasa saat proses pendinginan. Selain itu, dijelaskan tentang hukum fasa Gibbs dan kaidah lengan untuk menentukan jumlah dan jenis fasa dalam sistem logam.