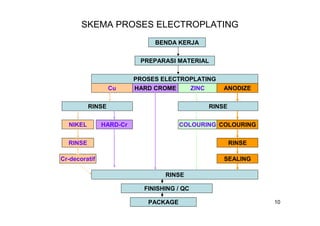
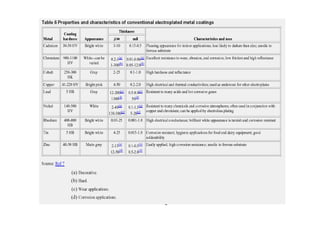
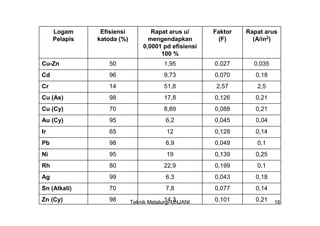
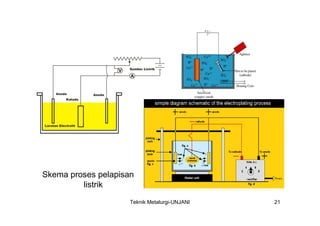
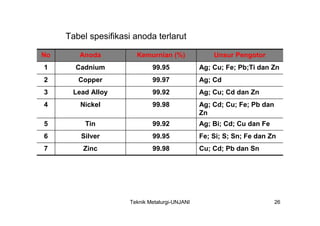
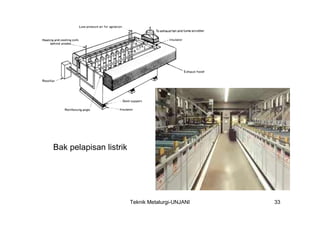
Dokumen ini membahas proses elektroplating, termasuk definisi, tujuan, dan teknik pelapisan logam untuk meningkatkan ketahanan korosi, tampak rupa, dan kehalusan permukaan. Ditekankan juga mengenai proses persiapan yang melibatkan pembersihan dan pencucian, serta pentingnya larutan elektrolit dan parameter proses seperti rapat arus dan temperatur. Serta, diuraikan kelebihan dan kekurangan elektroplating dibandingkan metode pelapisan lainnya.