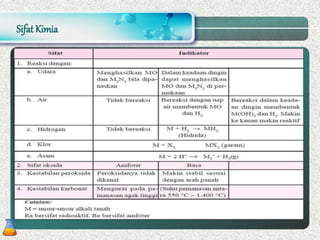
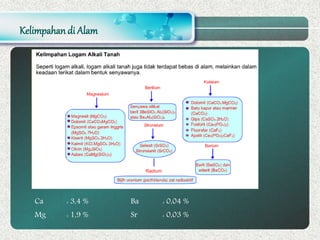
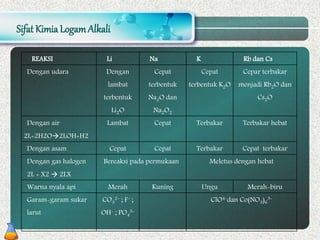
Dokumen ini membahas tentang sifat, kelimpahan, kegunaan, dan kerugian logam alkali dan alkali tanah, serta metode pembuatan mereka. Logam alkali sangat reaktif dan memiliki berbagai aplikasi, tetapi juga memiliki risiko kesehatan. Logam alkali tanah memiliki sifat yang mirip tetapi dengan dua elektron valensi, serta kegunaan yang bervariasi dalam industri dan kesehatan.





















![Sifat Fisika
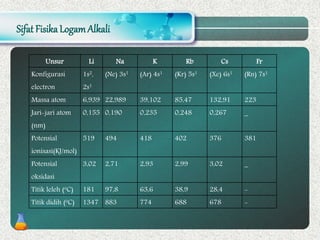
Sifat Umum Be Mg Ca Sr Ba
Nomor Atom 4 12 20 38 56
Konfigurasi Elektron [He] 2s2 [Ne] 3s2 [Ar] 4s2 [Kr] 5s2 [Xe] 6s2
Titik Leleh 1553 923 1111 1041 987
Titik Didih 3043 1383 1713 1653 1913
Jari-jari Atom (Angstrom) 1.12 1.60 1.97 2.15 2.22
Jari-jari Ion (Angstrom) 0.31 0.65 0.99 1.13 1.35
Energi Ionisasi I (KJ mol-
1)
900 740 590 550 500
Energi Ionisasi II (KJ mol-
1)
1800 1450 1150 1060 970
Elektronegativitas 1.57 1.31 1.00 0.95 0.89
Potensial Elektrode (V) -1.85 -2.37 -2.87 -2.89 -2.90
M2+ + 2e à M
Massa Jenis (g mL-1) 1.86 1.75 1.55 2.6 3.6](https://image.slidesharecdn.com/logamalkalidanalkalitanah-150914043949-lva1-app6892/85/Logam-alkali-dan-alkali-tanah-26-320.jpg)